Количество вещества, число Авогадро, молярная масса, молярный объём, уравнение связи
Тургалиева Галина Валентиновна,
Учитель химии и биологии, 1 категория.

Существует физическая величина, прямо пропорциональная числу частиц, составляющих данное вещество и входящих во взятую порцию этого вещества, которую называют количеством вещества ( ) .

Количество вещества — физическая величина, характеризующая количество однотипных структурных единиц, которые содержатся в веществе . Под структурными единицами понимаются любые частицы, из которых состоит вещество ( атомы , молекулы , ионы или любые другие частицы). Единицей измерения количества вещества в СИ служит моль . Нужно знать, что моль содержит столько же структурных частиц, сколько содержится атомов в 12г углерода
Число Авогадро ( N A )= 6,02*10 23 моль −1 .
![Молярная масса - это масса одного моля вещества . М= [ г/моль ] ( молярная масса численно равна молекулярной массе ) , отсюда](https://fsd.multiurok.ru/html/2018/12/14/s_5c136663174d6/img3.jpg)
Молярная масса
- это масса одного моля вещества .
М= [ г/моль ]
( молярная масса численно равна молекулярной массе )
, отсюда

Закон объемных отношений
Измеряя объемы, и объемы газов, в результате реакции Ж.Л. Гей-Люссак
открыл закон газовых (объемных) отношений:
«При постоянном давлении и температуре объемы вступающих в реакцию газов относятся друг к другу как небольшие простые целые числа»
Ж.Л. Гей-Люссак
1808

Например
Химическая реакция
Отношение объемов газов
Н 2 + Cl 2 2 HCl
1:1:2
2CH 4 C 2 H 2 +3H 2
2:1:3
2C+O 2 2CO
1:2
Химическая реакция
Отношение объемов газов
Н 2 + F 2 2 HF
1:1:2
2CH 4 C 2 H 2 +3H 2
2:1:3
2C+ O 2 2CO
1:2

Закон объёмных отношений позволил итальянскому учёному А. Авогадро предположить, что молекулы простых газов состоят из двух одинаковых атомов (Н 2 , N 2 , Cl 2 ,О 2 , F 2 … )
Всего лишь восемь элементов в природе существуют в виде двухатомных молекул: H 2 ; N 2 ; O 2 .
И все галогены: F 2 ; Cl 2 ; Br 2 ; I 2 ; At 2.
Молекула азота имеет такой вид :

А. Авогадро
1811
о
Итальянский ученый Амадео Авогадро сформулировал закон (для газов) :
в равных объемах различных газов при одинаковых условиях содержится одинаковое число молекул

Следствия (для газов)
- Отношение массы определённого объёма одного газа к массе такого же объёма другого газа, взятого при тех же условиях, называется плотностью первого газа по второму:
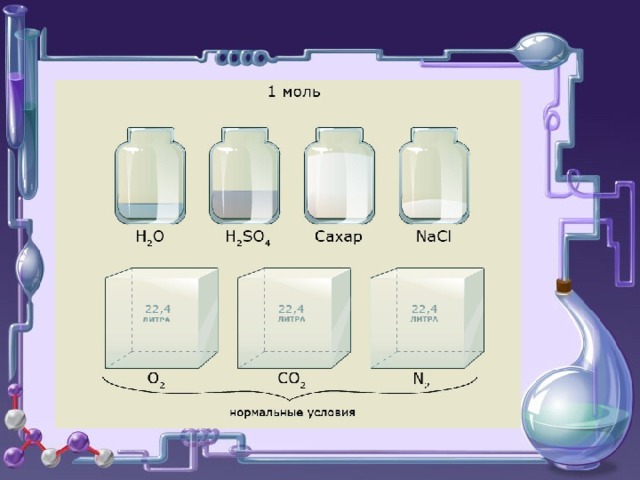
- Одно и то же число молекул различных газов при одинаковых условиях занимает одинаковые объемы.
- При н.у. 1 моль любого газа занимает объем 22,4 л.

Уравнение связи
Где n- количество вещества (моль)

Задачи (закрепление)
- Найдите число молекул в 2 молях водорода.
- Найдите массу 3 моль углекислого газа (СО2 )
- Рассчитайте массу 112 л водорода (н.у.)
- Что тяжелее: 2 моль СО2 или 2 моль СаО ?
- Найдите количество вещества серной кислоты ( H2SO4) массой 4,9 г
- Какой объем займет сернистый газ ( SO2) , масса которого равна 3,2 г?










![Молярная масса - это масса одного моля вещества . М= [ г/моль ] ( молярная масса численно равна молекулярной массе ) , отсюда](https://fsd.multiurok.ru/html/2018/12/14/s_5c136663174d6/img3.jpg)