Просмотр содержимого документа
«Урок по теме "Естественные семейства элементов"»

Естественные семейства элементов

План изучения материала урока:
1. Понятие «естественные семейства».
2. Название и нахождение в ПСХЭ.
3. Характеристика и свойства щелочных металлов.
4. Характеристика и свойства галогенов.
5. Вывод.

Естественные семейства – элементы, особенно близкие по свойствам их простых веществ.
- Естественные семейства делятся на:
- IА группа – щелочные металлы (кроме водорода)
- IIА группа – щелочноземельные металлы (кроме бериллия, магния)
- VIА группа – халькогены
- VIIA группа – галогены
- VIIA группа – благородные газы

Щелочные металлы: Li, Na, K, Rb, Cs
Физические свойства:
- Мягкие (легко режутся ножом).
- Легкие.
- Пластичные.
- Легкоплавкие.
- Хорошо проводят электрический ток.
- Обладают металлическим блеском.

Щелочные металлы: Li, Na, K, Rb, Cs
1. Реагируют с водой Ме 2 О реагируют с водой
2K +2Н 2 О = 2КОН + Н 2 К 2 О + Н 2 О = 2КОН
2. Реагируют с кислородом
2Li + O 2 = Li 2 O
3. Реагируют с хлором
2Na + CL 2 = 2NaCL
4. Реагируют с серой
2К + S = K 2 S
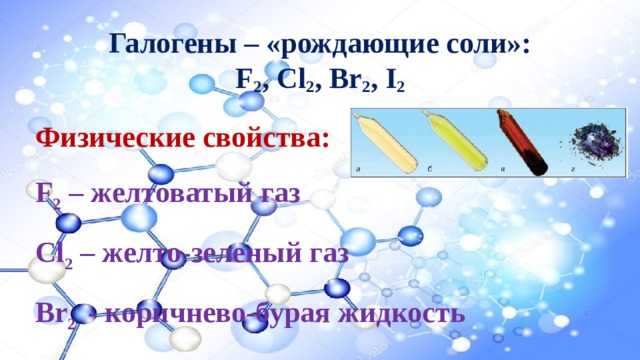
Галогены – «рождающие соли»: F 2 , Cl 2 , Br 2 , I 2
Физические свойства:
F 2 – желтоватый газ
Cl 2 – желто-зеленый газ
Br 2 - коричнево-бурая жидкость
I 2 – темно-фиолетовое твердое вещество

Галогены – «рождающие соли»: F 2 , Cl 2 , Br 2 , I 2
Химические свойства:
1. Реагируют с металлами.
2Al + 3Br 2 = 2AlBr 3
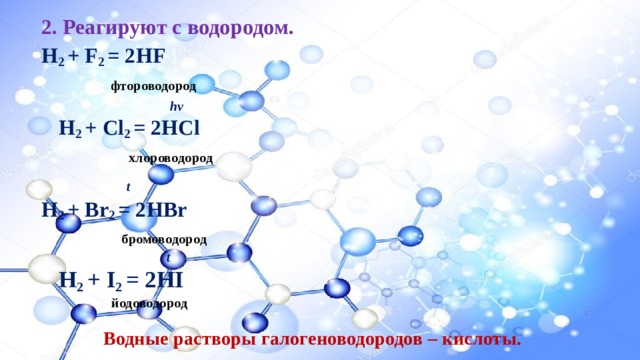
2. Реагируют с водородом.
H 2 + F 2 = 2HF
фтороводород
hv
H 2 + Cl 2 = 2HCl
хлороводород
t
H 2 + Br 2 = 2HBr
бромоводород
t
H 2 + I 2 = 2HI
йодоводород
Водные растворы галогеноводородов – кислоты.

Выводы:
- Щелочные металлы обладают наиболее ярко выраженными металлическими свойствами – типичные металлы.
- Галогены обладают наиболее ярко выраженными неметаллическими свойствами – типичные неметаллы.
- Простые вещества и однотипные соединения элементов одного семейства проявляют подобные свойства.


























