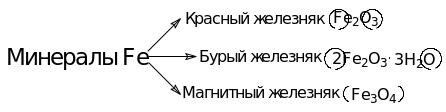Химия 9 класс
«Нахождение металлов в природе и общие способы их получения»
Цели урока:создать условия учащимся для формировния представлений о металлургии, способах получения металлов разной степени активности из минералов, горных пород и руд, ознакомить учащихся с природными соединениями металлов; развивать умение составления уравнений химических реакций.
Задачи:
- образовательные:; уметь устанавливать причинно-следственные связи смежду «составом», «химическими свойствами» и «получением металла»;
- развивающие:развитие умений сравнивать, обобщать, правильно формулировать задачи и излагать мысли; развитие логического мышления, внимания и умения работать в проблемной ситуации;
- воспитательные:формирование у учащихся познавательного интереса к химии; воспитание таких качеств характера, как настойчивость в достижении цели, интереса и любви к предмету через содержание учебного материала, умение работать в коллективе, взаимопомощи, культуры общения.
Планируемые результаты:
Предметные:
- научатся: составлять уравнения реакций, лежащих в основе получения металлов;
- получат возможность научиться: приводить примеры уравнений реакций, лежащих в основе промышленных способов получения чугуна и стали.
Метапредметные:
- регулятивные: учитывают правило в планировании и контроле способа действия;
- познавательные: используют поиск необходимой информации для выполнения учебных заданий с использованием учебной литературы;
- коммуникативные: учитывают разные мнения и стремятся к координации различных позиций в сотрудничестве.
Личностные:появляется гордость за российскую науку
Термины:металлургия, руды, минералы, гидрометаллургия, пирометаллургия, электрометаллургия.
Тип урока:урок формирования новых знаний.
Ход урока
1. Организационный момент(мотивация учащихся к активной познавательной деятельности). Учитель Приветствует учащихся, отмечает отсутствующих.
2. Актуализация знаний. Проверка домашнего задания. Учитель просит учащихся собрать рабочие тетради для проверки домашнего задания за это время раздает им карточки с заданиями на 15-20 минут.
Проверочная работа: «Общие химические свойства металлов»
Закончите уравнения возможных реакций:
а) S + O2 = SO2;
б) Si + 2NaOH + Н2O = Na2SiO3 + 2Н2;
в) 2Р + 3Mg = Mg3P2;
г) РН3 + 2O2 = Н3РO4;
д) 4NO2 + 2Н2O + O2 = 4HNO3.
3. Объяснение материала (формирование научного типа мышления, владения химической терминологией). Учитель сообщает тему и цели урока. Учащиеся записывают тему урока в тетрадях.
Учитель: Как вы думаете, ребята, в каком виде встречаются металлы в природе?
Учащиеся: Металлы встречаются в природе в самородном и связанном виде.
Учитель: Оказывается, о нахождении металла в природе можно судить в зависимости от его расположения в ряду напряжений.
Для наглядности и легкого запоминания учитель предлагает схему «Металлы в природе»
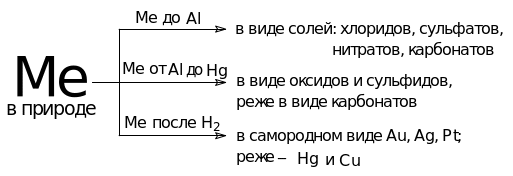
Схема 2. Металлы в природе
Учитель: Обращает внимание учащихся на схему «Металлы в природе» и подводит итог: большинство металлов в природе существует в связанном состоянии, т.е. в виде различных природных соединений. Химические природные соединения металлов называют минералами. Минералы в основном встречаются в виде оксидов либо в виде сульфидов.
Например:
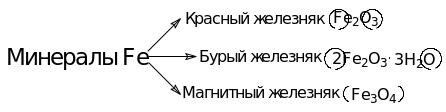

Схема 3. Минералы железа Схема 4. Сульфидные минералы
Минералы входят в состав горных пород и руд.
Природные образования, содержащие минералы металлов, пригодные для промышленного получения из них металлов, называют рудами. Наука о получении металлов из руд называется металлургией. В зависимости от способа извлечения металла из руды выделяют следующие виды металлургических процессов:
1.Пирометаллургия – это метод извлечения металлов из руд под действием высоких температур.
Сульфидные руды подвергают обжигу:
2CuS + 3O2 → 2CuO + 2SO2
Оксидные руды и оксиды восстанавливают водородом, углем, угарным газом, более активными металлами – алюминием (алюминотермия), магнием (магнийтермия).
CuO + C → Cu + CO
2Al + Cr2O3→ 2Cr + Al2O3
2.Гидрометаллургия – это метод получения металлов, основанный на химических реакциях, происходящих в растворах. Гидрометаллургия включает 2 способа:
a). Получение из различных руд растворимых солей металла
CuS + 4H2SO4(конц.) → CuSO4 + 4SO2 + 4H2O
б). Восстановление металла из раствора соли с помощью различных восстановителей (H2, C, CO, Me)
CuSO4 + Fe → FeSO4+ Cu
3.Электрометаллургия – это метод получения металлов из их солей, и оксидов под действием электрического тока.
2Al2O3(расплав) → 4Al + 3O2
2NaCl(расплав) → 2Na + Cl2
Металлы, стоящие в ряду напряжений до алюминия включительно, можно получить электролизом только расплавов оксидов и солей. Менее активные металлы можно восстановить электрическим током из растворов солей.
2CuSO4 + 2H2O → 2Cu + 2H2SO4 + O2↑
4. Домашнее задание: записи в тетрадях и задания:
1). Предложите технологическую цепочку производства свинца из минерала галенита PbS. Запишите уравнения реакций.
2). Сколько килограммов меди получается из 120т обогащенной горной породы, содержащей 20% сульфида меди (I), если выход меди составляет 90% от теоретически возможного?
5. Рефлексия:
С какими трудностями вы столкнулись при изучении этой темы и как вы решили эту проблему?
Что вам было интересно на уроке?
Что не понравилось?
Что нового вы узнали для себя?