Просмотр содержимого документа
«Урок-презентация "Белки." Химия 10 класс.»

Белки
Химия 10 класс
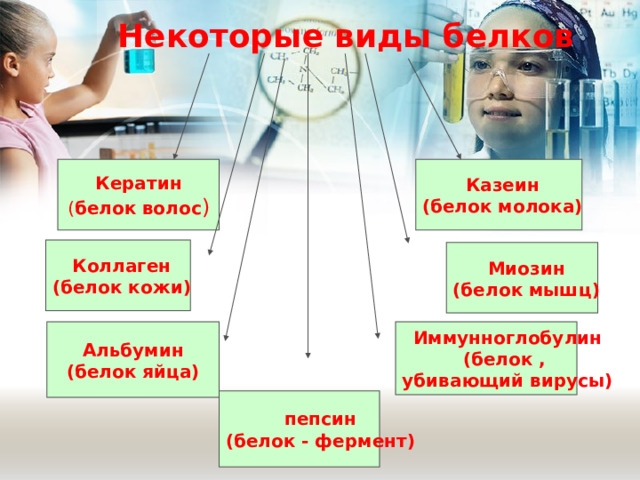
Некоторые виды белков
Казеин
Кератин
(белок молока)
( белок волос )
Коллаген
(белок кожи)
Миозин
(белок мышц)
Иммунноглобулин
Альбумин
(белок яйца)
(белок ,
убивающий вирусы)
пепсин
(белок - фермент)
1

Как устроен белок?
С 3032 Н 4816 О 872 N 780 Fe 4
гемоглобин
«Жизнь есть способ существования белковых тел…»
(Ф.Энгельс)
Белки – это биополимеры, состоящие из мономеров, которыми являются аминокислоты соединенные пептидной связью.
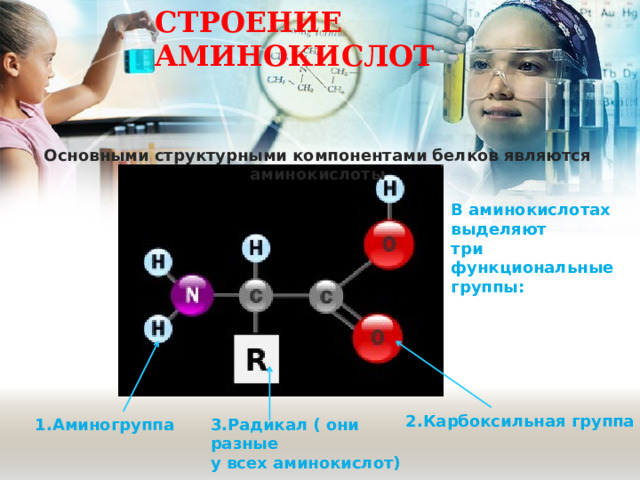
СТРОЕНИЕ АМИНОКИСЛОТ
Основными структурными компонентами белков являются аминокислоты
В аминокислотах
выделяют
три функциональные
группы:
2.Карбоксильная группа
3.Радикал ( они разные
у всех аминокислот)
1.Аминогруппа

Образование пептидной связи
Аминокислоты могут реагировать друг с другом: карбоксильная группа одной аминокислоты реагирует с аминогруппой другой аминокислоты с образованием пептидной связи и молекулы воды.
NH 2 – CH 2 – COOH + NH 2 – CH 2 – COOH =
NH 2 – CH 2 – CO – NH – CH 2 – COOH + H 2 O
Связь – CO – NH – , соединяющая отдельные аминокислоты в пептид, называется пептидной.

Белки
Сложные могут включать:
- ионы металла (металлопротеиды)
-пигмент (хромопротеиды),
-комплексы с липидами (липопротеины),
нуклеиновыекислоты(нуклеопротеиды),
-остаток фосфорной кислоты (фосфопротеиды),
-углевод (гликопротеины)
Простые:
Состоят только из
аминокислотных
остатков

Структура белка
Первичная структура – это полипептидная цепь линейной формы из последовательно соединенных пептидной связью (– CO – NH –) аминокислот.
– NH – CH – CO – NH – CH – CO – NH – CH –
R 1 R 2 R 3
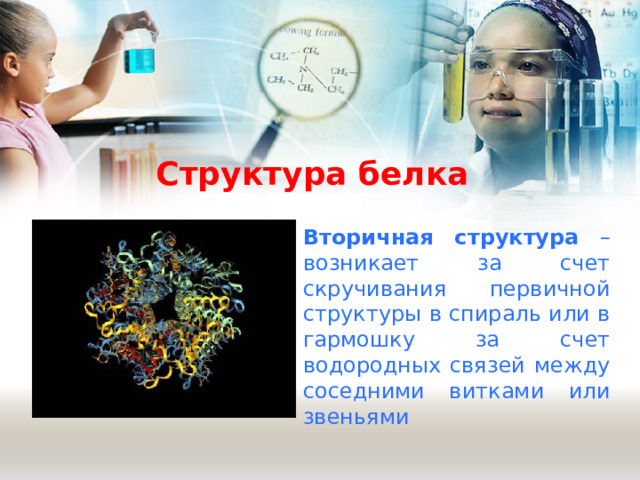
Структура белка
Вторичная структура – возникает за счет скручивания первичной структуры в спираль или в гармошку за счет водородных связей между соседними витками или звеньями

Структура белка
Третичная структура – это глобулярная форма, образующаяся за счет гидрофобных связей между радикалами аминокислот вторичной структуры

Структура белка
Четвертичная структура – представляет собой объединение нескольких глобул с третичной структурой в единый комплекс
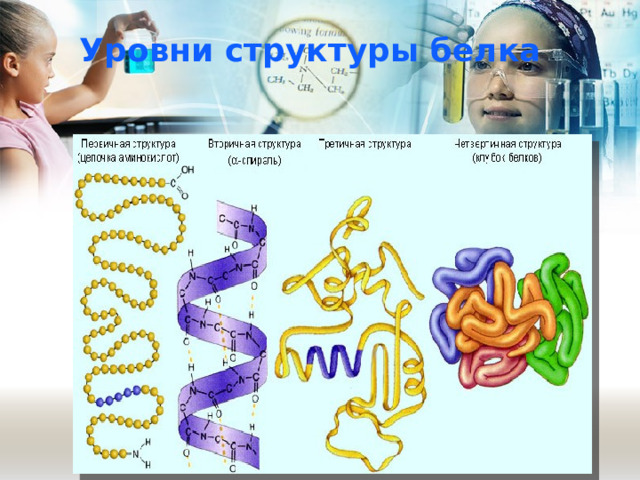
Уровни структуры белка

Свойства белков
Белки могут быть как растворимы, так и нерастворимы в воде в зависимости от их состава и структуры.

Свойства белков
Водорастворимые белки образуют коллоидные растворы, белок в воде набухает и его объём увеличивается – это гидратация

Свойства белков
- Кислоты, щелочи и высокая температура разрушают структуру белков и приводят к их денатурации .
- Белки также денатурируют под действием спирта и тяжелых металлов.
Денатурация
ОБРАТИМАЯ
Если сохранена
первичная структура
НЕОБРАТИМАЯ
Если первичная
структура разрушена

Свойства белков
- Гидролиз- разложение белков на аминокислоты под действием воды и ферментов
Аминокислота-метионин

Свойства белков
- Горение- образуются углекислый газ, вода и азот (запах жженых перьев)

Свойства белков
- Пенообразование - белки способны образовывать системы: жидкость-газ

Свойства белков
- Поместите кусочек прессованного творога в пробирку и добавьте несколько капель азотной кислоты. Осторожно нагрейте.
(Ксантопротеиновая реакция)

Свойства белков
- Налейте в пробирку 2 мл яичного белка. Добавьте такой же объем концентрированного раствора гидроксида натрия и несколько капель раствора сульфата меди (II).
(Биуретовая реакция)

Функции белков
Функция
Определение
1. Строительная
Пример
Материал клетки
2. Транспортная
Переносят различные вещества
Кератин, коллагены
3. Защитная
4. Каталитическая
Обезвреживают защитные вещества
Гемоглобин
Ускоряют протекание химических реакций в организме
5. Двигательная
Иммуноглобулины
Ферменты
Выполняют все виды движений
6. Регуляторная
Регулируют обменные процессы
Миозин, актин
Гормоны