Отгадайте о чём идёт речь
Я, газ, легчайший и бесцветный,
Неядовитый и безвредный,
Соединяясь с кислородом,
Я для питья даю вам воду!

Тема урока «Водород» План урока
1. Водород в природе.
2. Историческая справка.
3. Водород – химический элемент.
4. Водород – простое вещество.
5. Получение и собирание водорода.
6. Физические свойства водорода.
7. Применение водорода.

Водород в природе.
Первый я на белом свете:
Во вселенной, на планете
Превращаюсь в лёгкий гелий,
Зажигаю Солнце в небе.
Гость из космоса пришёл
В воде приют себе нашёл!
(Объясните смысл этого стихотворения изучив материал учебника нахождение водорода в природе стр. 71)
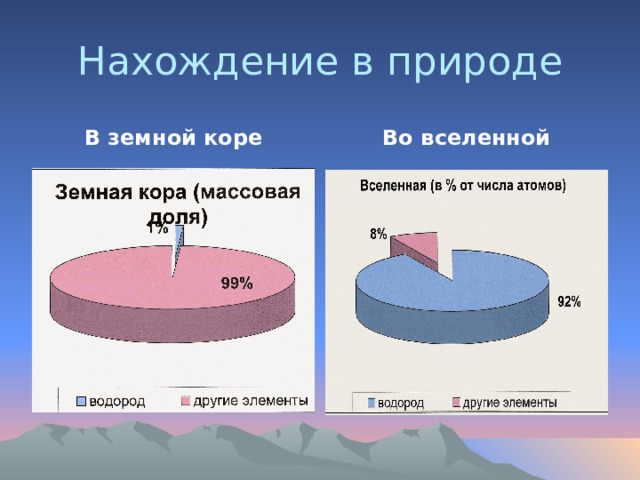
Нахождение в природе
В земной коре
Во вселенной
Исторические сведения
- Водород был известен ещё в XVI веке Теофрасту Парацельсу (1493-1541)
- Его получали Ван-Гельмонт(1577-1644),
Роберт Бойль (1627-1691),
Николя Лемери (1645-1715),
Михаил Васильевич Ломоносов (1711-1765),
Джозеф Пристли и др.

Всё те же открытия.
- В 1766 году известный английский учёный Генри Кавендиш получил «искусственный воздух» действием цинка на разведённую соляную кислоту. Это было совершенно новое вещество, которое хорошо горело и получило название «горючего воздуха»

Открытие водорода
- Лишь в 1787 году Антуан Лавуазье доказал, что «горючий воздух»,открытый в 1766 году входит в состав воды и дал ему название «гидрогениум», т.е. «рождающий воду», «водород».

Водород – химический элемент.
Характеристика водорода по периодической системе.
- 1. Порядковый номер.
- 2. Номер периода.
- 3. Номер группы.
- 4. Относительная атомная масса.
- 5. Валентность водорода.

Водород – простое вещество.
Н 2

Водород как простое вещество и как химический элемент
Параметры сравнения
Химический элемент
Химическая формула
Простое вещество
Н
Относительная атомная или молекулярная массы
A r(H) = 1
Н 2
Свойства
M r (H 2 ) =2
Входит в состав простых и сложных веществ .
Обладает набором физических и химических свойств.

Ответьте на вопрос.
- Если бы перед вами стояла задача получить большое количество водорода, какое сырьё вы бы выбрали и почему ?

Получение водорода из воды с помощью солнечной энергии

Получение водорода
В промышленности :
2СН 4 + О 2 = 2СО + 4Н 2 ↑
2H 2 O = 2H 2 ↑ + O 2 ↑
В лаборатории :
Zn + H 2 SO 4 = ZnSO 4 + H 2 ↑

Получение водорода в лаборатории
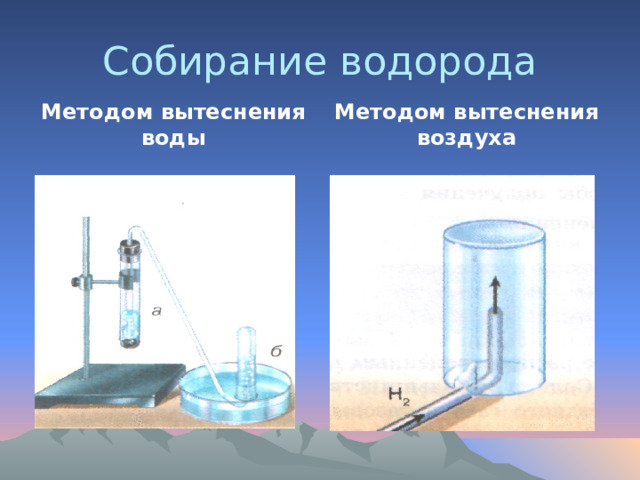
Собирание водорода
Методом вытеснения воды
Методом вытеснения воздуха

А сейчас - физминутка !

Образование гремучей смеси
Обычно лёгок и летуч,
Он вдруг становится могуч:
Его нагрев неосторожно
Взорвать в округе всё возможно.

Физические свойства водорода
- Лёгкий горючий газ без цвета, запаха и вкуса.
- Температура плавления -259,15
- Температура кипения -252,7
- Плохо растворим в воде.

Некоторые области применения водорода

Применение водорода
Водородом заполняли дирижабли вплоть до 1937 года, пока не взорвался немецкий дирижабль «Гинденбург». Погибло 36 человек. Размеры дирижабля достигали размеров двух футбольных полей.

Водород в качестве горючего

Водород – аккумулятор энергии

Если вы согласны с утверждениями, поставьте плюс.
- 1. Я узнал много нового и интересного.
- 2. На все возникшие в ходе урока вопросы я получил ответы.
- 3. Мне это пригодится в будущей профессиональной деятельности и в повседневной жизни.
- 4. Считаю, что работал добросовестно и достиг цели урока.

Спасибо за урок!
Запишите домашнее задание.
Стр.71 – 74(читать)
Подготовить сообщения по темам:
«Водород во Вселенной»,
«Старинные способы получения водорода»,
«Из истории развития воздухоплавания».