Урок химии по теме "Основания".
Дата: 24.12.16г.
Класс: 8а
Цель урока: знакомство с классом неорганических веществ - основаниями.
Метапредметные:
способствовать развитию познавательной деятельности;
логического мышления;
умения сравнивать, обобщать, делать выводы.
Предметные:
дать определение основания, как класса неорганических веществ;
отработать навыки классификации оснований по растворимости;
закрепить навыки определения степени окисления в сложных веществах и составлять формулу по степени окисления;
познакомить учащихся с составом, классификацией и представителями класса оснований;
продолжить формирование знаний об ионах на примере сложных гидроксид-ионов;
дать понятие о качественных реакциях и индикаторах;
формировать навыки обращения с химической посудой и реактивами;
формировать бережное отношение к своему здоровью.
Реактивы и оборудование:
кристаллические щелочи и их растворы (КОН, NaOH),
Са(ОН)2 – "известковая вода", гашеная известь;
индикаторы: лакмус, метилоранж, фенолфталеин;
гидроксид алюминия– порошок.
Ход урока
Перед уроком раздаю инструктивные карточки и опорные конспекты, а также таблицы по рефлексии.
1. Приветствие.
2. Проверка домашнего задания.Урок начинается с проверки домашнего задания.
Учащимся предлагаются карточки (2 варианта), в карточке 6 формул (необходимо определить класс вещества, назвать вещество и определить степень окисления каждого элемента). На выполнение работы 5-7 минут.
Работы сдаются учителю, а 2 ученика выходят к доске проверить ответы (у учащихся есть возможность оценить свои знания самостоятельно).
3. Актуализация знаний.
(Слайд 1.) Тема урока не объявляется ???????
Учащимся предлагается выполнить задание
(слайд № 2) на электронной доске высвечиваются формулы:
СO2
NaOH
Fe2О3
Ca(OH)2
K2O
Al(OH)3
ЗАДАНИЕ выписать в тетрадь бинарные соединения, назвать их (проверяем)
??????? - Какой класс соединений остался?
4. Изучение новой темы.
Давайте попробуем разобраться, что это за вещества. Кроме бинарных соединений, существуют сложные вещества, которые состоят из трех элементов.
В течение урока нам с вами предстоит составить опорный конспект и презентацию, которую можно использовать для объяснения в других классах. Работать вы будете в парах.
Вы видите, что названия темы в опорном конспекте нет. Чтобы разобраться, что это за вещества и как они называются, предлагаю ответить на 1 блок вопросов в ваших инструктивных карточках и составить по ним схему в опорном конспекте.
1. Что стоит на первом месте у этих соединений?
2. Что стоит на втором месте? Чем похожи эти вещества?
Данный класс веществ называется ОСНОВАНИЯ (запишите в конспект). Проверяем и заносим ответы в презентацию.(слайд 3)
А что это за группа такая ОН? Как она называется? И какова степень окисления у этой группы атомов? Ответьте на 2 блок вопросов, ответы запишите в конспект.
II. 1. Из каких элементов состоит группа -ОН?
Н – гидрогениум
О – оксигениум
2. Зная латинские названия, попробуйте составить название -ОН группы, исходя из того, что сначала называют корень последнего в формуле элемента, а затем впереди стоящего. В конце записывается слово группа.
3. Зная степени окисления каждого из элементов этой группы, попробуйте определить общую степень окисления этой группы атомов. Для этого можно взять –ОН в скобки и написать степень окисления за скобками.
(Проверяем, заносим в презентацию слайд 4)
Настало время дать определение данному классу веществ. Для этого ответьте на вопросы 3 блока и запишите ответы в опорный конспект.
III. 1. Это простые или сложные вещества?
2. Что стоит на первом месте?
3. Что стоит на втором месте и сколько их?
4. На основании определения составьте общую формулу оснований
(Проверяем, заносим в презентацию слайд 5,6)
Давайте попробуем составить формулы оснований:
Гидроксид натрия
Гидроксид калия
Гидроксид кальция
Гидроксид алюминия
В названии основания гидроксогруппа будет иметь название ГИДРОКСИД. Прошу вас записать формулы оснований. Ответьте на 4 блок вопросов.
IV.Гидроксид натрия, гидроксид калия, гидроксид кальция, гидроксид алюминия.
(Проверяем, заносим в презентацию слайд 7)
А теперь давайте рассмотрим физические свойства оснований. Предлагаю вам рассмотреть образцы оснований у вас на столах и ответить на вопросы 5 блока.
V.1. Какого цвета выданные вещества?
2. Какое агрегатное состояние у выданных веществ?
3. Растворимы ли они в воде? (посмотрите демонстрацию растворимости и на основании увиденного заполните схему).
Давайте рассмотрим образцы оснований и проверим, как они растворяются в воде.
Демонстрационный опыт "Растворимость оснований"
(Проверяем, заносим в презентацию слайд 8,9)
Есть еще один источник позволяющий нам узнать растворимо основание или нет - это таблица растворимости (объяснить как ею пользоваться)
А как отличить прозрачный бесцветный раствор гидроксида кальция (известковую воду) – от других подобных растворов?
Демонстрационный опыт
продуть через гидроксид кальция углекислый газ –(что наблюдаете?) наблюдаем помутнение раствора.
(слайд№10) Такиереакции, в результате которых доказывается наличие данного вещества или иона, называются КАЧЕСТВЕННЫМИ. (записать в опорный конспект!!!)
Это доказательство воспринимается нами в виде образовавшегося осадка или газа, появления запаха или изменение цвета.
Вещество, с помощью которого доказывается наличие другого вещества называетсяреактивом на распознаваемое вещество. В нашем случае углекислый газ является реактивом на «известковую воду».
Реактивы могут быть не только на одно вещество, но и на целую группу или класс веществ. Так щелочи можно распознать с помощью особых реактивов – ИНДИКАТОРОВ ( указателей)
Индикаторы меняют окраску в зависимости от среды раствора.
Давайте посмотрим , как ведут себя индикаторы в разных средах
Лабораторные опыты
На столах у учащихся стоят наборы индикаторов и 6 пронумерованных пробирок.
Учащимся предлагается повторить правила техники безопасности при работе с реактивами и приступить к выполнению работы по инструктивным карточкам.
Инструктивная карточка.
Вспомните правила техники безопасности при работе с химическими реактивами.
Определите, кто будет выполнять опыт.
Прочитайте внимательно задание .
Выполните задание в соответствие с требованиями в инструктивной карточке.
В пробирку под номером 1и 2 капните по 1-2 капли лакмуса
В пробирку под номером 3 и 4 капните по 1-2 капли м/о
В пробирку под номером 5 и 6 капните по 1-2 капли ф/ф
Что вы наблюдаете? Свои наблюдения сравните с таблицей в учебнике.
После выполнения лабораторного опыта проводим обсуждение и вывод.Учащиеся отмечают, как изменяется цвет индикатора в щелочной среде, а в нейтральной цвет индикатора сохраняется
(слайд № 11)
| Индикатор | Нейтральная среда | Щелочная среда |
| Лакмус | фиолетовый | синий |
| Метиловый оранжевый | оранжевый | желтый |
| Фенолфталеин | бесцветный | малиновый |
А теперь я предлагаю вам заслушать доклад о значении и применении оснований и кратко отметить это в опорном конспекте.
(Проверяем, заносим в презентацию слайд 12)
Рефлексия.
Итак, мы с вами добрались до финиша. Вы много нового сегодня узнали, поэтому попытайтесь честно ответить на вопросы таблицы, поставив плюс в той колонке, которая, наиболее реально соответствует вашему уровню усвоения сегодняшнего материала.Карточки раздаются в начале урока.
| | Все понял | Частично понял | Ничего не понял |
| 1. Состав оснований | | | |
| 2. Название оснований | | | |
| 3. Составление формул по названию | | | |
| 4. Классификация оснований | | | |
| 5. Качественная реакция на основания Са(ОН)2 | | | |
| 6. Взаимодействие с индикаторами | | | |
| 7. Применение и значение | | | |
Домашнее задание: п.19, вопросы 4,5 (слайд 13)
В конце урока, если остается время, можно просмотреть полученную презентацию, тем самым обобщив знания, полученные на уроке.
Используемая литература:
Габриелян О.С. Химия. 8 класс: учебник для общеобразовательных учебных заведений. – 4-е изд., стереотип. – М.: Дрофа, 2002.
Алексинский В.Н. Занимательные опыты по химии: книга для учителя – 2-е изд.– М.: Просвещение, 1995.
Аликберова Л. "Занимательная химия: книга для учащихся, учителей и родителей. – М.: АСТ–ПРЕСС, 1999.
Степин Б.Д., Аликберова Л.Ю. "Книга по химии для домашнего чтения. – 2-е изд. – М.: Химия, 1995.







 Опорный конспект Дата:
Опорный конспект Дата: 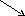


 По растворимости воде
По растворимости воде