
Атомы, молекулы и ионы

Демокрит (около 460 до н.э— около 360 до н. э.) древнегреческий философ.
Основоположник
атомистического учения.
Ввел термин «атом»

М.В . Ломоносов
(1711-1765)
Вошёл в науку как первый химик, обосновал учение об атомах и молекулах, дал определение физической химии , весьма близкое к современному, и предначертал обширную программу физико-химических исследований
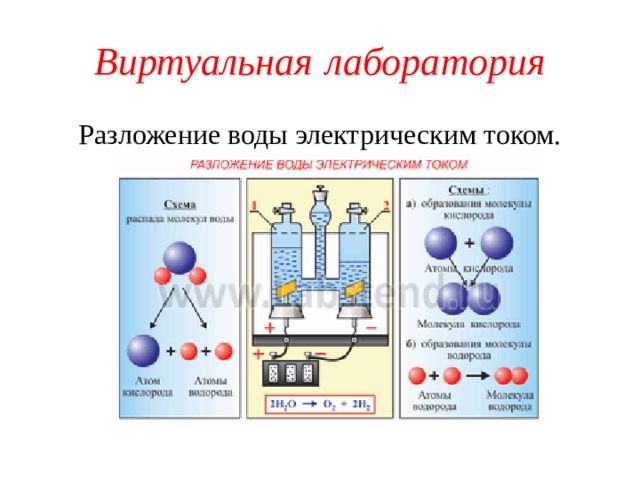
Виртуальная лаборатория
Разложение воды электрическим током.
- Атом - это мельчайшая, химически неделимая электронейтральная частица, состоящая из положительно заряженного ядра и отрицательно заряженных электронов.
- Молекулы –это наименьшие частицы многих веществ, способная существовать самостоятельно и сохранять его химические свойства.

Положения атомно-молекулярного учения
1. Вещества состоят из атомов;
2. При взаимодействии атомов образуются простые и сложные молекулы;
3. При физических явлениях молекулы сохраняются, их состав не изменяется; при химических – разрушаются, их состав изменяется;
4. Молекулы веществ состоят из атомов; при химических реакциях атомы в отличие от молекул сохраняются;
5. Атомы одного элемента сходны друг с другом, но отличаются от атомов любого другого элемента;
6. Химические реакции заключаются в образовании новых веществ из тех же самых атомов, из которых состояли исходные вещества.

Тема урока: Вещества молекулярного и немолекулярного строения. Типы кристаллических решеток.

Агрегатные состояния вещества
Вода
t пл= 0 ° C
t кип=10 0 ° C
ГАЗООБРАЗНОЕ
ТВЕРДОЕ
ЖИДКОЕ

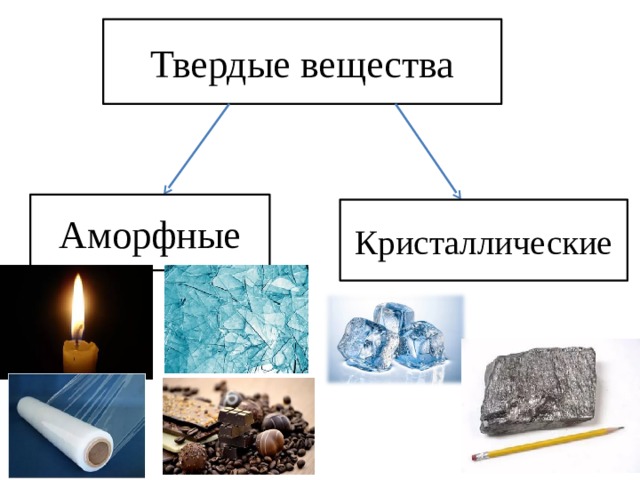
Твердые вещества
Аморфные
Кристаллические
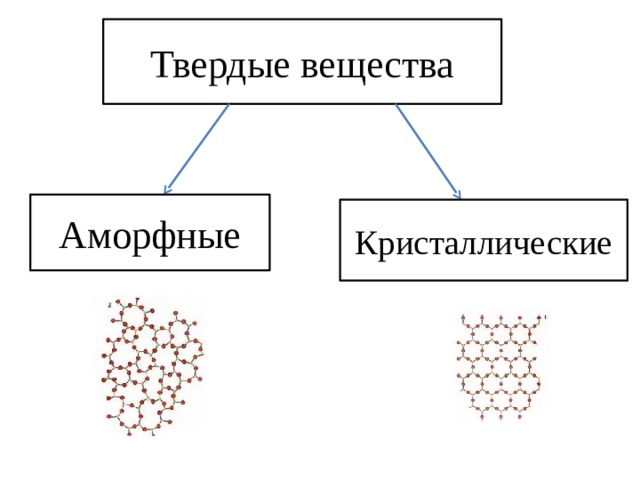
Твердые вещества
Аморфные
Кристаллические
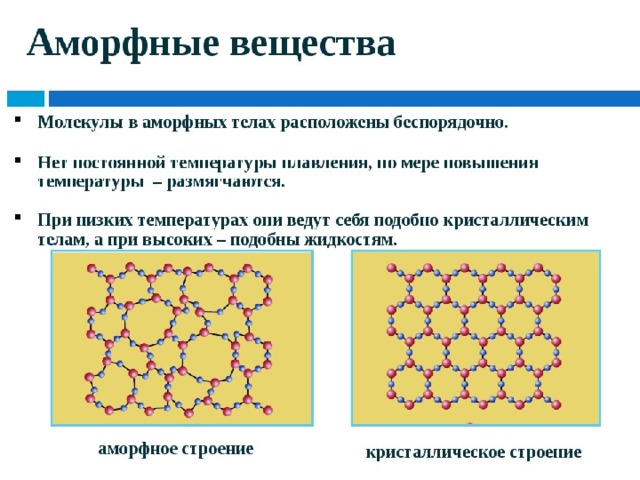
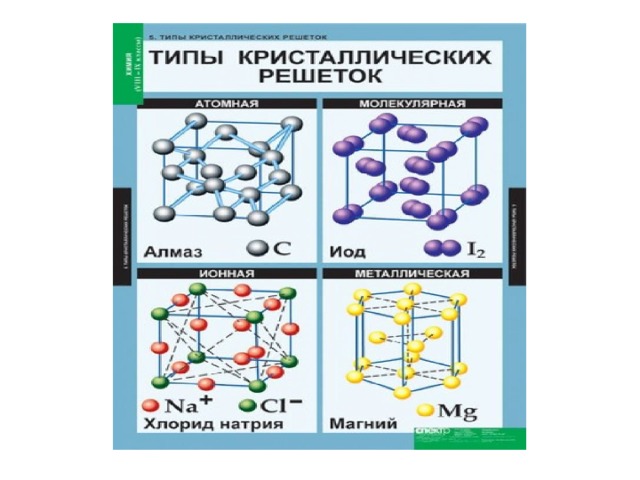
Тип решётки
Виды частиц
в узлах решётки
Вид связи между частицами
Примеры веществ
Физические свойства веществ
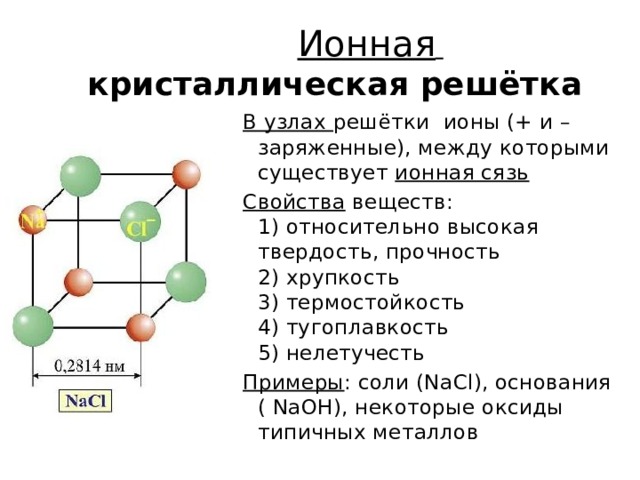
Ионная кристаллическая решётка
В узлах решётки ионы (+ и – заряженные), между которыми существует ионная сязь
Свойства веществ: 1) относительно высокая твердость, прочность 2) хрупкость 3) термостойкость 4) тугоплавкость 5) нелетучесть
Примеры : соли (NaCl), основания ( NaOH), некоторые оксиды типичных металлов
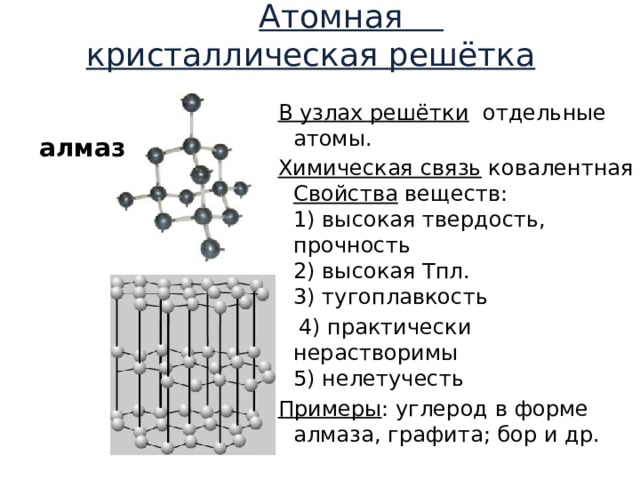
Атомная кристаллическая решётка
В узлах решётки отдельные атомы.
Химическая связь ковалентная Свойства веществ: 1) высокая твердость, прочность 2) высокая Тпл. 3) тугоплавкость
4) практически нерастворимы 5) нелетучесть
Примеры : углерод в форме алмаза, графита; бор и др.
алмаз
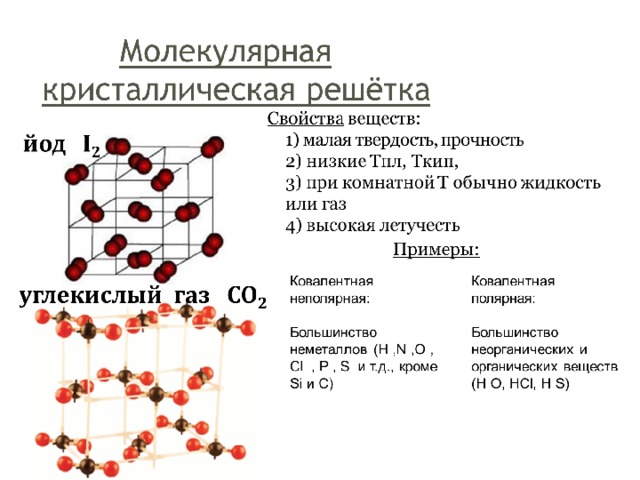
Вещества бывают молекулярного и немолекулярного строения.
Молекулярные вещества -это вещества , мельчайшими структурными частицами которых являются молекулы.
молекула кислорода
молекула воды

Молекулярные вещества имеют:
- Низкие температуры плавления и кипения;
- Находятся в стандартных условиях в твердом, жидком или газообразном состоянии;
- Например:
вода - жидкость; t пл = 0 o С; t кип = 100 o С;
кислород - газ; t пл = -219 o С; t кип = -183 o С;
оксид азота(V)- твердое в-во;t пл = 30,3 o С; t кип = 45 o С;

!!! К молекулярным веществам относятся:
- большинство простых веществ неметаллов: О 2, S 8 ,P 4 , H 2 , N 2 , Cl 2
- соединения неметаллов друг с другом( бинарные и многоэлементные): NH 3, СО 2, H 2 SО 4,

Немолекулярные вещества - это вещества, мельчайшими структурными частицами которых являются атомы или ионы.
Немолекулярные вещества :
- находятся в стандартных условиях в твердом состоянии;
- имеют в стандартных условиях высокие температуры плавления и кипения;
Например:
натрий хлорид- твердое в-во; t пл = 801 o С; t кип = 1465 o С;
медь твердое в-во; t пл = 1083 o С; t кип = 2573 o С;

К немолекулярным веществам относятся:
-простые вещества металлы и их сплавы: Cu, Na, Fe;
-соединения металлов с неметаллами: NaH, Na 2 SO 4 ,CuCl 2
- неметаллы: бор, кремний, углерод(алмаз) и фосфор(красный и черный)
- некоторые бинарные соединения неметаллов: SiC,SiO 2
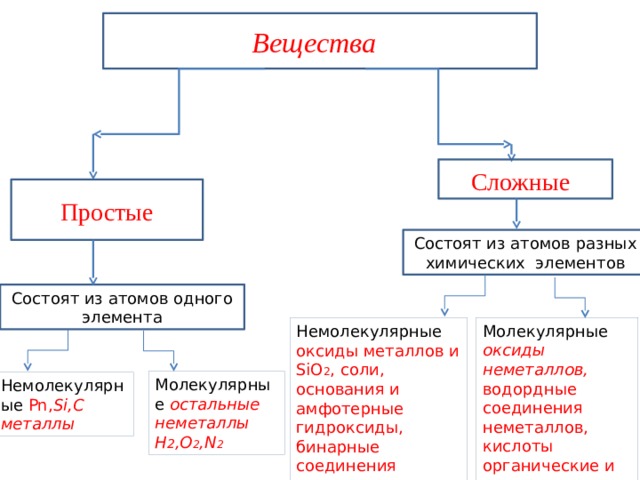
Вещества
Сложные
Простые
Состоят из атомов разных химических элементов
Состоят из атомов одного элемента
Молекулярные оксиды неметаллов, водордные соединения неметаллов, кислоты органические и неорганические
Немолекулярные оксиды металлов и SiO 2 , соли, основания и амфотерные гидроксиды, бинарные соединения металлов и неметаллов.
Молекулярные остальные неметаллы H 2 ,O 2 ,N 2
Немолекулярные Рn, Si,C
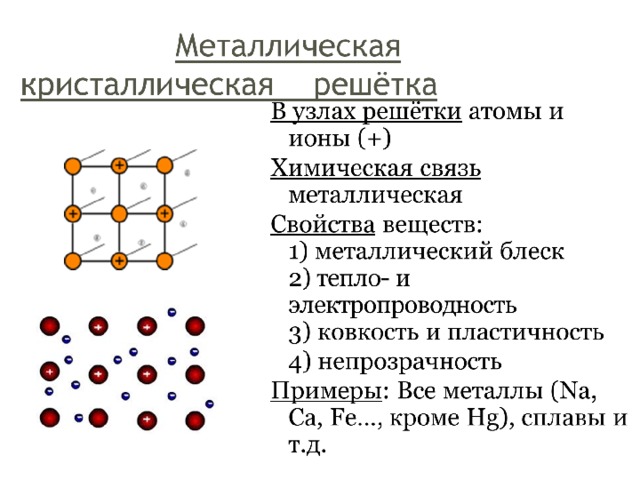
металлы

Виртуальная лаборатория
Получение сульфида железа

Сопоставление
Смесь
Химическое соединение
- Вещества можно смешать в любых массовых отношениях, т.е. состав смесей переменный .
- Вещества водящие в состав смесей, сохраняют свои свойства.
- Вещества входящие в состав смеси, можжно разделить физическими способами
- Механическое смешивание не сопровождается выделением теплоты или другими признаками химических реакций
- Состав химических соединений постоянный.
- Вещества образующие соединения, свои свойства не сохраняют, таккак получается химическое соединение с другими свойствами.
- Химическое соединение можно разложить с помощью химических реакций.
- Об образовании химических соединений можно судить по признакам химических реакций.

Закрепление
- 1. Допишите приведенные ниже предложения, заменив многоточия подходящими по смыслу понятиями «химический элемент», «атом», «молекула»: а) ... кислорода состоят из ... одного ... . б) ... кислорода содержит два ... . в) В состав ... воды входят ... двух ..., одним из которых является кислород. г) ... кислорода входят в состав воздуха.
- 2. Какие неточности допущены в выражении: «В соке антоновских яблок много железа»? В каком виде находится железо в яблочном соке?

- 3. Из приведенного перечня: сера, железо, сульфид железа, вода дистиллированная, вода минеральная, вода речная — выпишите названия веществ, состоящих из:
- а) атомов одного химического элемента; б) атомов разных химических элементов; в) смесей. 4. Используя слово «медь» , составьте два предложения, в одном из которых говорится о меди как простом веществе, в другом — о меди как химическом элементе.

Домашняя работа
- Параграф 4,5 упр. 11, 12, 13.















































