
Повторение по теме «ОКСИДЫ»
8 класс

Составьте формулы таких оксидов:
Fe 2 O 3
а) оксид железа (III)
б) оксид серы (IV)
в) оксид лития
г) оксид кремния (IV)
SO 2
Li 2 O
SiO 2

Назовите формулы оксидов
H 2 SO 4 , CaO, CuCl 2 , P 2 O 5 , BaO, SO 3 , Na 2 CO 3 , Na 2 O, N 2 O 5 , NaOH, Na 2 O, Cu(OH) 2.

Укажите формулу кислотного оксида.
А. К 2 О
Б. SiO 2
В. SrO
Г. СО

2. Укажите формулу несолеобразующего оксида.
Б. Аl 2 О 3
В. СО 2
Г. N 2 O

3. Укажите формулу амфотерного оксида.
А. К 2 О
Б. Аl 2 О 3
В. SO 2
Г. СО

4. Укажите формулу основного оксида.
А. СаО
Б. Н 2 О
В. Аl 2 О 3
Г. SO 2

ВОДОРОД. ПОЛУЧЕНИЕ И ХИМИЧЕСКИЕ СВОЙСТВА
8 КЛАСС
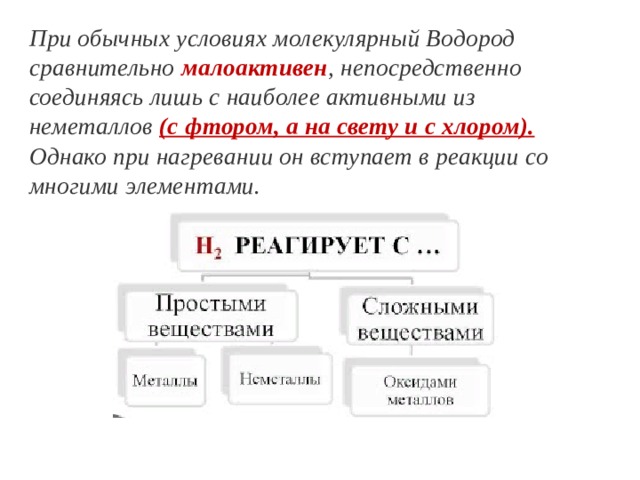
При обычных условиях молекулярный Водород сравнительно малоактивен , непосредственно соединяясь лишь с наиболее активными из неметаллов (с фтором, а на свету и с хлором). Однако при нагревании он вступает в реакции со многими элементами.
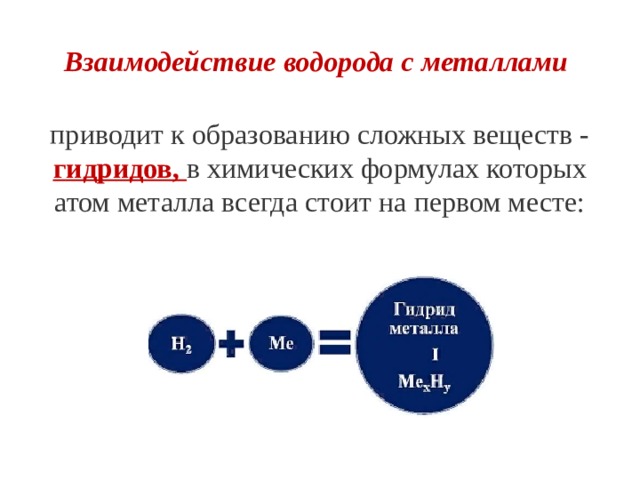
Взаимодействие водорода с металлами
приводит к образованию сложных веществ - гидридов, в химических формулах которых атом металла всегда стоит на первом месте:

При высокой температуре Водород непосредственно реагирует с некоторыми металлами (щелочными, щелочноземельными и другими), образуя белые кристаллические вещества - гидриды металлов (LiН, NaН, КН, СаН 2 и др.)
Н 2 + 2Li = 2LiH
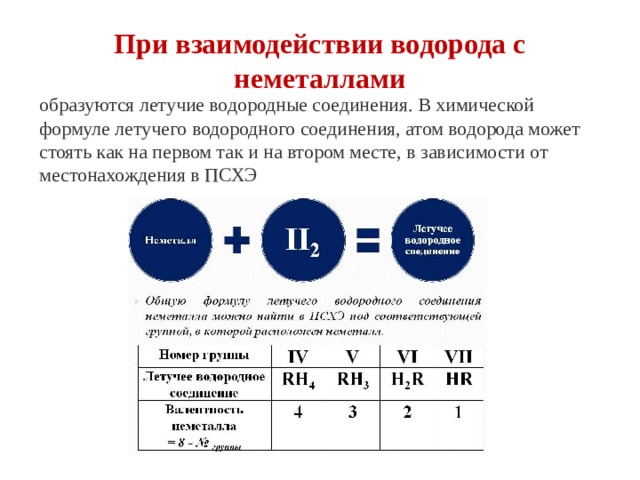
При взаимодействии водорода с неметаллами
образуются летучие водородные соединения. В химической формуле летучего водородного соединения, атом водорода может стоять как на первом так и на втором месте, в зависимости от местонахождения в ПСХЭ
С кислородом водород образует воду:
2Н 2 + О 2 = 2Н 2 О + Q
При обычных температурах реакция протекает крайне медленно, выше 550°С - со взрывом (смесь 2 объемов Н 2 и 1 объема О 2 называется гремучим газом ) .

С галогенами
Водород образует галогеноводороды, например:
Н 2 + Cl 2 = 2НСl
При этом с фтором Водород взрывается (даже в темноте и при - 252°С), с хлором и бромом реагирует лишь при освещении или нагревании, а с йодом только при нагревании.

С азотом
Водород взаимодействует с образованием аммиака:
ЗН 2 + N 2 = 2NН 3
лишь на катализаторе и при повышенных температуpax и давлениях.

с серой
При нагревании Водород энергично реагирует с серой:
Н 2 + S = H 2 S (сероводород),
значительно труднее с селеном и теллуром.

С чистым углеродом
Водород может реагировать без катализатора только при высоких температуpax:
2Н 2 + С (аморфный) = СН 4 (метан)

Водород вступает в реакцию замещения с оксидами металлов
при этом образуются в продуктах вода и восстанавливается металл. Водород - проявляет свойства восстановителя:
Водород используется для восстановления многих металлов , так как отнимает кислород у их оксидов:
CuO + H 2 = Cu + H 2 O
Fe 3 O 4 + 4H 2 = 3Fe + 4Н 2 О
Применение водорода
Синтез аммиака, гидрогенизации жиров и при гидрировании угля, масел и углеводородов. Кроме того, водород применяют для синтеза соляной кислоты, метилового спирта, синильной кислоты, при сварке и ковке металлов, а также при изготовлении ламп накаливания и драгоценных камней. В продажу водород поступает в баллонах под давлением свыше 150 атм. Они окрашены в тёмно-зелёный цвет и снабжаются красной надписью "Водород".
Водород используется для превращения жидких жиров в твердые (гидрогенизация), производства жидкого топлива гидрогенизацией углей и мазута. В металлургии водород используют как восстановитель оксидов или хлоридов для получения металлов и неметаллов (германия, кремния, галлия, циркония, гафния, молибдена, вольфрама и др.
Практическое применение водорода многообразно: им обычно заполняют шары-зонды, в химической промышленности он служит сырьём для получения многих весьма важных продуктов (аммиака и др.), в пищевой - для выработки из растительных масел твёрдых жиров и т. д. Высокая температура (до 2600 °С), получающаяся при горении водорода в кислороде, используется для плавления тугоплавких металлов, кварца и т. п. Жидкий водород является одним из наиболее эффективных реактивных топлив. Ежегодное мировое потребление водорода превышает 1 млн. т.












































