Вопросы современной физики
Лекция 3
Преподаватель:
Шляхтина С.М.

Основополагающие признаки атомистики
- неизменность атомов (т.е. несотворимость и неуничтожимость материи);
- противопоставление атомов пустому пространству (признание объективности пространства и движения).

МЕХАНИСТИЧЕСКИЙ АТОМИЗМ

Недостатки механистической атомистики:
- отсутствие достоверного экспериментального материала;
- не являлась достаточно обоснованной естественнонаучной теорией;
- атомы рассматривались как частицы, лишенные возможности превращения;
- единственной формой движения принималось механическое движение;
- стремилась все явления природы рассматривать как модификацию механического движения.

открытия XIX—XX вв.:
Открытие рентгеновских лучей и радиоактивного излучения в 1896 г. А. Беккерелем и исследованием его в 1898 г. П. Кюри и М. Склодовской-Кюри. Радиоактивный распад показал: радиоактивность не связана с внешними, механическими воздействиями, а определя-ется внутренними процесса-ми, проявляющимися в виде статистических закономер-ностей;

- создание теории электромагнитно-го поля Дж. Максвеллом (1860-1865 гг.);


- открытие явления электромагнитной индукции М. Фарадеем (1831 г.).
М. Фарадей и Дж. Максвелл впервые обнаружили ее непригодность и неприменимость к электромагнитным явлениям;
Фарадей (Faraday) Майкл (22 сентября 1791, Лондон; 25 августа 1867, там же),

- экспериментальное доказательство делимости атомов и открытие электрона английским физиком Дж. Дж. Томсоном (1897 г.), за что он был удостоен Нобелевской премии в 1906 г.
Джозеф Джон Томсон
(1856 - 1940)
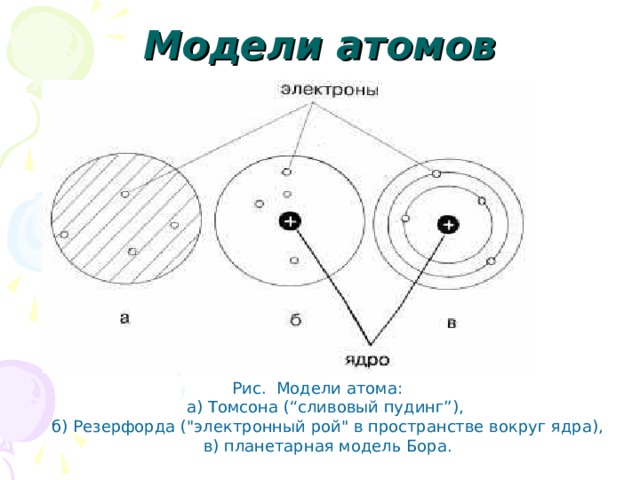
Модели атомов
Рис. Модели атома:
а) Томсона (“сливовый пудинг”),
б) Резерфорда ("электронный рой" в пространстве вокруг ядра),
в) планетарная модель Бора.
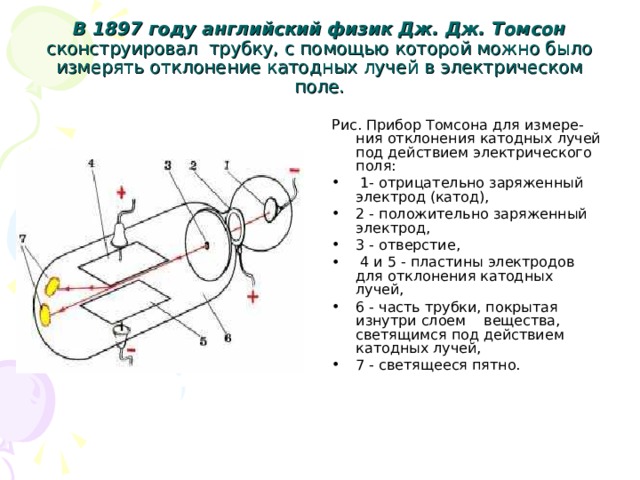
В 1897 году английский физик Дж. Дж. Томсон сконструировал трубку, с помощью которой можно было измерять отклонение катодных лучей в электрическом поле.
Рис. Прибор Томсона для измере-ния отклонения катодных лучей под действием электрического поля:
- 1- отрицательно заряженный электрод (катод),
- 2 - положительно заряженный электрод,
- 3 - отверстие,
- 4 и 5 - пластины электродов для отклонения катодных лучей,
- 6 - часть трубки, покрытая изнутри слоем вещества, светящимся под действием катодных лучей,
- 7 - светящееся пятно.
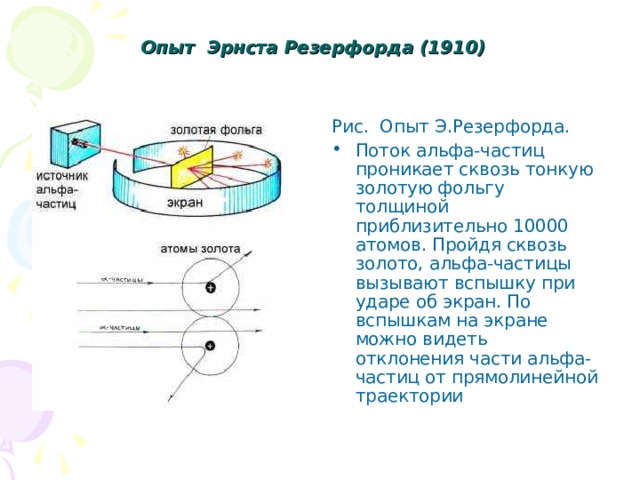
Опыт Эрнста Резерфорда (1910)
Рис. Опыт Э.Резерфорда.
- Поток альфа-частиц проникает сквозь тонкую золотую фольгу толщиной приблизительно 10000 атомов. Пройдя сквозь золото, альфа-частицы вызывают вспышку при ударе об экран. По вспышкам на экране можно видеть отклонения части альфа-частиц от прямолинейной траектории
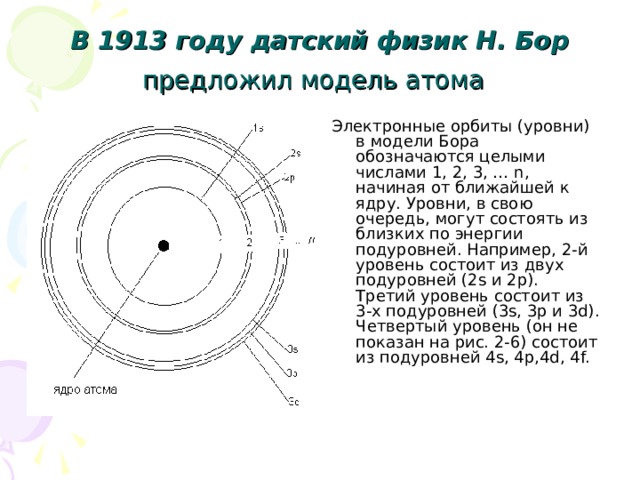
В 1913 году датский физик Н. Бор предложил модель атома
Электронные орбиты (уровни) в модели Бора обозначаются целыми числами 1, 2, 3, … n, начиная от ближайшей к ядру. Уровни, в свою очередь, могут состоять из близких по энергии подуровней. Например, 2-й уровень состоит из двух подуровней (2s и 2p). Третий уровень состоит из 3-х подуровней (3s, 3p и 3d). Четвертый уровень (он не показан на рис. 2-6) состоит из подуровней 4s, 4p,4d, 4f.
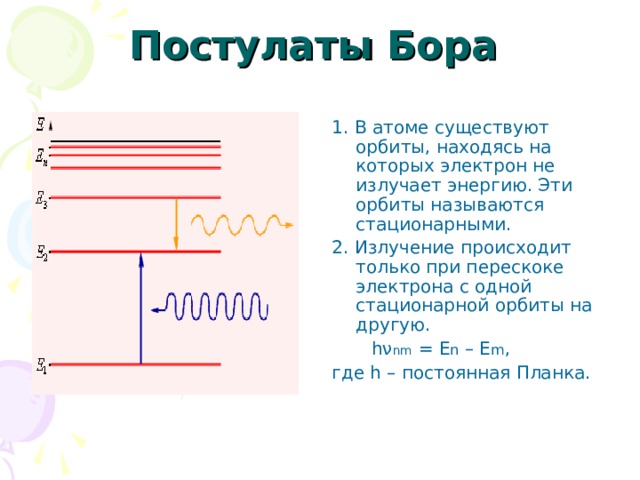
Постулаты Бора
1. В атоме существуют орбиты, находясь на которых электрон не излучает энергию. Эти орбиты называются стационарными.
2. Излучение происходит только при перескоке электрона с одной стационарной орбиты на другую.
hν nm = E n – E m ,
где h – постоянная Планка.

ПРЕДПОСЫЛКИ ДЛЯ СОЗДАНИЯ БОЛЕЕ ВЫСОКОГО УРОВНЯ РАЗВИТИЯ АТОМИЗМА
Недостатки теории Бора:
Значение теории Бора:
1. Постулаты Бора являлись гениальной догадкой.
2. Рассматривая орбиты, Бор пользовался методами классической физики, а объяснял излучение с квантовой точки зрения, т. е. использовал как классические, так и квантовые представления.
3. Постулаты были промежуточной фазой между классической и квантовой механикой, которая была сформирована в 20-х гг. XX в.
- показала неправомерность абсолютизации классических принципов в физике;
- вскрыла ограниченность ньютоновских представлений;
- убедила научный мир в том, что господствующая физическая теория дает приблизительное, относительно верное описание явлений действительности и в процессе развития науки будет неизменно обогащаться, уточняться, полнее отражать действительность, способствуя созданию более последовательных фундаментальных теорий.

КВАНТОВАЯ ТЕОРИЯ СТРОЕНИЯ АТОМА
В 20-х годах прошлого века французский физик Л. де Бройль выдвинул гипотезу о том, что электрон обладает свойствами не только частицы, но и волны.
Французский физик Луи Виктор Пьер Раймон де Бройль (1892-1987) родился в Дьеппе.
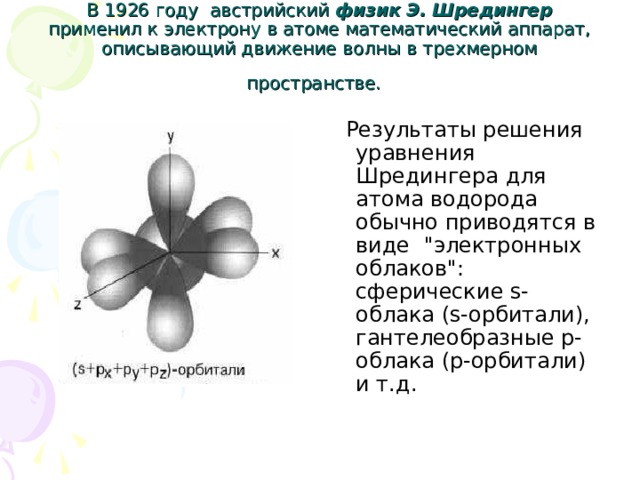
В 1926 году австрийский физик Э. Шредингер применил к электрону в атоме математический аппарат, описывающий движение волны в трехмерном пространстве.
Результаты решения уравнения Шредингера для атома водорода обычно приводятся в виде "электронных облаков": сферические s-облака (s-орбитали), гантелеобразные p-облака (p-орбитали) и т.д.

C оотношения неопределённостей
В упрощённой формули-ровке эти соотношения утверждают, что допол-нительные физические величины не могут быть одновременно точно определены.
X p ≥ = h/(2 ), где x – неопределённость координаты (частицы или системы), p – неопределённость её импульса, а h = 6,6.10-34 Дж.с = 4,1.10-15 эВ.с - постоянная Планка.
Гейзенберг Вернер Карл
(1901–1976),

характер современного атомизма:
- корпускулярно-волновой природы элементарных частиц;
- волновые характеристики — это различные проявления единого материального образования. Исследования Л. де Бройля показали, что квантово-механическая природа есть у всех видов материи. Классическая механика исключала возможность дифракции электрона, протона, нейтрона, а экспериментальные данные подтвердили гипотезу де Бройля и определили новый подход к пониманию процессов микромира.

СУЩЕСТВЕННЫЕ ОСОБЕННОСТИ АТОМИЗМА XX в.
1. Состояние частицы не может быть определено классическими понятиями.
2. Вводится волновая функция, дающая полное квантово-механическое описание физического состояния частицы.
3. Обнаруживается всеобщая взаимо-превращаемость элементарных частиц, обоснованная огромным экспериментальным материалом, которая выражает взаимную связь и взаимопревращение объектов микромира и свидетельствует о качественном многообразии форм материи и их взаимообусловленности.

ЭЛЕМЕНТАРНЫЕ ЧАСТИЦЫ
По массе:
1. Легкие частицы — лептоны (фотон, электрон, позитрон). Фотоны не имеют массы покоя.
2. Частицы средней массы — мезоны (мю-мезон, пи-мезон).
3. Тяжелые частицы — барионы. К ним относятся нуклоны — составные части ядра: протоны и нейтроны. Протон — самый легкий барион.
4. Сверхтяжелые — гипероны.

ЭЛЕМЕНТАРНЫЕ ЧАСТИЦЫ
Устойчивых разновидностей немного:
- фотоны (кванты электромагнитного излучения);
- гравитоны (гипотетические кванты гравитационного поля);
- электроны;
- позитроны (античастицы электронов);
- протоны и антипротоны;
- нейтроны;
- нейтрино — самая загадочная из всех элементарных частиц.