ОГЭ по ХИМИИ ЗАДАНИЕ №22
Для того, чтобы выполнить задание 22. Необходимо наизусть знать формулы и названия кислот и солей и уметь составлять формулы. Так же нужно знать, как вещества взаимодействуют друг с другом (типичные реакции веществ -учебник 8 класса О.С. Габрелян )
Оксиды-это сложные вещества, состоящие из двух химических элементов, один из которых — кислород.
Основания- это сложные вещества, в которых атомы металлов соединены с одной или несколькими гидроксильными группами.
Соли-это сложные вещества, состоящие из атомов металлов и кислотных остатков.
Кислоты-это сложные вещества, состоящие из одного или нескольких атомов водорода, способных замещаться атомами металлов, и кислотного остатка.
Чтобы быстрее научиться выполнять реакции веществ, можно порешать несколько цепочек превращений.
Цепочка 1:
Дана схема превращений:
Сu - СuС12- Cu(N03)2- X
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для второго превращения составьте сокращённое ионное уравнение реакции.
Пояснение.
Напишем уравнения реакции, соответствующие схеме превращений:
1) Сu + С12 = СuС12
2) СuС12 + 2AgNO3 = 2AgCl + Cu(NO3)2
3) 2Cu(NO3)2 2CuO + 4NO2 + O2
Составим сокращённое ионное уравнение для второго превращения:
4) CI- + Ag+ = AgCl
Цепочка 2:
Дана схема превращении:
Сu -CuS04- Сu(ОН)2--- HNO3-X
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для второго превращения составьте сокращённое ионное уравнение реакции.
Пояснение.
Напишем уравнения реакции, соответствующие схеме превращений:
1) Сu + 2H2SO4 (к) = CuSO4 + SO2 + 2H2O
2) CuSO4 + 2NaOH = Na2SO4 + Сu(ОН)2
3) Сu(ОH)2 + 2HNO3 = Cu(NO3)2 + 2H2O
Составим сокращённое ионное уравнение для второго превращения:
4) Сu2++ 2OH - = Сu(ОН)2
нужно уметь составлять ионное уравнение.
Порядок составления ионных уравнений:
1. Записывают молекулярное уравнение реакции
2. Определяют растворимость каждого из веществ с помощью таблицы растворимости
3. Записывают уравнения диссоциации растворимых в воде исходных веществ и продуктов реакции
4. Записывают полное ионное уравнение реакции
5. Составляют сокращенное ионное уравнение, сокращая одинаковые ионы с обеих сторон
После повторения и закрепления всей теории можно перейти к решению заданий.
Описание:
Задание 1:
Даны вещества: MgO, H3PO4, NaCl, AgNO3, HCl(p-p), Ba(NO3)2. Используя воду и необходимые вещества только из этого списка, получите в две стадии нитрат магния. Опишите признаки проводимых реакций. Для второй реакции напишите сокращённое ионное уравнение реакции.
Ответ:
Составлены уравнения двух проведённых реакций:
1)MgO + 2НС1 = MgCl2 + Н20
2)MgCl2 + 2AgNO3 = 2AgCl + Mg(NO3)2
Описаны признаки протекания реакций:
3)для первой реакции: растворение осадка;
4) для второй реакции: образование белого осадка.
Составлено сокращённое ионное уравнение второй реакции:
б) Ag+ + Сl- =AgCl
Задание 2:
Даны вещества: Na2SO4, ВаС12, растворы НС1, H2SO4 и NH3. Используя воду и необходимые вещества только из этого списка, получите в две стадии раствор хлорида аммония. Опишите признаки проводимых реакций. Для второй реакции напишите сокращённое ионное уравнение реакции.
Ответ: Составлены уравнения двух проведённых реакций:
H2SO4 + 2NH3 = (NH4)2SO4
(NH4)2SO4 + ВаС12 = BaSO4 + 2NH4C1 Описаны признаки протекания реакций:
для первой реакции: видимые признаки реакции отсутствуют;
для второй реакции: образование белого осадка. Составлено сокращённое ионное уравнение второй реакции:
Ва2- + SO42- = BaSO4
Задание 3:
Даны следующие вещества: HCl(p-p), HgS(p-p), Li3PO4, А1(0Н)3, Na3PO4, NaOH. Используя воду и необходимые вещества только из этого списка, получите в две стадии фосфат алюминия. Опишите признаки проводимых реакций. Для второй напишите сокращённое ионное уравнение реакции.
Ответ:
Составлены уравнения двух проведённых реакций:
А1(ОН)3 + ЗНС1 = А1С13 + ЗН2O
2) А1С1 + Na3PO4= AlPO4 + 3NaCl
Описаны признаки протекания реакций:
3)для первой реакции: растворение осадка;
4)для второй реакции: выпадение белого осадка.
Составлено сокращённое ионное уравнение второй реакции:
5)А13+ + PO43- = А1РO4
Задание 4:
Даны вещества: AgNO3, ZnSO4, Сu, NaOH, раствор H2SO4. Используя воду и необходимые вещества только из этого списка, получите в две стадии гидроксид меди(П). Опишите признаки проводимых реакций. Для второй реакции напишите сокращённое ионное уравнение реакции.
Ответ:
Составлены уравнения двух проведённых реакций:
1)Сu + 2AgNO3 = Cu(NO3)2 + 2Ag
2)Cu(NO3)2 + 2KOH = Cu(OH)2 + 2KNO3
Описаны признаки протекания реакций:
3)для первой реакции: выделение серого осадка металлического серебра и изменение цвета раствора (появление голубой окраски раствора);
4)для второй реакции: выпадение голубого осадка.
Составлено сокращённое ионное уравнение второй реакции:
5)Cu2+ + 20Н - = Си(ОН)2
Задание 5:
Даны растворы веществ: FeCl2, Fe2(S04)3, HN03, NaOH, AgNO3, HC1. Используя необходимые вещества только из этого списка, получите в две стадии нитрат железа(Ш). Опишите признаки проводимых реакций. Для первой реакции напишите сокращённое ионное уравнение реакции.
Ответ:
Составлены уравнения двух проведённых реакций:
1)Fe2(S04)3 + 6NaOH = 2Fe(OH)3+ 3Na2SO4
2)Fe(OH)3 + 3HNO3 = Fe(NO3)3 + 3H2O
Описаны признаки протекания реакций:
3) для первой реакции: выпадение бурого осадка
4) для второй реакции: растворение бурого осадка
Составлено сокращённое ионное уравнение первой реакции:
Fe3+ + ЗОН- =Fe(OH)3
Задание 6:
Даны вещества: CaCO3, H3P04, NaOH, AgN03, HCl(p-p), Ba(NO3)2. Используя воду и необходимые вещества только из этого списка, получите в две стадии нитрат кальция. Опишите признаки проводимых реакций. Для второй реакции напишите сокращённое ионное уравнение реакции.
Ответ:
Составлены уравнения двух проведённых реакций:
1) СаСO3 + 2НС1 = СаС12 + Н2O + СO2
2) СаС12 + 2AgN03 = 2AgCl +Ca(NO3)2
Описаны признаки протекания реакций:
3) для первой реакции: растворение осадка и выделение газа;
4)для второй реакции: образование белого осадка.
Составлено сокращённое ионное уравнение второй реакции:
Ag+ + CI- = AgCl
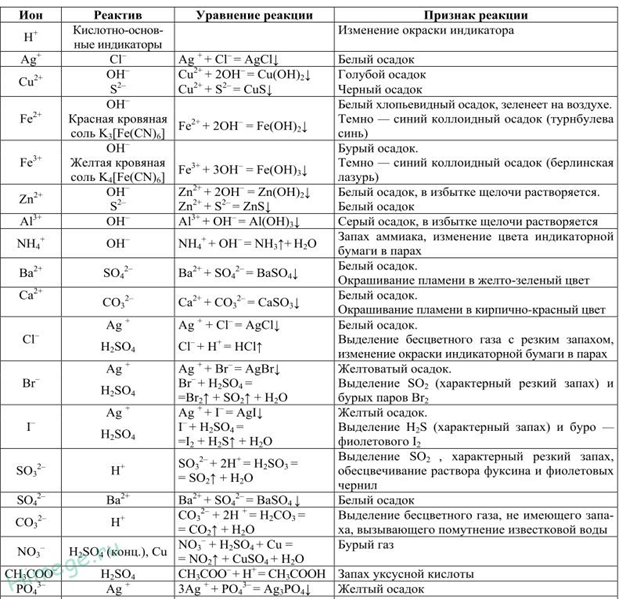
ПРИЛОЖЕНИЕ
Таблица для определения ионов и результата реакции.