Экзаменационная работа по химии за курс 8 класса
Часть 1. Выберите один правильный ответ.
1. К простым веществам относится
1) кислород 2) мел 3) азотная кислота 4) углекислый газ
2. Распределению электронов по энергетическим уровням атома хлора соответствует ряд чисел
1) 2, 8, 5 2) 2, 7 3) 2, 8, 7 4) 2, 5
3. Наиболее выражены металлические свойства у
1) кремния 2) натрия 3) алюминия 4) магния
4. Степень окисления +5 азот проявляет в соединении
1) NO 2) N2O3 3) NO2 4) N2O5
5. Химическая связь в молекуле аммиака NH3
1) ионная 2) металлическая
3) ковалентная неполярная 4) ковалентная полярная
6. Выберите формулу кислотного оксида
1) BaO 2) SiO2 3) CO 4) Na2O
7. Смесь воды и бензина можно разделить с помощью
1) перегонки 2) фильтрования
3) выпаривания 4) делительной воронки
8. Коэффициент перед формулой кислорода в уравнении реакции, схема которой С2Н2 + О2 –– СО2 + Н2О, равен
1) 2 2) 3 3) 4 4) 5
9. Гидроксид кальция реагирует с
1) HCl 2) Fe(OH)2 3) MgO 4) Ag
10. Большинство кислотных оксидов реагирует
1) только с водой 2) только с кислотами
3) со щелочами и кислотами 4) с водой и щелочами
11. Формула вещества Х в схеме превращений Сu –– X –– CuCl2
1) CuO 2) Cu(OH)2 3) Cu2O 4) CuOH
12. Лакмусом можно распознать
1) соляную кислоту 2) гидроксид железа (III)
3) воду 4) оксид кремния (IV)
13. Реакцией обмена является
1) Cu(OH)2 = CuO + H2O 2) ZnO + H2SO4 = ZnSO4 + H2O
3) Zn + 2HCl = ZnCl2 + H2 4) Fe + S = FeS
Часть 2.
14. Установите соответствие между процессом в природе и явлением:
Процессы в природе Явления
1) почернение серебряных украшений А) физическое
2) плавление парафина Б) химическое
3) туман
4) соление огурцов
15. С оксидом магния могут взаимодействовать
серная кислота
хлорид меди (II)
гидроксид натрия
медь
оксид серы (VI)
16. Установите соответствие между исходными веществами и продуктами
реакции.
Исходные вещества Продукты реакции
А) ВаО + SО3 1) Ва(NО3)2 + АgСl
Б) Ва(ОН)2 + H2SО4 2) ВаSО4 +Н2
В) ВаСl2 + АgNО3 3) ВаSО4
4) ВаSО4 +Н2О
17. Вычислите массовую долю углерода в карбонате кальция СаСО3.
Ответ_______ % . (Запишите число с точностью до целых.)
18. Какая масса соли необходима для приготовления 400 г 2%-ного раствора соли?
Ответ_______г. (Запишите число с точностью до целых.)
Часть 3.
19. Осуществите превращения: 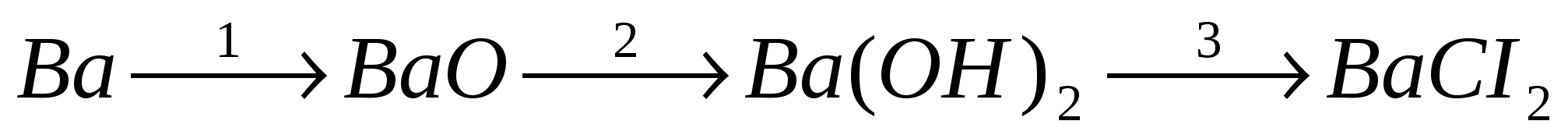
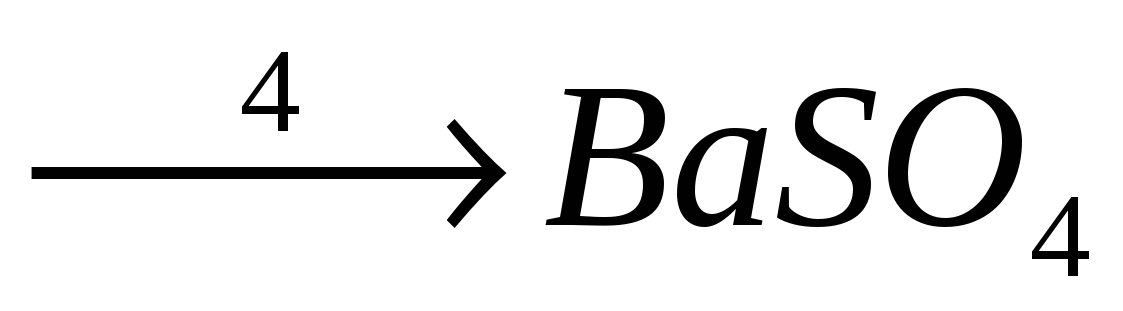
20. Какая масса оксида магния получится при сгорании магния в 6,4 г кислорода?

















