
Проверь свои знания по теме «Уравнение состояния идеального газа»
Тренировочный тест

1.Назови макроскопические параметры:
Масса, давление, объем, температура
давление, объем, температура

P, V, T
К макроскопическим параметрам идеального газа относятся: давление, объем и температура!
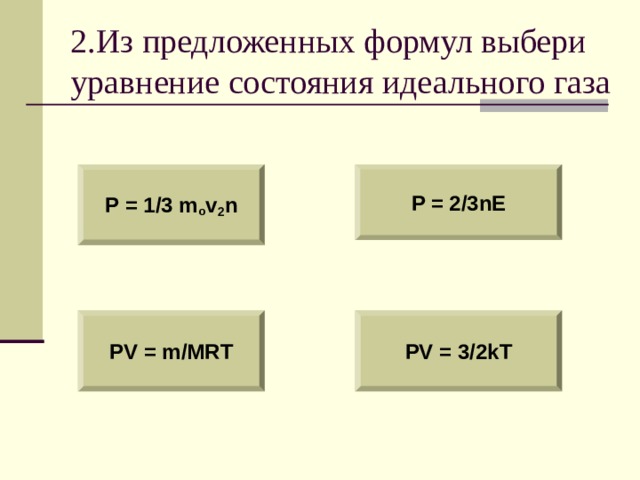
2.Из предложенных формул выбери уравнение состояния идеального газа
P = 1/3 m o v 2 n
P = 2/3nE
PV = m/MRT
PV = 3/2kT

Неправильно!
Повтори теорию!

Молодец!
Переходи к следующему вопросу

Неправильно!
Повтори теорию!

pv = m/MRT
Уравнением состояния идеального газа называется зависимость между макроскопическими параметрами: давлением, объемом и температурой!

Молодец!
Переходи к следующему вопросу
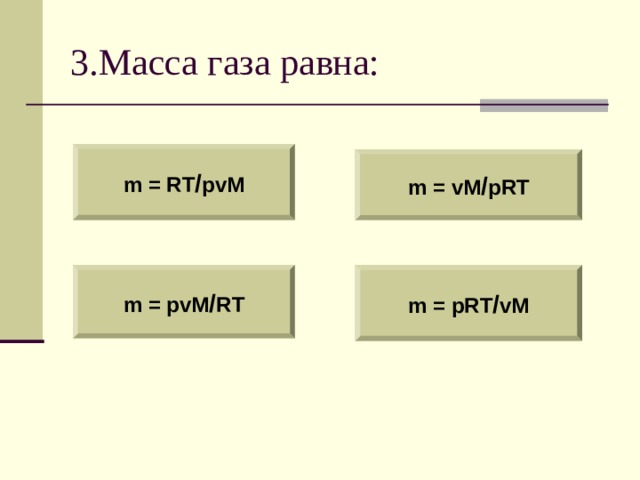
3.Масса газа равна:
m = RT / pvM
m = vM / pRT
m = pvM / RT
m = pRT / vM

Молодец!
Переходи к следующему вопросу

Неправильно!
Повтори теорию!

Чтобы выразить неизвестную величину из уравнения Менделеева – Клапейрона, умножь левую и правую часть уравнения на знаменатель (М), получишь: р vM = mRT , найди неизвестный множитель, разделив произведение на известные множители.
pv = m/MRT
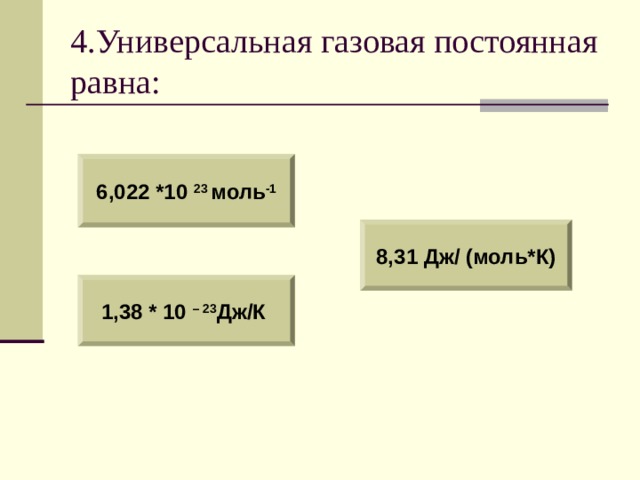
4.Универсальная газовая постоянная равна:
6,022 *10 23 моль -1
8,31 Дж/ (моль*К)
1,38 * 10 – 23 Дж/К

Неправильно!
Повтори теорию!

Молодец!
Переходи к следующему вопросу

k N A = R
Универсальной газовой постоянной называется произведение числа Авогадро и постоянной Больцмана: 6,02 * 10 23 * 1,38 * 10 -23
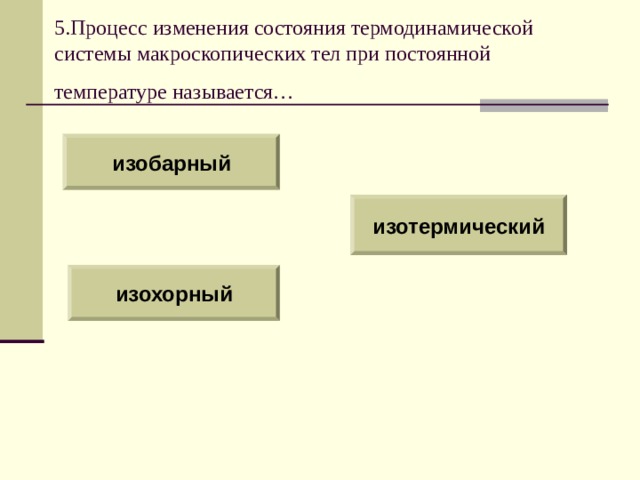
5.Процесс изменения состояния термодинамической системы макроскопических тел при постоянной температуре называется…
изобарный
изотермический
изохорный

Согласно уравнению состояния газа в любом состоянии с неизменной температурой произведение давления газа на его объем остается постоянным. Процесс изотермический.
T = const
Закон Бойля-Мариотта
pv = const

Молодец!
Переходи к следующему вопросу

Неправильно!
Повтори теорию!

6.Газовый закон для изобарного процесса – это…
PV = const
p/T = const
v/T = const

Неправильно !
Повтори теорию!

Молодец!
Переходи к следующему вопросу
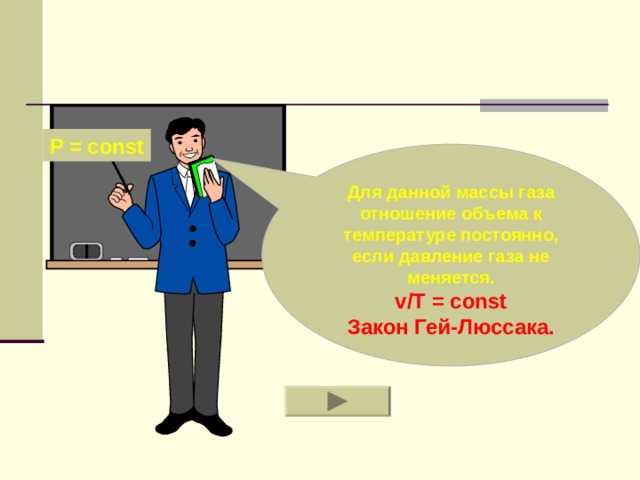
P = const
Для данной массы газа отношение объема к температуре постоянно, если давление газа не меняется.
v/T = const
Закон Гей-Люссака.
7. Газовый закон Шарля устанавливает зависимость между:
Давлением и
объемом
Объемом и
температурой
Между давлением и
температурой

Неправильно!
Повтори теорию!

Поздравляю!
Переходи к следующему вопросу
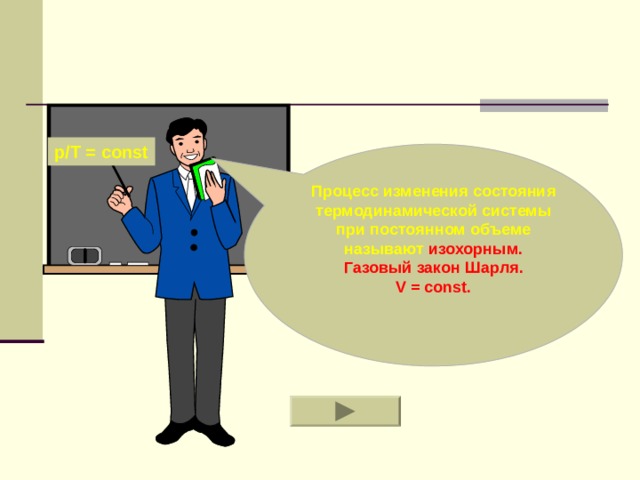
p/T = const
Процесс изменения состояния термодинамической системы при постоянном объеме называют изохорным.
Газовый закон Шарля.
V = const.
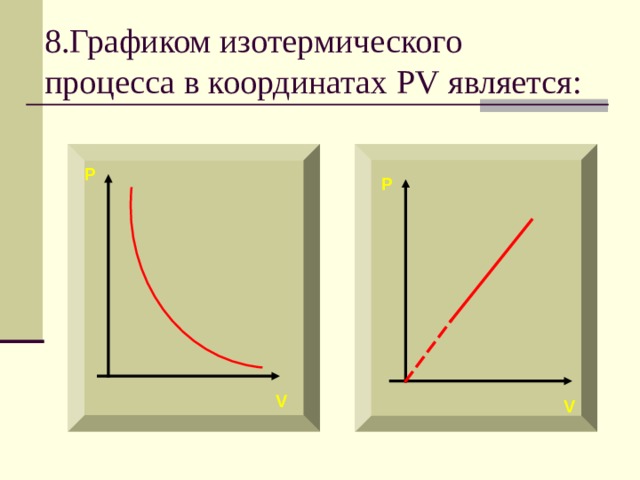
8.Графиком изотермического процесса в координатах PV является:
P
P
V
V

Поздравляю!
Переходи к следующему вопросу

Неправильно!
Повтори теорию!

Зависимость между давлением и объемом в изотермическом процессе обратно пропорциональная. Графиком в координатах PV является изотерма – гипербола.
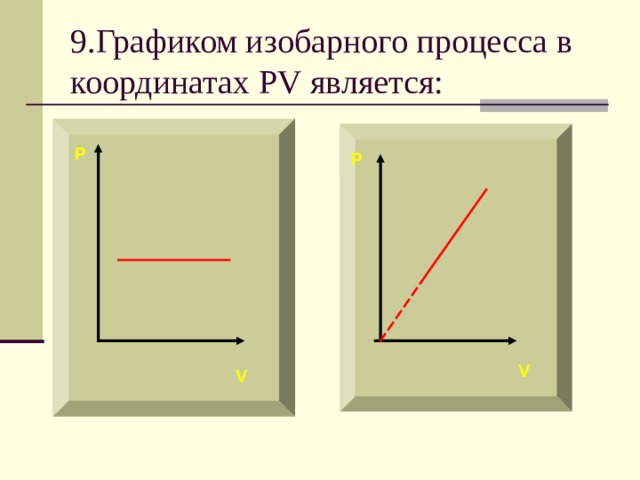
9.Графиком изобарного процесса в координатах PV является:
P
P
V
V

Поздравляю!
Переходи к следующему вопросу

Неправильно!
Повтори теорию!

Если процесс изобарный давление постоянно, в координатах PV график прямая линия параллельная оси объема.
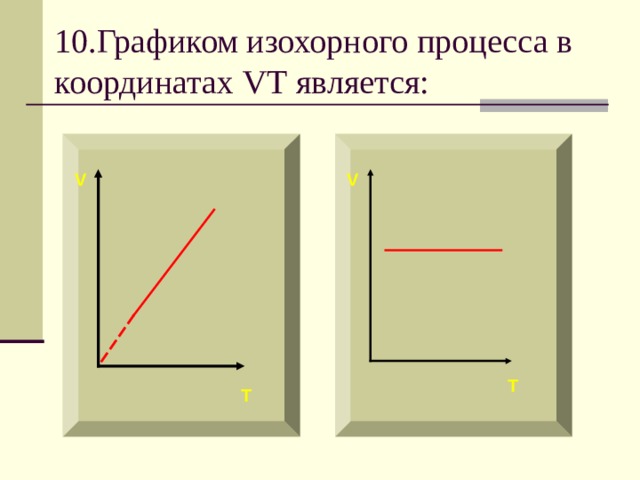
10.Графиком изохорного процесса в координатах VT является:
V
V
T
T

Поздравляю!
Переходи к следующему вопросу

Неправильно!
Повтори теорию!

Если процесс изохорный объем постоянный, в координатах VT график - прямая линия параллельная оси температуры.

Реши задачу:
Найди давление газа бутана (С 4 Н 8 ) в баллоне для портативных
газовых плит объемом 0,5 л и массой 250г
при температуре 20 0 С
21,7 МПа
12кПа

Поздравляю!
Переходи к следующей задаче

Неправильно!
Посмотри решение

Решение:
Переведи единицы измерения объема, массы, температуры в СИ.
Найди молярную массу бутана:
M=( 4*12 + 1*8) * 10 -3 = 56 10 -3
кг/моль
Из уравнения М-К вырази давление: p = mRT / VM , выполни вычисления.
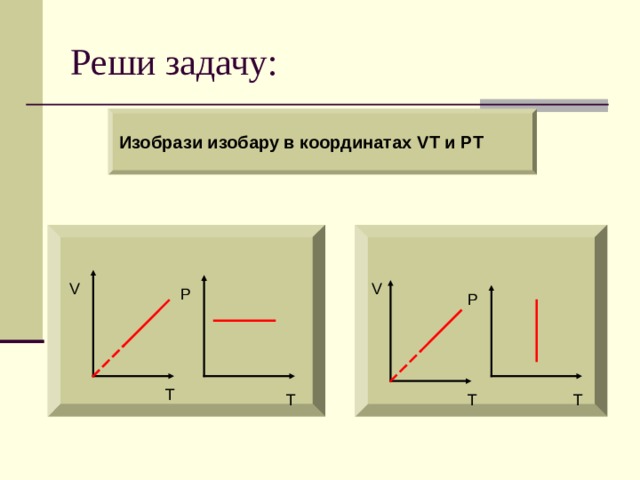
Реши задачу:
Изобрази изобару в координатах VT и PT
V
V
P
P
T
T
T
T

Поздравляю!
Переходи к контрольному тесту
- Переходи к контрольному тесту

Неправильно!
Повтори теорию
































































