Тема: Законы термодинамики. Внутренняя энергия.
Класс: 10.
Цель урока: Создать условия для личностной самореализации каждого обучающегося в процессе актуализации ранее изученного материала и освоения новой темы, способствовать развитию личностных, учебно-познавательных, коммуникативных компетенций.
Задачи урока:
1. Предметные - сформулировать 1 закон термодинамики, рассмотреть следствия, вытекающие из него; добиться усвоения учащимися закона сохранения и превращения энергии для тепловых процессов; показать практическую значимость закона при решении задач;
2. Метапредметные – развивать способы мыслительной деятельности (анализ, сравнение, обобщение), развитие речи (владение физическими понятиями, терминами), способствовать развитию умения сопоставлять факты; логично и сжато строить свой ответ, систематизировать учебный материал;
3. Личностные – воспитывать устойчивый интерес к предмету, положительное отношение к знаниям, умение оценивать, вырабатывать собственную позицию.
Предварительная подготовка. Учащиеся получили задание ознакомиться с историей открытия закона сохранения энергии, историей изобретения вечных двигателей.
Тип урока: изучение нового материала.
Ход урока
Организационный момент.
Актуализация знаний.
Фронтальный опрос в форме беседы:
Что такое внутренняя энергия, какой буквой она обозначается, какой формулой определяется?
От чего зависит изменение внутренней энергии, какой формулой можно найти это изменение?
Какими способами можно изменить внутреннюю энергию системы? (за счет совершения работы, либо за счет теплообмена с окружающими телами)
Похлопайте в ладоши. Что произошло и почему? (нагревание за счет работы самого тела). Как обозначается и определяется такая работа?
Вам сильно наступили на ногу. Что произошло и почему? (нагревание за счет совершения работы внешних сил над телом).
Как определить работу газа по графику? (по площади фигуры под изолинией).
Изучение нового материала.
Энергия в природе не возникает из ничего и не исчезает: количество энергии неизменно, она только переходит из одной формы в другую.
Кинетическая энергия частиц определяется скоростью, а значит - температурой тела.
Потенциальная - расстоянием между частицами, а значит - объемом.
Следовательно: U=U(T,V) - внутренняя энергия зависит от объема и температуры.
Сумма кинетических энергий хаотического движения всех частиц тела относительно центра масс тела (молекул, атомов) и потенциальных энергий их взаимодействия друг с другом называется внутренней энергией. U = Ek + Ep (слайд 2).
Способы изменения внутренней энергии (слайд 3):
Теплопередача (конвекция, излучение, теплопроводность);
Совершение работы (работа газа – 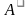 ; работа внешних сил – А).
; работа внешних сил – А).
Геометрический смысл работы (слайд 4): работа численно равна площади под графиком процесса на диаграмме.
Количество теплоты (слайд 5,6) – это физическая величина, показывающая, какая энергия передана телу в результате теплообмена.
Закон сохранения и превращения энергии для тепловых процессов называется 1 законом термодинамики (слайд 7). Обмен энергией между термодинамической системой и окружающими телами в результате теплообмена и совершаемой работы.
Если при нагревании газ расширяется и при этом совершает работу A, то первый закон термодинамики можно сформулировать по-другому (слайд 8): Количество теплоты, переданное газу, равно сумме изменения его внутренней энергии и работы, совершенной газом.
Так как работа газа и работа внешних сил вследствие 3-го закона Ньютона равны по модулю и имеют противоположный знак: Aвнешн = –AI
Применение 1 закона термодинамики к изопроцессам (слайд 9):
изохорный процесс (v=const) т.к. ΔV=0, то A= 0, значит первый закон термодинамики выглядит так: Δ U=Q Газ увеличивает свою внутреннюю энергию за счет теплоты, полученной из внешней среды. Если газ нагревается, то ΔU 0. Если газ охлаждается, то ΔU
Изотермический процесс (T=const) т.к. T=const, то ΔU = 0, значит первый закон термодинамики выглядит так: Q = А´ (слайд 10).
Изобарный процесс (р = const), при изобарном нагревании T0, U0, газ совершает работу, тепло поглощается (слайд 11-13).
Адиабатный процесс (слайд 14) - это модель термодинамического процесса, происходящего в системе без теплообмена с окружающей средой. Линия на термодинамической диаграмме состояний системы, изображающая равновесный (обратимый) адиабатический процесс, называется адиабатой.
Закрепление материала.
Задачи (слайд 15):
Идеальный газ получил количество теплоты, равное 300 Дж, и совершил работу, равную 100 Дж. Как изменилась внутренняя энергия газа?
Идеальный газ совершил работу, равную 300 Дж. При этом внутренняя энергия уменьшилась на 300 Дж. Каково значение количества теплоты в этом процессе?
Идеальный газ совершил работу, равную 600 Дж. При этом его внутренняя энергия увеличилась на 250 Дж. Какое количество теплоты получил газ?
Тепловые двигатели (слайд 16) – это устройства, превращающие внутреннюю энергию топлива в механическую энергию.
Виды тепловых двигателей (слайд 17): паровая машина; паровая турбина; газовая турбина; двигатель внутреннего сгорания; реактивный двигатель.
Домашнее задание.
Выучить определения, формулы по теме «1 закон термодинамики». Решить задачу:
Идеальный газ получил количество теплоты, равное 540 Дж, и совершил работу,
равную 220 Дж. Как изменилась внутренняя энергия газа?







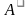 ; работа внешних сил – А).
; работа внешних сил – А). 









