III глава

Химиядагы сандык катыштар
Заттын саны - моль. Моль масса
Сабактын максаты: заттын саны моль.Авогадро саны. Заттын абсоюттук массасы жөнүндө түшүнүк берип, заттарды түзүүчү бөлүкчөлөр жонүндөгү билимдерге таянып, затты түзүүчү бөлүкчөлөрдүн санын билүү боюнча көнүгүү иштөө менен түшүнүктөрдү калыптандыруу.
Көрсөткүчтөр: эгерде окуучу затты түзүүчү эӊ майда бөлүкчөнү ченп алууга мүмкүн экендигин түшүнсө, ар түрдүү газдар бирдей көлөмдү ээлей тургандыгын билишсе, ошол билимди пайдаланып маселе, мисал иштей алышса, газдардын көлөмүн, андагы кармалган бөлүкчөлөрдү эсептеп чыгара алышса.
С абакты уюштуруу: 1.Жаӊы теманы кабыл алууга окуучуларды даярдоо.
абакты уюштуруу: 1.Жаӊы теманы кабыл алууга окуучуларды даярдоо.
(чөйрө түзүү)
2.Өтүлгөн темалар боюнча кайталоо, жаны теманы кабыл үчүн көнүгүүлөр менен окуучуларды машыктыруу.Мисалы:
Формула деп эмнени түшүнөсүӊөр?
Химиялык формула деген эмне?
Бул жазуулар эмнени түшүндүрөт?
3Н, 2Н2О, 5О2, 3CuCI2 ,7CI , 3N2 ,5Fe2O3 ,2CuO , H2 ,O.
Валенттүүлүк деп эмнени түшүнөсүӊөр?
N2O ,SiO2 , Li2O , P2O5 ,CaO, HF ,MgCI2 , FeCI3 бул заттардын курамындагы элементтердин валенттүүлүгүн тапкыла деген суроолор берилет.
3.Эки атом суутек, бир атом кремний, 3 атом кычкылтектен турган заттын формуласын жазгыла.
4.Берилген сүрөттөр боюнча кайсы зат, кандай атомдордон тура тургандыгы боюнча айтып бергиле.
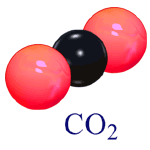
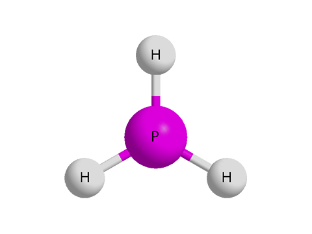
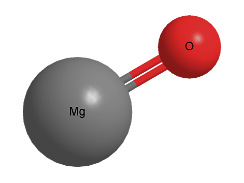
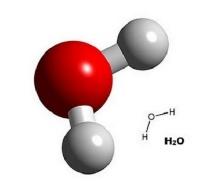 а) б) в) г)
а) б) в) г)
Мугалим окуучу менен бирдикте өтүлгөн темаларды эске түшүрүп жаӊы тема айтылат.
Сабактын жүрүшү:
Мугалим: Химия предмети – заттар жана алардын бири-бирине айлануулары жөнүндөгү илим экендигин эске салып, ал заттардын лабораторияда , химиялык заводдордо өндүрүлүп алынары айлтылат. Өндүрүп алуу үчүн аны ченеп алуу керек, ошондуктан заттарды ченөө зарылчылыгы келип чыккан- деп мугалим маалымдайт.
З атты эмне менен ченөө ыӊгайлуу? Мисалы төмөнкү чен бирдиктерди билесиӊер.
атты эмне менен ченөө ыӊгайлуу? Мисалы төмөнкү чен бирдиктерди билесиӊер.
У бакыттын бирдиги –секунд, мүнөт, саат, сутка, ай, жыл.
бакыттын бирдиги –секунд, мүнөт, саат, сутка, ай, жыл.
У зундуктун бирдиги – мм, см, м, км.
зундуктун бирдиги – мм, см, м, км.
 Көлөмдүн бирдиги – мл, л, тонна.
Көлөмдүн бирдиги – мл, л, тонна.

Затты түзүп туруучу ,бөлүкчөлөр атом менен молекуланы эмне менен ченөө керек?
( окуучулар өз алдынча иштешет андан группада талкууланат)
Окуучу: Лабораторияда атом , молекуланы саноо мүмкүнчүлүгү жок деген жыйынтыка келиши мүмкүн.
М угалим: лабораторияда заттарды тараза менен ченеп алышат.Ошондуктан бир эле учурда заттын массасы менен аны түзүп туруучу атом , молекуланын санын ченөөчү чен бирдикти кабыл алуу зарыл болду. Мындай бирдик моль деп мугалим окуучуларга билдирүү жасайт, да ага аныктама берилет. ( окуу китеби $16).
угалим: лабораторияда заттарды тараза менен ченеп алышат.Ошондуктан бир эле учурда заттын массасы менен аны түзүп туруучу атом , молекуланын санын ченөөчү чен бирдикти кабыл алуу зарыл болду. Мындай бирдик моль деп мугалим окуучуларга билдирүү жасайт, да ага аныктама берилет. ( окуу китеби $16).
Көмүртектин бир атомунун массасы 19,93
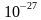 кг экендигин билип, көмүртек атомунун массасынын 1/12 бөлүгүндө 6,02
кг экендигин билип, көмүртек атомунун массасынын 1/12 бөлүгүндө 6,02 1023
1023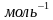 атом , молекула кармалат деген формула доскага жазылат. Демек моль - 6,02
атом , молекула кармалат деген формула доскага жазылат. Демек моль - 6,02 1023
1023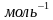 молекула ( атом) кармалагн заттын саны. Бул сан Авогадро саны деп аталат.
молекула ( атом) кармалагн заттын саны. Бул сан Авогадро саны деп аталат.
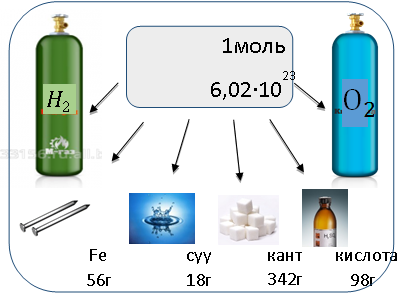
1 моль сууда 6,02 1023
1023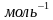 сандагы молекула,
сандагы молекула,
1моль алюминийде 6,02 1023
1023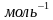 сандагы алюминийдин атому,
сандагы алюминийдин атому,
1моль күкүрт кислотасында 6,02 1023
1023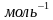 сандагы күкүрт кислотасынын бар экендиги айтылат. Бул маалымат менен окуучулар таанышкнадан кийин окуучулар оозеки иштеген тапшырмалар менен иштешет.
сандагы күкүрт кислотасынын бар экендиги айтылат. Бул маалымат менен окуучулар таанышкнадан кийин окуучулар оозеки иштеген тапшырмалар менен иштешет.

Демек Авогадро санын, заттын санын билүү менен ошол затта кармалган атомдун жана молекуланын санын табууга болот. Ал үчүн төмөнкү формуланы пайдаланабыз деп төмөнкү формула берилет:
Текст окулуп, талкууланагандан кийин формула боюнча бир нече көнүгүү иштелет.
Маселе: ( ар бир окуучу өз алдыгнча иштешет).
окуучу 0,25 моль хлордуу суутек,
-окуучу 1,5 моль көмүртектин ( IV) оксиди,
окуучу 0,5 моль кычкылтек ,
окуучу 0,01 моль суутекте канча молекула кармалат?
З
 арыл болгон бөлүкчөлөрдүн заттарда болушу үчүн аларды кандай массалык катышта алуу керек? (окуучулар өз алдынча иштешет)
арыл болгон бөлүкчөлөрдүн заттарда болушу үчүн аларды кандай массалык катышта алуу керек? (окуучулар өз алдынча иштешет)
Мугалимдин билдирүүсү менен формуланын негизинде көнүгүү иштелет.
Бул үчүн моль масса деген түшүнүк пайдаланылат. 1моль заттын масасасы моль масса деп аталат. Мугалим маалымат берет , да формула берилет.


Андан кийин окуучулар менен бирдикте бир нече көнүгүү иштелет.
Mr ( H2O) = 18 M ( H2O) = 18г/ моль
Mr (Fe) = 56 M ( Fe) = 56г/ моль
Mr ( H2SO4) = 98 M ( H2SO4) = 98г/ моль
Заттардын молекулалык массасы молдук массага барбар экендигин далилдөө үчүн бир нече оозеки иштелүүчү көнүгүүлөр берилип , андан кийин окуучулардын топ менен иштөөсүн уюштурат.
I - топ. 0,25 моль күкүрт кислотасынын ( H2SO4) массасын тапкыла?
. II - топ. 3 моль күкүрт кислотасында канча молекула кармаалат?
III - топ. 0,15 моль суунун ( H2O) массасын тапкыла?
IV - топ. 0,5 моль темирде канча атом кармалат?
Андан кийин окуу китебиндеги өз алдынча иштөө үчүн көнүгүүлөрдүн 3- тапшырмасы аткарылат.Окуучулар Авогадро санын, моль массаны чыгарууну үйрөнгөндөн кийин мугалим окуучуларга суроо менен кайрылат.
 Заттын абсолюттук массасын табууга болобу?
Заттын абсолюттук массасын табууга болобу?
Бул суроого жооп берүү үчүн окуучулар текст менен иштешет. Тексти иштеген убакыт белгиленип берилет.
 Текст: Абсолюттук масса- өтө кичинекей болгондуктан, аны салыштырмалуу бирдик менен ченелет. Абсолюттук атомдук масса кандай эсептелинет? Алтын, жез, кальций, коргошун, жез, кремнийдин абсоюттук массасы эмнеге барабар? Абсоюттук атомдук масса менен атомдук массаны айырмалап билүү керек. Атомду түзгөн элементтер абдан кичинекей, эӊ оор атомду да абдан сезгич таразаларда тартууга мүмкүн эмес. Ошондуктан абсолюттук атомдук массанын бирдиги катары көмүртек атомунун 1/12 бөлүгү кабыл алынган.Салыштырмалуу атомдук масса- берилген атомдун массасы көмүртек атомунун 1/12 ,бөлүгүнөн канча эсе чоӊураак экендигин көрсөтүүчү сан. Мисалы жездин атомунун салыштырмалуу атомдук массасы 64 ( жакындаштырылган түрдө) болсо, бул жездин атому көмүртек атомунун 1/12 бөлүгүнөн 64 эсе оор дегенди түшүндүрөт. Салыштырмалуу атомдук масса Аr менен белгиленет.
Текст: Абсолюттук масса- өтө кичинекей болгондуктан, аны салыштырмалуу бирдик менен ченелет. Абсолюттук атомдук масса кандай эсептелинет? Алтын, жез, кальций, коргошун, жез, кремнийдин абсоюттук массасы эмнеге барабар? Абсоюттук атомдук масса менен атомдук массаны айырмалап билүү керек. Атомду түзгөн элементтер абдан кичинекей, эӊ оор атомду да абдан сезгич таразаларда тартууга мүмкүн эмес. Ошондуктан абсолюттук атомдук массанын бирдиги катары көмүртек атомунун 1/12 бөлүгү кабыл алынган.Салыштырмалуу атомдук масса- берилген атомдун массасы көмүртек атомунун 1/12 ,бөлүгүнөн канча эсе чоӊураак экендигин көрсөтүүчү сан. Мисалы жездин атомунун салыштырмалуу атомдук массасы 64 ( жакындаштырылган түрдө) болсо, бул жездин атому көмүртек атомунун 1/12 бөлүгүнөн 64 эсе оор дегенди түшүндүрөт. Салыштырмалуу атомдук масса Аr менен белгиленет.
 м ассанын атомдук бирдиги.
м ассанын атомдук бирдиги.
Көмүртек атому.

1 м.а.б = 1/12 · m (12C) = 1,66 · 10-27 кг болот.
Андан кийин төмөнкү формула берилип кээ бир элементтердин атомдук массаларын табуу тапшырмасы берилет.

Сабак жыйынтыкталып, окуучулардын билимдери бааланат.
IV глава

Химиялык реакциянын типтери
Сабактын максаты: Жаратылыштагы кубулуштарды бөлүп таанып билишет. Мисалдар келтире алат. Физикалык, химиялык кубулуштар боюнча көнүгүү иштей алат. Химиялык реакция боюнча түшүнүк алышат. Химиялык реакция деген түшүнүк алат. Химиялык реакциялардын типтери менен таанышып, жаратылышта , турмушта реакциянын маанисин окуп үйрөнөт.
Көрсөткүчтөр: эгерде окуучу жаратылыштагы кубулуштарды айырмалай алса, ага жаратылыштагы бир нече кубулуштарды мисалга келтире алса, химиялык реакцияларды теӊдемелер менен туюнтуп жаза алса, химиялык реакциянын типтерин айырмалай алса, мисалдар менен реакциянын теӊдемелерин жаза алса.ошол билимди пайдаланып маселе, мисал иштей алышса,
С абакты уюштуруу: 1.Жаӊы теманы кабыл алууга окуучуларды даярдоо.
абакты уюштуруу: 1.Жаӊы теманы кабыл алууга окуучуларды даярдоо.
(чөйрө түзүү)
2.Өтүлгөн темалар боюнча кайталоо, жаны теманы кабыл үчүн көнүгүүлөр менен окуучуларды машыктыруу. Тапшырма:
Төмөнкү химиялык реакциянын теӊдемелрин аягына чыгарып , жазып коэфиценттерин койгула.

1.?...Na + O2 ?… Na2O

2.?...Ag2O ?Ag +… O2

3.?...Cr +?...O2 ?... Cr2O3

4.?...S + ?...O2 ?...SO3
3. 3,2г суутек кычкылтекте күйгөндө канча грамм суу пайда болот ? Жообу; 3,6г
Мугалим окуучу менен бирдикте өтүлгөн темаларды эске түшүрүп жаӊы тема айтылат.
С абактын жүрүшү:
абактын жүрүшү:
Жаратылышта кандай кубулуштар жүрүп турат?
( окуучулар өз алдынча иштешет, андан кийин группада иштешет)
Мугалим: Химия предмети – заттар жана алардын бири-бирине айлануулары жөнүндөгү илим экендигин эске салып, бардык жаратылышта жүрүп турган химиялык кубулуштар – химиялык реакция болуп санала тургандыгы айтылат. Химиялык реакция учурунда заттардын ортосундагы бир байланыш үзүлүп, экинчи бир пайда болгон заттардын ортосунда жаӊы химиялык байланыш пайда болот.
Бардык химиялык реакция экиге бөлүнөт жөнөкөй жана татаал болуп.
Жөнөкөй химиялык реакцияга – кошулуу, ажыроо, орун алмашуу, алмашуу реакциясы кирет.
А нда эмесе ушул химиялык реакциянын ар бирине эксперимент жасап көрөлү , деп мугалим экспермиент көрсөтөт, ал эми окуучулар экспериментти көрүп дептерлерине жыйынтык жазышат.
нда эмесе ушул химиялык реакциянын ар бирине эксперимент жасап көрөлү , деп мугалим экспермиент көрсөтөт, ал эми окуучулар экспериментти көрүп дептерлерине жыйынтык жазышат.
Эксперимент:
Бир аз пробиркага темир таарындысын ( кара түстө) салып, ага күкүрт ( сары) порошогун салып , жакшылап аралаштырабыз. Андан пробирканы кыпчыгыч менен кармап аны спирт шамынын жардамы менен ысытабыз. Пробикадагы заттын өӊү кара түскө өзгөрөт.


темир
к
Пробиркадагы заттын өӊү өзгөрө тургандыгын окуучулар байкап,дептерине жазышат. Эмне үчүн пайда болгон заттын өӊү баштапкы заттын өӊүнө окшобойт? Анткени пробиркада баштапкы затка окшобогон башка жаӊы зат пайда болду. Суроо талкууланат да реакция кандай реакция экендиги айтылат.
Теӊдемеси жазылат.

Fe + S FeS
Бул реакция кошулуу реакциясы. Аныктамасы берилет.Бир заттан бир нече жаӊы заттарды пайда кылуу менен жүрүүчү реакция экендиги айтылат.
Аныктама окуучулардын дептерине жазылат. Схемасы берилет.

Экспермент: Аммонийдин дихроматынын ажырашы:
А ммонийдин дихроматынан ( өӊү саргыч-кызыл) бир аз өлчөмдө алып , аны асбест листинин үстүнө коюп, аны акырындап ысытабыз. Реакция жүрө баштайт. Реакция жылуулукту бөлүп чыгаргандыктан өзүнөн-өзү жүрө баштайт. Аммонийдин дихроматынын өӊү жашыл түскө өзгөрүп башка зат пайда болот. Теӊдемеси жазылат
(NH4)2Cr2O7 = Cr2O3 + N2 + 4H2O
Пробиркадагы заттын өӊү өзгөрө тургандыгын окуучулар байкап,дептерине жазышат. Эмне үчүн пайда болгон заттын өӊү баштапкы заттын өӊүнөокшобойт? Деген суроо ко юлуп талкууланат да реакция кандай реакция экендиги айтылат да, аныктама берилет.
Ажыроо реакциясынын схемасы:
Э кинчи реакциянын тиби – ажыроо реакциясы.
 3-экспермент:
3-экспермент:
Пробикага жездин сульфатыны эритмесине темир мыкты салабыз. Реакция жүрүп, темир мыктын бетине жездин кызгылт катмары пайда болот. Эритменин көгүш өӊү акырындап жашыл түскө өзгөрөт. Темир эритмеден жезди сүрүп чыгарат. Теӊдемеси томөнкүдөй:
CuSO4 + Fe = FeSO4 + Cu
Демек татаал зат менен жөнөкөй зат аракеттенишкенде татаал зат менен жөнөкөй зат орун алмашып , бир татаал зат жана жөнөкөй зат пайда болгон реакция орун алмашуу реакциясы деп аталат.
 Химиялык реакция жүргөндүгүн кандай билүүгө болот?
Химиялык реакция жүргөндүгүн кандай билүүгө болот?
( окуучулар өз алдынча иштешет, группада талкууланат)
Окуучу: заттын өӊү өзгөрөт.
Окуучу: газ бөлүнүп чыгат,
Мугалим : чөкмө пайда болот - деп кошумчалап сабак жыйынтыкталат. Окуучулар байкагандарын дептерине жазып жыйынтыкташат.
Окуучулардын билимдери бааланат.











 а) б) в) г)
а) б) в) г) бакыттын бирдиги –секунд, мүнөт, саат, сутка, ай, жыл.
бакыттын бирдиги –секунд, мүнөт, саат, сутка, ай, жыл. Көлөмдүн бирдиги – мл, л, тонна.
Көлөмдүн бирдиги – мл, л, тонна. угалим: лабораторияда заттарды тараза менен ченеп алышат.Ошондуктан бир эле учурда заттын массасы менен аны түзүп туруучу атом , молекуланын санын ченөөчү чен бирдикти кабыл алуу зарыл болду. Мындай бирдик моль деп мугалим окуучуларга билдирүү жасайт, да ага аныктама берилет. ( окуу китеби $16).
угалим: лабораторияда заттарды тараза менен ченеп алышат.Ошондуктан бир эле учурда заттын массасы менен аны түзүп туруучу атом , молекуланын санын ченөөчү чен бирдикти кабыл алуу зарыл болду. Мындай бирдик моль деп мугалим окуучуларга билдирүү жасайт, да ага аныктама берилет. ( окуу китеби $16).
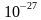 кг экендигин билип, көмүртек атомунун массасынын 1/12 бөлүгүндө 6,02
кг экендигин билип, көмүртек атомунун массасынын 1/12 бөлүгүндө 6,02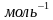 атом , молекула кармалат деген формула доскага жазылат. Демек моль - 6,02
атом , молекула кармалат деген формула доскага жазылат. Демек моль - 6,02










