
Муниципальное Бюджетное Общеобразовательное Учреждение Средняя Общеобразовательная Школа №1
Зачетная работа по элективному курсу:Химия в быту. « Жесткость воды и способы ее устранения»
Выполнили: Ученики 9 класса Б Серов В.М Силантьев А.А
Руководитель проекта
Учитель химии
Пермякова О.Е

Цель работы:
- Изучить понятие «жесткость воды», её влияние и способы устранения жесткости.
- Провести исследование жесткости различных видов воды.
- Проверить полученные знания по теме.

Содержание работы:
- Вода-источник всего живого.
- Определение жесткости воды и ее негативное влияние.
- Виды жесткости.
- Способы устранения жесткости.
- Уравнения устранения жесткости.
- Практическая часть.
- Тест «Проверь себя».
- Используемые материалы.

Вода-источник всего живого.
Вода́ —химическое вещество в виде прозрачной жидкости, не имеющей цвета, запаха и вкуса. Около 71 % поверхности Земли покрыто водой.

Вода-источник всего живого.
По особенностям происхождения, состава или применения, выделяют несколько видов воды: мягкая и жесткая вода, минеральная вода, дистиллированная вода…

Вода-источник всего живого.
Вода играет уникальную роль как вещество, определяющее возможность существования и саму жизнь всех существ на Земле. Она выполняет роль универсального растворителя, в котором происходят основные биохимические процессы живых организмов.

Жесткость воды.
Природная вода, проходя через известковые горные породы и почвы, обогащается солями кальция и магния ( а также железа) и становится жесткой.
Жесткость воды.
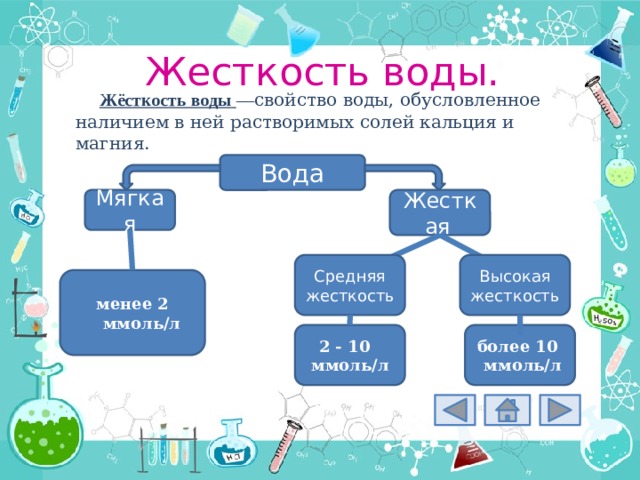
Жёсткость воды — свойство воды, обусловленное наличием в ней растворимых солей кальция и магния.
Вода
Жесткая
Мягкая
Средняя жесткость
Высокая жесткость
менее 2 ммоль/л
2 - 10 ммоль/л
более 10 ммоль/л

Негативное влияние.
- Заболевание суставов.
- Накопление солей в организме.
- Образованию камней в почках, желчном и мочевом пузырях.
- Образование накипи.
- Ухудшение вкуса пищи, приготовленной на жёсткой воде.
- Плохо растворяет мыло.
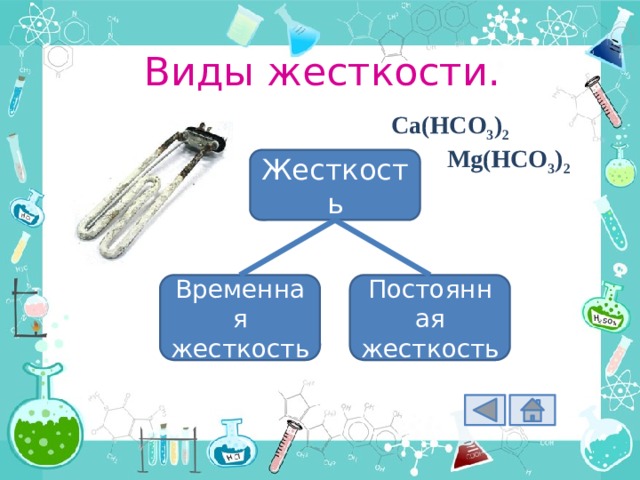
Виды жесткости.
Ca(HCO 3 ) 2
Mg(HCO 3 ) 2
Жесткость
Временная жесткость
Постоянная жесткость

Временная жесткость.
Временная жесткость вызвана присутствием в воде гидрокарбонатов кальция, магния и железа и устраняется простым кипячением. При этом гидрокарбонаты разлагаются, и в осадок выпадают вещества, образующие накипь.

Постоянная жесткость.
Постоянная жесткость обусловлена другими солями кальция и магния(сульфаты, хлориды, нитраты и др.). Такая жесткость не устраняется кипячением воды, так как растворы этих солей устойчивы к нагреванию.

Способы устранения жесткости.
Промышленные:
- Добавление кальцинированной соды Na 2 CO 3
- Добавление гашеной извести Ca(OH) 2
Бытовые:
- Кипячение и вымораживание
- Фильтрование
- Добавление умягчителей

Кипячение и вымораживание.
Кипячение снижает общую жесткость на 30-40%. При нагревании жесткой воды образуется накипь - нерастворимые соединения кальция, магния и оксид железа(III).
Вымораживание снижает общую жесткость на 70-80%.

Фильтрование.
Фильтрование снижает общую жесткость до 80%.Внутри картриджа фильтра содержится смесь из активированного угля и катионообменники. Уголь адсорбирует вредные органические вещества и хлориды. Катионообменники снижают общую жесткость.


Добавление умягчителей.
Снижение общей жёсткости достигает 100%. Умягчители предназначены для снижения общей жёсткости воды в стиральных машинах. Воду нельзя использовать для приготовления пищи, нельзя пить.

Добавление Na 2 CO 3 или Ca(OH) 2
Кроме кипячения, устранить временную жесткость можно гашеной известью Ca(OH) 2 .
Постоянную жесткость устраняют, обрабатывая воду раствором соды Na 2 CO 3 .

Уравнения устранения жесткости.
- Кипячение Добавление гашеной извести Ca(OH) 2
- Кипячение
- Добавление гашеной извести Ca(OH) 2
- Добавление соды Na 2 CO 3
- Добавление соды Na 2 CO 3

Устранение временной жесткости
Ca(HCO 3 ) 2 = CO 2 ↑ + CaCO 3 ↓ + H 2 O
Mg(HCO 3 ) 2 = Mg(OH) 2 ↓ + CO 2 ↑
- Добавление гашеной извести Ca(OH) 2
Ca(HCO 3 ) 2 + Ca(OH) 2 =2CaCO 3 +2H 2 O
Mg(HCO 3 ) 2 + Ca(OH) 2 =CaCO 3 xMgCO 3 +H 2 O

Устранение постоянной жесткости.
- Добавление соды Na 2 CO 3
- Добавление соды Na 2 CO 3
Ca(NO 3 ) 2 + Na 2 CO 3 = CaCO 3 ↓ + 2NaNO 3
2MgSO 4 +H 2 O + Na 2 CO 3 = Mg(OH) 2 CO 3 ↓+ CO 2 +2Na 2 SO 4

Практическая часть.
Практическая работа:
«Устранение жесткости различных видов воды».
Цель работы:
- Определить жесткость воды различных видов.
- Изучить способ устранения жесткости с помощью соды.
Оборудование и реактивы:
- Пробирки, химический стакан
- Раствор соды Na 2 CO 3.
- Цифровой фотоаппарат.

Практическая часть
Исследуемые растворы:
- Водопроводная вода
- Вода «Святой источник»
- Кипячёная вода

Практическая часть
Ход работы:
В нашей практической работе мы исследовали жесткость природной воды: «Святой источник», кипячёной воды и водопроводной воды. Для устранения жесткости можно использовать раствор соды Na 2 CO 3. Мы прилили раствор в три чашки и наблюдали за происходящим.


Практическая часть.
Уравнения:
MgCl 2 + Na 2 CO 3 = MgCO 3 ↓ + 2NaCl
CaCl 2 + Na 2 CO 3 = CaCO 3 ↓ + 2NaCl
Mg(HCO 3 ) 2 + Na 2 CO 3 = 2NaHCO 3 + MgCO 3 ↓
Ca(HCO 3 ) 2 + Na 2 CO 3 = 2NaHCO 3 + CaCO 3 ↓

Практическая часть.
Вывод:
Кипячёная вода обладает большей жесткостью, то есть содержит наибольшее количество солей магния и кальция. Этот вид воды наиболее пригоден для питья, так как даёт организму соли кальция и магния, но не пригоден для хозяйственных целей.

Тест «Проверь себя»
Вопрос №1
Вопрос №2
Вопрос №3
Вопрос №4
Вопрос №5
Вопрос № 6

Вопрос№1
Укажите мягкую воду
- Вода Чёрного моря
- Океаническая вода
- Дождевая вода
- Ключевая вода
- Минеральная вода

Вопрос№2
Какое свойство НЕ проявляет жёсткая вода?
- Хорошо проводит электрический ток
- Хорошо проводит тепло
- Образует накипь при кипячении
- Плохо растворяет мыло (мыло плохо пенится)

Вопрос№3
Какие вещества можно использовать для смягчения жесткой воды?
- Ca(OH) 2 и Na 2 CO 3
- H 2 SO 4 и CaSO 4
- NaHCO 3 и H 2 SO 4
- Na 2 CO 3 и H 2 SO 4

Вопрос№4
Укажите для каких целей пригодна жесткая вода.
- Для охлаждения двигателей внутреннего сгорания
- Орошения полей
- Для питания паровых
- Стирки белья

Вопрос№5
Какое вещество можно использовать для удаления накипи на внутренних стенках чайника?
- Пищевую соду
- Уксусную кислоту
- Поваренную соль
- Кальцинированную соду

Вопрос№6
Каким способом можно устранить постоянную жесткость воды?
- Добавлением соды
- Кипячением
- Добавлением гашеной извести
- Добавлением кислоты

МОЛОДЕЦ!
На ПЯТЕРОЧКУ нарабооотал!

Плохо!
На ДВОЕЧКУ потяяянет!

Используемые материалы.
- http://ru.wikipedia.org
- http://www.bestboilers.ru
- http://www.xumuk.ru

Спасибо за внимание!
































































