Просмотр содержимого документа
«Азот и его соединения»
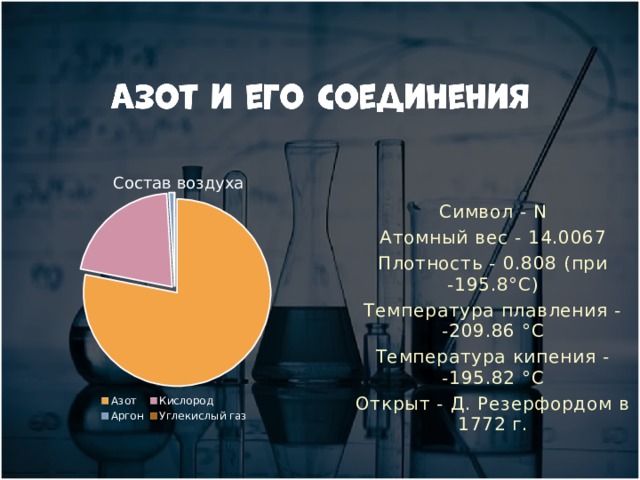
Символ - N
Атомный вес - 14.0067
Плотность - 0.808 (при -195.8°C)
Температура плавления - -209.86 °C
Температура кипения - -195.82 °C
Открыт - Д. Резерфордом в 1772 г.
Состав воздуха

Широко применяется в качестве хладагента в различном бытовом и промышленном оборудовании.

Цель данной работы:
изучение физических и химических свойств азота, его соединений и применении их в экспериментах.

Задачи работы:
1.Выявление значения азота для природы и деятельности человека.
2.Изучение физических и химических свойств азота.
3.Постановка эксперимента с калиевой селитрой.

- Аммиак (N 3 H)
- Соли аммония
- Жидкий азот

Соединения азота имеют огромное значение для различных отраслей промышленности и сельского хозяйства.
Азот считается основой всего живого, поскольку он входит в состав белков.

Бесцветный газ
Без запаха
Мало растворим в воде

Взаимодействие с водородом
Взаимодействие с металлами
Взаимодействие с кислородом
3H2 + N2 = 2NH3.
O2 + N2 = 2NO.
6Li + N 2 = 2Li 3 N.

- неорганическое соединение, калиевая соль азотной кислоты с формулой KNO3
- Практически не токсичен для живых организмов

Приготавливают насыщенный раствор калийной селитры KNO 3
опускают в него на 5-7 минут лист газетной бумаги.
По истечении указанного времени его вынимают из раствора и сушат

Затем вносят в пламя горелки, он не горит, а тлеет.

ВЫВОДЫ
- Выявили, что азот в качестве самостоятельного химического элемента является неотъемлемой частью живой природы, поскольку входит в состав белков.
- Подтвердили использование N 2 человеком в самых различных соединениях для осуществления промышленной, сельскохозяйственной, медицинской и повседневной деятельности.