Просмотр содержимого документа
«Презентация к уроку химии в 11 классе "Ионная связь"»

19 октября
Типы химической связи.
Ионная связь

Свойства
Изменение свойств
Радиус атома
В периодах
В группах
Умень-шается
Электроотрицательность
Увели-чива-
Металлические свойства,
(Способность атомов притягивать ē) ē
Увели-чивается
Неметаллические св-ва,
Умень-шается
Восстановительная спос.
Умень-шается
ется
Увели-чивается
Окислительная способн.
Увели-чивается
Умень-шается
+



 2 " width="640"
2 " width="640"
ИС – разница электроотрицательностей 2


Образование ионов
Атом 0 – ē Катион +
Атом 0 + ē Анион -

:
:
:
:
переход ē
_
+
0
0
:
:
.
*
.
Na
Cl
Na + Cl
*
эо Na 0 эоCl 0
0,9 3,0
Силы электростатического притяжения
или ионная связь

Механизм образования ИС (ионной связи).
-
+
M
·
H
·

Na 0 +11))) (((+17 Cl 0
2 8 1 782
Na + +11)) (((+17 Cl -
28 882

КАТИОН
АНИОН
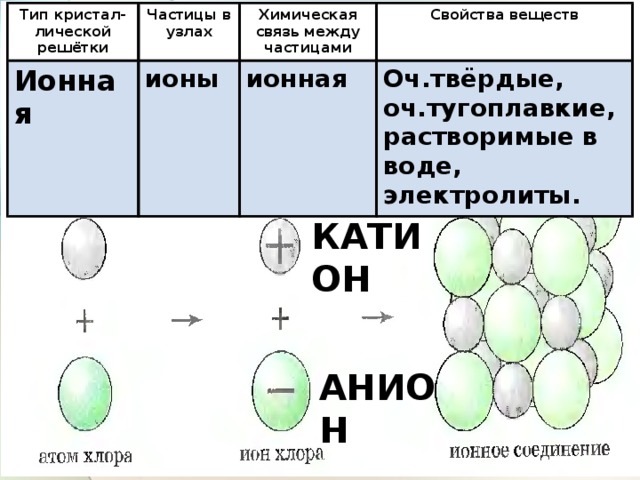
Тип кристал-лической решётки
Частицы в узлах
Ионная
Химическая связь между частицами
ионы
Свойства веществ
ионная
Оч.твёрдые, оч.тугоплавкие, растворимые в воде, электролиты.
КАТИОН
АНИОН

+
-
+
-
+
-
+
-
-
+
+
-
-
+
+
-
+
+
+
-
+
-
-
+
+
+
-
-
-
-
+
+
+
-
+
-
+
-
+
-
-
+
+
-
+
-
+
+
+
-
+
-
-
-
+
-
+
+
-
-
+
+
+
-
+
+
-
-
-
+
-
+
+
-
+
-
-
-
+
+
-
+
-
-
-
+
Механизм электролитической диссоциации
веществ с ионной связью
Рис.4 .
Раствор
-
-
+
+
+
-
-
+
-
-
-
+
+
-
-
+
+
+
+
-
-
-
+
+
+
-
+
-
+
Рисунок 1.
Н 2 О
Кристалл
Гидратированные ионы
NaCl → Na + + Cl -
14

ГИДРАТАЦИЯ –
реакция соединения веществ (молекул, атомов, ионов) с водой

Электролиты
Катод
-
Анод
+
-
+
Катионы
-
+
-
+
Анионы
-
+

Термины:
Электроотрицательность
Ионы
Катион
Анион
Ионная связь
Простые и сложные ионы
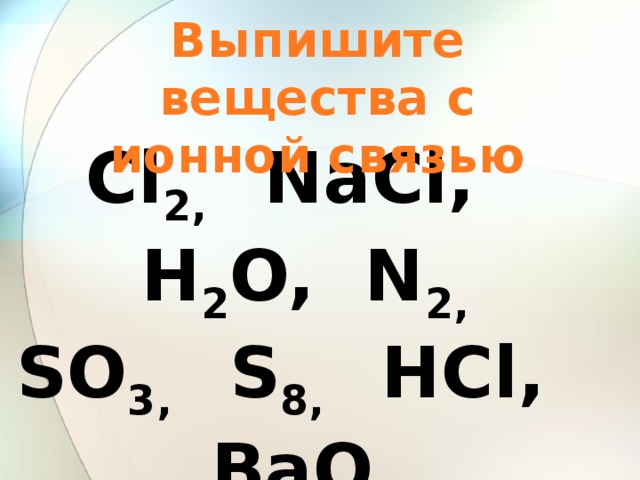
Выпишите вещества с ионной связью
Cl 2, NaCl, H 2 O, N 2,
SO 3, S 8, HCl, BaO,
P 4, P 2 O 5, NO 2, K 2 O, LiF, H 2, AlBr 3,

Выпишите вещества с ионной связью
Cl 2, NaCl , H 2 O, N 2,
SO 3, S 8, HCl, BaO ,
P 4, P 2 O 5, NO 2, K 2 O , LiF , H 2, AlBr 3 ,

Металл Неметалл
Na Cl
Ba O
K 2 O
Li F
Al Br 3

Домашнее задание:
Учить §3,
упр. 6,7,8,9 письменно










 2 " width="640"
2 " width="640"

























