Просмотр содержимого документа
«Рабочий лист»
Рабочий лист №1
Тема урока: Реакции разложения.
Знать: что такое реакции разложения.
Уметь : записывать реакции разложения.
Задание 1. Ответь на вопросы.
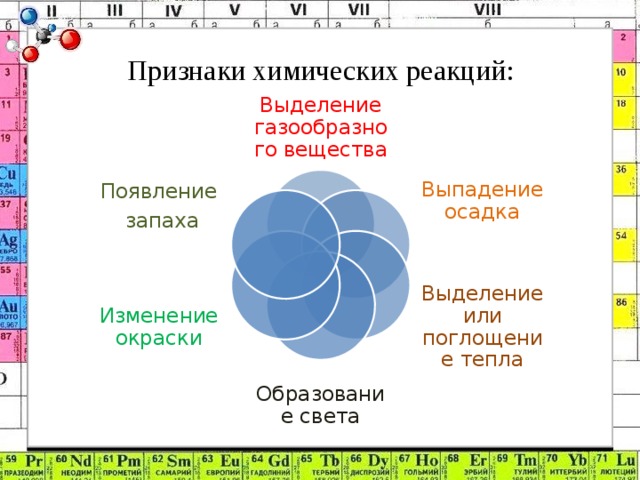
1.Какие условия протекания реакции вам известны? --------------------------------- ------------------------------------------------------------------------------------- ---------------------- ----------------------------------------------------------------------------------------------------------
2.Как еще называют химические явления? ------------------------------------------
3.Приведите примеры химических явлений. ----------------------------------------------------- ---------------------------------------------
Задание№2.
Записать разложения воды в виде химической реакции:
 ____H2O____........._+_.........__________
____H2O____........._+_.........__________
Задание №3


 Записать уравнение реакции разложения малахита (CuOH)2CO3 …..+…….+………
Записать уравнение реакции разложения малахита (CuOH)2CO3 …..+…….+………
Задание №4
Записать уравнение реакции разложения бихромата аммония
 (NH4) 2Cr2O7 -------------------------------- ---------------------
(NH4) 2Cr2O7 -------------------------------- ---------------------
Задание №4
Реакция разложения это……………………………………………………………………………
………………………………………………………………………………………………………………………
Рабочий лист №2
Выполняя опыты, соблюдай правила техники безопасности.!!!!!!!
Опыт №1 нагрейте пероксид водорода. Идет реакция? (Очень медленно). Добавьте в пробирку с пероксидом водорода( немного) оксид марганца (IV). Что наблюдаете? (Выделение газа). Проверяем тлеющей лучинкой, она ярко вспыхивает. Значит, образовавшийся газ – это кислород.
Записываем уравнение реакции разложения пероксида водорода и в рабочем листе и на доске.
H2O2=……. +…….
Опыт №2 вместо оксида марганца (IV) можно положить кусочек сырого картофеля, реакция тоже пойдет быстрее.
Задание №5 Взаимопроверка
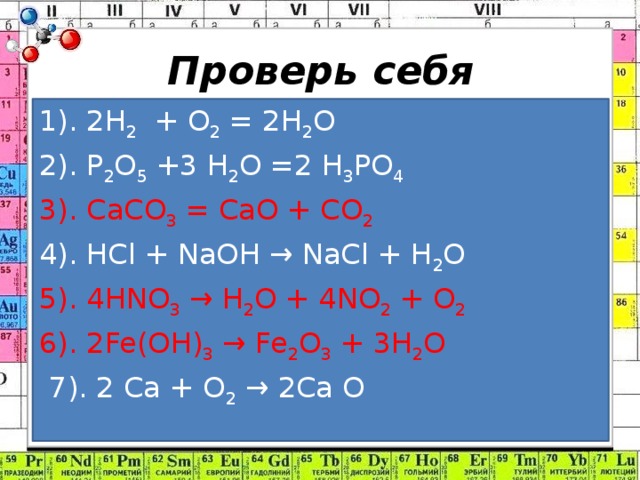
Даны схемы химических реакций:
1).2H2 + O2 = 2H2O
2).P2O5 + H2O = H3PO4
3).CaCO3 = CaO + CO2
4).HCl + NaOH → NaCl + H2O
5). 4HNO3 → 2H2O + 4NO2 + O2
6).2Fe(OH)3 → Fe2O3 + 3H2O
7). 2Ca + O2 → 2CaO
Отметь реакции разложения. Под какими цифрами написаны реакции разложения
Просмотр содержимого презентации
«презентация к уроку»





 ____
____

 (
(