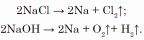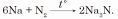Tema:Natriý.
Meýilnamasy:
1.Natriniň açylyşy.
2.Natriniň fiziki häsiýetleri.
3.Natriniň himiki häsiýetleri.
4.Natriniň izotoplary.
5.Natriniň alnyşy.
6.Natriniň ulanylyşy.
7.Natriniň elementiniň önümleri.
Na duzlar görnüşinde tebigatda giňden ýaýrandyrlar. Olardan NaCl – galit, daş duzy, Na2SO4•10H2O – mirabilit, KCl – silwin, KCl•NaCl – silwinit, KCl•MgCl2•6H2O – karnallit ýaly minerallary mysal hökmünde görkezmek bolar. Bulardan başga-da, tebigatda NaNO3, Na2CO3•10H2O, Na2B4O7•10H2O duşýar. Ýerüsti ösümlikleriň külünde K2CO3, suwotularyň külünde Na2CO3 bardyr.
Türkmenistanda natriý elementleriniň duzlary birnäçe ýerlerde (daş duzy NaCl (Babahojada, Jebelde, Köýtendagda), glauber duzy Na2SO4•10H2O (Garabogaz köl aýlagynda), silwinit (Garlykda, Köýtendagda, Garabilde) duş gelýär.
Natriý elementleriniň alnyşy. Natriý elementini 1807-nji ýylda iňlis alymy G.Dewi tarapyndan açyldy.
Natriý elementi nahar duzunyň NaCl ýa-da natriý gidroksidiniň NaOH rasplawyny elektroliz etmek usuly bilen alynýar:
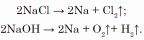
Natriý elementiň fiziki häsiýetleri. Natriý kümüşsöw ak reňkli ýumşak metallardyr. Ol suwuk hala geçmek temperaturasy litiý elementiniňkiden pesdir, ýagny aňsat suwuk hala geçýärler. Ol howada durnuksyzdyrlar.
Natriý elementiň himiki häsiýetleri. Bu element himiki taýdan işjeň metaldyr. Olar himiki reaksiýalarda diňe gaýtaryjy häsiýetleri ýüze çykarýar. Birleşmelerinde bu element diňe bir walentlidirler we okislenme derejesi diňe +1 bolup bilýär. Natriý birnäçe sada we çylşyrymly maddalar bilen reagirleşýärler. Natriý elementi kislorod bilen otag temperaturasynda reagirleşýärler. Litiý elementinden tapawutlylykda, reaksiýa netijesinde natriý peroksidi emele gelýär:
2Na + O2 (howa) → Na2O2 (ýanýar, garyndy Na2O);
Natriý elektrik razrýadynda azot bilen reagirleşýär.
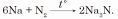
Natriý galogenler bilen reagirleşýär we netijede, bu elementiň galogenidi emele gelýär:
2Na + Cl2 → 2NaCl;
Natriý otag temperaturasynda suw bilen reagirleşýär. Şonda wodorod bölünip çykýar:
2Na + 2H2O → 2NaOH + H2;
Otag temperaturasynda natriý duz kislotasynyň gowşadylan ergini bilen reagirleşýär. Şonda wodorod bölünip çykýar.
2Na + 2HCl → 2NaCl + H2;
Natriý elementiniň birleşmelerinden natriý hloridi, natriý karbonatlary, natriý sulfaty we beýlekiler köp maddalary almak üçin başlangyç maddadyr. Ondan başga- da, NaCl iýmitiň düzümine we ot-iýme goşulýar.
Natriý karbonaty (soda) alýuminiý, aýna, sabyn önümçiliklerinde ulanylýar. NaOH emeli süýümleri we boýaglary almakda, nebit önümlerini arassalamakda giňden ulanylýar. Na2O2 agartmakda we zyýansyzlandyrmakda (dezinfeksiýa), Na2SO4 aýna önümçiliginde, mineral dökün hökmünde ulanylýar.
Natriý metalynyň howada ýanyşy. Natriý gidroksidiniň alnyşy.
Natriý metalynyň bir bölejigini pyçak bilen kesip, ony demirden ýasalan çemçejikde gyzdyrsak, ol howada otlanýar we ýanmak netijesinde natriý peroksidini emele getirýär:
2Na + O2 → Na2O2.
Tejribe sorujy şkafda geçirilse, gowy bolar.
Emele gelen natriý peroksidi örän işjeň madda bolup, sirke kislotasy bilen garylanda, ol otlanýar. Şonuň ýaly-da, kömür, kükürt, ownadylan ýagdaýyndaky metallar, natriý peroksidi bilen güýçli reagirleşýärler. Bolup geçýän reaksiýalaryň deňlemelerini ýazyň. Natriý peroksidi bilen kömürturşy gazynyň arasynda geçýän «organiki däl fotosinteziň» deňlemesini ýazyň. Şonda natriý peroksidi bilen birlikde, az mukdarda, onuň oksidi hem emele gelýär. Diýmek, bu tejribede natriý metalyny howada ýakyp alan reňkli maddamyz natriý peroksidi bilen natriý oksidiniň garyndysydyr. Arassa natriý oksidini almak üçin natriniň nitratyna natrini täsir etdirýärler. Şonda natriý oksidi bilen birlikde azot hem bölünip çykýar.

Natriý peroksidi, şonuň ýaly-da, natriý oksidi suwda eredilse, iki ýagdaýda hem erginde natriý gidroksidi emele gelýär. Bu tejribäni geçirmek üçin ýokarky tejribe işinde, natriý metalyny howada ýakmak netijesinde, alnan garyndyny bir bulgur suwda eredeliň. Şonda alnan ergine lakmus kagyzyny batyryp, olaryň reňki boýunça haýsy maddanyň emele gelendigini kesgitleýäs. Reaksiýanyň deňlemesini ýazyp. Tejribe işi geçirilende alnan maddalar elimize degse ýa-da degmese-de, tejribe işini geçirip bolanyňyzdan soňra elimizi suw akdyryp, tä ýylmançaklyk aýrylýança, ýuwýaň