Сабақ жоспары / План урока
Пән / Предмет ХИМИЯ
Сынып/Класс ДЕВЯТЫЙ Сабақ / Урок № 55 Күні / Дата 08.04.2013 год
Тақырыбы / Тема: Бензол. Получение из ацетилена. Физические свойства и применение.
Генетическая связь между углеводородами.
Сабақтың мақсаты / Цель урока: ознакомить с ароматическими углеводородами на примере бензола.
Білімділік / 0бразоватепъная:\ объяснить причину ароматичности, рассмотрев строение молекулы бензола; ознакомить с его свойствами, применением.
Дамытушылық / Развивающая: развивать умения устанавливать взаимосвязь между строением молекулы и свойствами веществ; сравнивать, анализировать; развивать умения использовать теоретические знания на практике.
Тәрбиелік / Воспитательная: воспитывать умение сосредоточиться, организоваться.
Көрнекілігі / Оборудование: доска, интерактивная доска, флипчарт, компьютер;бензол, бромная вода, пробирки, штатив.
Пәнаралық байланыс Межпредметныe связи:
География.
Сабақ барысы / Ход урока:
1.Ұйымдастыру кезені
Организационный момент
Приветственное слово учителя. Организация учащихся.
2.Үй тапсырмасы тексеру
Проверка домашнего задания.
Таблица
| У глеводороды глеводороды Характеристика | Алканы | Алкены | Алкины |
| 1.Общая формула | СnH2n+2 | СnH2n | СnH2n-2 |
| 2.Гибридизация | sp3- | sp2 | sp |
| 3.Наличие кратных связей | - | -С=С- | -С≡С- |
| 4.Угол между σ-связями | 109028, | 1200 | 1800 |
| 5.Простейший представитель | СН4 МЕТАН | С2Н4 ЭТИЛЕН (этен) | С2Н2 АЦЕТИЛЕН (этин) |
Сравните свою таблицу с данной. Внесите изменения. Что вы еще можете добавить?
3.Білімін тексеру
Проверка знаний:
Какая масса карбида кальция потребуется при сжигании 1м3 ацетилена (у.н.), если выход ацетилена составляет 60% по сравнению с теоретически возможным?
Ответ: 4760кг.
4.Жана тақырыптың мазмұны
Изложение нового материал:
Какова молекулярная формула углеводорода, массовая доля углерода в котором 93,2%. Плотность паров вещества по водороду равна 39.
( В результате решения задачи получена формула С6Н6.
УЧИТЕЛЬ:
К какому классу известных вам углеводородов можно отнести данное вещество?
-Полученный углеводород к изученным классам отнести нельзя, так как его формула не соответствует ни одной общей формуле известных углеводородов.
УЧИТЕЛЬ:
Данное вещество относится к ароматическим углеводородам. Называется оно - БЕНЗОЛ.
Какова же структурная формула бензола?
Предположительно в молекуле бензола ( согласно молекулярной формуле) должны быть кратные связи.
Возможно его формула СН2=СН-С≡С-СН=СН2.
Наличие кратных связей можно определить при помощи реакции взаимодействия непредельного углеводорода с бромной водой.В результате реакции бромная вода обесцвечивается.
( Демонстрация опыта: в пробирку наливается бромная вода (2 мл) и приливается 1 мл бензола).
Что вы наблюдаета?
-Бромная вода не изменилась.
Каково же строение молекулы бензола?
В специально оборудованных лабораториях проводят следующий опыт:
Бензол нагревают в присутствии катализатора с водородом, при этом получают вещество с молекулярной формулой С6Н12. Это вещество не обесвечивает бромную воду, значит оно относится к предельным углеводородам. Структурная формула данного вещества
 .
.
Следовательно молекула бензола тоже имеет циклическое строение. Но судя по молекулярной формуле, должны быть и кратные связи. В 1865 году Кекуле доказал, что в молекуле бензола простые связи чередуются с двойными. Структурная формула бензола выглядит так: или
или  .
.
Такая структура молекулы определяет иные свойства бензола в отличие от других непредельных углеводородов.
Бензол может при определённых условиях присоеденять атомы хлора, но гораздо легче в молекуле бензола происходит замещение атомов водорода на другие атомы и группы атомов. Эту способность назвали ароматичностью.
Как же образуется молекула бензола?
Атомы углерода в молекуле бензола имеют sp2-гибридизацию. Все шесть орбиталей перекрываются над и под плоскостью с соседними р-орбиталями, располагаясь перпендикулярно плоскости с σ-связями.
В результате образуется единая π- система, состоящая из 6 р-орбиталей. Образуется 6 π-электронная система. В результате электронная плотность σ-связей и р-электронов распределяется равномерно, поэтому все связи в молекуле бензола одинаковые и прочные – это и есть ароматичность.
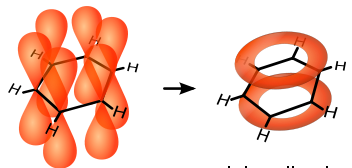
Такое строение молекулы бензола объясняет его свойства.
Итак, молекула бензола –правильный шестиугольник, в которой простые связи чередуются с двойными.
Какова же общая формула ароматических углеводородов: СnH2n-6
Получение.
Бензол получают из каменноугольной смолы, нефти, газов, образующихся при коксовании угля.
А также синтезируют из ацетилена: 3С2Н2→С6Н6.
Физические свойства.
Бензол- бесцветная, маслянистая жидкость с характерным запахом. Не растворяется в воде. ЯДОВИТ!
Химические свойства.
Также как и другие углеводороды бензол горит в кислороде сильно коптящим пламенем. (Почему?)
2С6Н6+ 15О2→12СО2+6Н2О
При обычных условиях бензол инертен. Вреакцию вступает при нагревании и в присутствии катализатора.
Применение:
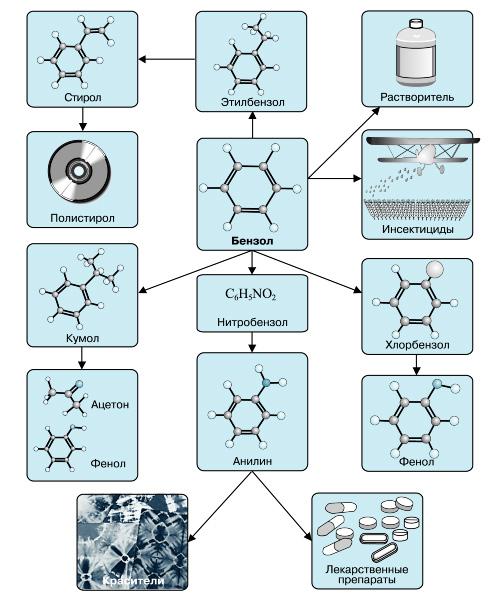
Органический растворитель.
Получение красителей.
Изготовление взрывчатых веществ.
Производство ядохимикатов.
Изготовление лекарственных препаратов.
5.Өгілген тықырыпты бекіту
Первичное закрепление изученного материала:
Выполнить задание 5 стр.161.
СН4→С2Н2→С6Н6
Итог урока:
1.С каким углеводородом вы познакомились на уроке?
2.В чём особенность данного углеводорода?
3.Как его можно получить?
4.Где его применяют?
|6. Үйге тапсырма беру
Задание на дом:
§50.





 глеводороды
глеводороды .
.











