10 класс
Дата ___20.01.2022_____
Тема : Этиленгликоль и глицерин как представители предельных многоатомных спиртов. Качественная реакция на многоатомные спирты и ее применение для распознавания глицерина в составе косметических средств. Практическое применение этиленгликоля и глицерина.
Цель: дать понятие об многоатомных спиртах, свойствах и примении.
Оборудование: Образцы глицерина, модели молекул изображенных на доске или в табл. Реактивы (Глицерин, гидроксид меди), лаб. посуда.
Ход урока:
Организационный момент.
Проверка отсутсвующих.
Проверка готовности к уроку.
Изучение нового материала.
Многоатомные спирты – органические соединения, в молекулах которых содержится несколько гидроксильных групп (-ОН), соединённых с углеводородным радикалом
Гликоли (диолы)

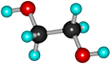
Этиленгликоль (этандиол)
Формула
Модели молекулы
шаростержневая
полусферическая
HO-CH2CH2-OH

Физические свойства многоатомных спиртов
- Сиропообразная, вязкая бесцветная жидкость, имеет спиртовой запах, хорошо смешивается с водой, сильно понижает температуру замерзания воды (60%-ый раствор замерзает при -49 ˚С) –это используется в системах охлаждения двигателей – антифризы.
–Этиленгликоль токсичен – сильный Яд! Угнетает ЦНС и поражает почки.
Триолы

Глицерин (пропантриол-1,2,3)
Формула
Модели молекулы
шаростержневая
полусферическая
HOCH2-СH(OH)-CH2OH


–Бесцветная, вязкая сиропообразная жидкость, сладкая на вкус. Не ядовит. Без запаха. Хорошо смешивается с водой.
–Распространён в живой природе. Играет важную роль в обменных процессах, так как входит в состав жиров (липидов) животных и растительных тканей.
Номенклатура
В названиях многоатомных спиртов (полиолов) положение и число гидроксильных групп указывают соответствующими цифрами и суффиксами -диол (две ОН-группы), -триол (три ОН-группы) и т.д. Например:

Получение многоатомных спиртов
Получение двухатомных спиртов
В промышленности
1. Каталитическая гидратация оксида этилена (получение этиленгликоля):
2. Взаимодействие дигалогенпроизводных алканов с водными растворами щелочей:

3. Из синтез-газа:
2CO + 3H2 250°,200МПа,kat → CH2(OH)-CH2(OH)
В лаборатории
1. Окисление алкенов:
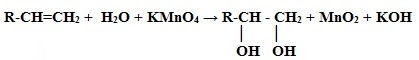
Получение трёхатомных спиртов (глицерина)
В промышленности
Омыление жиров (триглицеридов): Химические свойства многоатомных спиртов:
Химические свойства многоатомных спиртов:
Кислотные свойства
1. С активными металлами: HO-CH2-CH2-OH + 2Na → H2↑+ NaO-CH2-CH2-ONa (гликолят натрия)
2. С гидроксидом меди(II) – качественная реакция!

Упрощённая схема
Основные свойства
С галогенводородными кислотами
HO-CH2-CH2-OH + 2HCl H+↔ Cl-CH2-CH2-Cl + 2H2O
С азотной кислотой
 Тринитроглицерин - основа динамита
Тринитроглицерин - основа динамита
Применение
– Этиленгликоль производства лавсана, пластмасс, и для приготовления антифризов — водных растворов, замерзающих значительно ниже 0°С (использование их для охлаждения двигателей позволяет автомобилям работать в зимнее время); сырьё в органическом синтезе.
– Глицерин широко используется в кожевенной, текстильной промышленности при отделке кож и тканей и в других областях народного хозяйства. Сорбит (шестиатомный спирт) используется как заменитель сахара для больных диабетом. Глицерин находит широкое применение в косметике, пищевой промышленности, фармакологии, производстве взрывчатых веществ. Чистый нитроглицерин взрывается даже при слабом ударе; он служит сырьем для получения бездымных порохов и динамита ― взрывчатого вещества, которое в отличие от нитроглицерина можно безопасно бросать. Динамит был изобретен Нобелем, который основал известную всему миру Нобелевскую премию за выдающиеся научные достижения в области физики, химии, медицины и экономики. Нитроглицерин токсичен, но в малых количествах служит лекарством, так как расширяет сердечные сосуды и тем самым улучшает кровоснабжение сердечной мышцы.
Закрепление нового материала. Л/О № 3 Растворение глицерина в воде. Реакция глицерина с гидроксидом меди»
Цель: изучить свойства гицерина в воде и с гидроксидом меди.
Оборудование: штатив с пробирками, глицерин, гидроксид натрия, сульфат меди, вода
Ход работы:
Правила ТБ.
Выполнение работы по инструкции.

Вывод:

ИЛИ С увеличением числа гидроксильных групп в молекуле вещества возрастает подвижность атомов водорода, т. е. увеличиваются кислотные свойства. Поэтому атомы водорода могут замещаться не только на активные щелочные металлы. Так, например, многоатомные спирты взаимодействуют с гидроксидом меди в щелочной среде (уравнение приведено в упрощенном виде) : 
 упрощенный вид реакции
упрощенный вид реакции
При взаимодействии гидроксида меди (II) с глицерином и другими многоатомными спиртами в присутствии щелочи происходит растворение гидроксида и образуется комплексное соединение синего цвета. Эта реакция используется для обнаружения многоатомных спиртов
Рефлексия.
Выставление оценок.
Д/з § 21, стр 104, № 4,7
















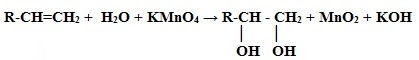
 Химические свойства многоатомных спиртов:
Химические свойства многоатомных спиртов: 

 Тринитроглицерин - основа динамита
Тринитроглицерин - основа динамита


 упрощенный вид реакции
упрощенный вид реакции









