Контрольная работа за I полугодие
1 вариант
11а
1. На рисунке изображена модель электронного строения атома некоторого химического элемента.
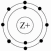
На основании анализа предложенной модели выполните следующие задания:
1) определите химический элемент, атом которого имеет такое электронное строение;
2) укажите номер периода и номер группы в Периодической системе химических элементов Д. И. Менделеева, в которых расположен этот элемент;
3) определите, к металлам или неметаллам относится простое вещество, которое образует этот химический элемент.
2. Составьте электронную формулу атомов элементов: селен, ртуть.
3. Периодическая система химических элементов Д. И. Менделеева – богатое хранилище информации о химических элементах, их свойствах и свойствах их соединений. Так, например, известно, что с увеличением порядкового номера химического элемента радиусы атомов в периодах уменьшаются, а в группах увеличиваются.
Учитывая эти закономерности, расположите в порядке уменьшения радиусов атомов следующие элементы: фосфор, углерод, азот, кремний. В ответе запишите символы элементов в нужной последовательности.
4. Проследите изменение электроотрицательности в следующем ряду элементов:
I – Cl – P – N – O – Se – Br
5.

6. Определите тип химической связи в следующих веществах:
FеСl3, SO3, HBr, Р2О5, СrО, Н2, Cu
7. Вычислите массовую долю (в процентах) соли в растворе, полученном при сливании 120 г 7%-го раствора и 30 г 35%-го раствора этой соли. Ответ запишите с точностью до десятых.
8. К 8%–ному раствору соли добавили 20 г 24%–го раствора этой же соли и получили 10%–ный раствор. Вычислите массу воды (в граммах), которая содержалась в исходном 8%–ном растворе. Ответ запишите с точностью до десятых.
9. Составьте уравнение возможной диссоциации веществ:
SiO2, MnCl2, HClO4, Na2CrO4, Cr(NO3)3, Al2(SO4)3, Mg(OH)2
Контрольная работа за I полугодие
1 вариант
11б
1. На рисунке изображена модель электронного строения атома некоторого химического элемента.
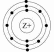
На основании анализа предложенной модели выполните следующие задания:
1) определите химический элемент, атом которого имеет такое электронное строение;
2) укажите номер периода и номер группы в Периодической системе химических элементов Д. И. Менделеева, в которых расположен этот элемент;
3) определите, к металлам или неметаллам относится простое вещество, которое образует этот химический элемент.
2. Составьте электронную формулу атомов элементов: цинк, свинец.
3. Периодическая система химических элементов Д. И. Менделеева – богатое хранилище информации о химических элементах, их свойствах и свойствах их соединений. Так, например, известно, что с увеличением порядкового номера химического элемента способность отдавать электроны – восстановительная способность – в периодах ослабевает, а в группах усиливается.
Учитывая эти закономерности, расположите в порядке усиления восстановительной способности следующие элементы: рубидий, натрий, литий, калий. В ответе запишите символы элементов в нужной последовательности.
4. Проследите изменение радиусов атомов в следующем ряду элементов:
Li – O – S – Si – C – F – Br
5.
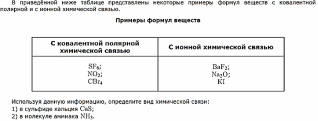
6. Определите тип химической связи в следующих веществах:
CuO, HF, O2, Na2O, Аl, ВаO, Сr
7. Вычислите массовую долю (в %) соли в растворе, полученном после добавления 50 мл воды и 10 г соли к 200 г 12%-го раствора этой же соли. Ответ запишите с точностью до целых.
8. Из 8%-го раствора гидроксида натрия выпарили 24 мл воды и получили 10%-ный раствор. Вычислите массу (в граммах) исходного раствора гидроксида натрия. Ответ представьте в виде целого числа.
9. Составьте уравнение возможной диссоциации веществ:
CuCl2, PbS, HNO3, K3PO4, Zn(OH)2, Fe2(SO4)3, Zn(NO3)2
Контрольная работа за I полугодие
1 вариант
11г
1. На рисунке изображена модель электронного строения атома некоторого химического элемента.

На основании анализа предложенной модели выполните следующие задания:
1) определите химический элемент, атом которого имеет такое электронное строение;
2) укажите номер периода и номер группы в Периодической системе химических элементов Д. И. Менделеева, в которых расположен этот элемент;
3) определите, к металлам или неметаллам относится простое вещество, которое образует этот химический элемент.
2. Составьте электронную формулу атомов элементов: мышьяк, тантал.
3. Периодическая система химических элементов Д. И. Менделеева – богатое хранилище информации о химических элементах, их свойствах и свойствах их соединений. Так, например, известно, что с увеличением порядкового номера химического элемента радиусы атомов в периодах уменьшаются, а в группах увеличиваются.
Учитывая эти закономерности, расположите в порядке увеличения радиусов атомов следующие элементы: углерод, бор, бериллий, азот. В ответе запишите символы элементов в нужной последовательности.
4. Проследите изменение основных свойств оксидов в следующем ряду элементов:
K – Na – Al – B – Be – Ca – K
5.

6. Определите тип химической связи в следующих веществах:
NO, S8, NaCl, Ca, K3N, MgO, SO2
7. Вычислите массу воды (в граммах), которую нужно выпарить из 200 г 12%-го раствора нитрата натрия, чтобы получить раствор, в котором массовая доля соли равна 20%. Ответ запишите с точностью до целых.
8. К 10%-ному раствору соли добавили некоторое количество этой же соли и получили 300 г 19%-го раствора. Вычислите массу соли (в граммах), добавленной к исходному раствору. В ответ запишите целое число.
9. Составьте уравнение возможной диссоциации веществ:
FeCl3, N2O5, HMnO4, NH4NO3, Ca(HCO3)2, Al2(SO4)3, Cr(OH)3
Контрольная работа за I полугодие
1 вариант
11л
1. На рисунке изображена модель электронного строения атома некоторого химического элемента.
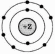
На основании анализа предложенной модели выполните следующие задания:
1) определите химический элемент, атом которого имеет такое электронное строение;
2) укажите номер периода и номер группы в Периодической системе химических элементов Д. И. Менделеева, в которых расположен этот элемент;
3) определите, к металлам или неметаллам относится простое вещество, которое образует этот химический элемент.
2. Составьте электронную формулу атомов элементов: рубидий, висмут.
3. Периодическая система химических элементов Д. И. Менделеева – богатое хранилище информации о химических элементах, их свойствах и свойствах их соединений. Так, например, известно, что с увеличением порядкового номера химического элемента в периодах электроотрицательность элементов увеличивается, а в группах – уменьшается.
Учитывая эти закономерности, расположите в порядке увеличения электроотрицательности следующие элементы: фтор, кислород, бериллий, сера. Запишите знаки элементов в нужной последовательности.
4. Проследите изменение радиуса атомов в следующем ряду элементов:
O – Sе – К – Nа –Cl – F – Be
5.

6. Определите тип химической связи в следующих веществах:
Ba, CO2, HCl, K2O, O3, HI, Ca2Si
7. Вычислите массу воды (в граммах), которую нужно выпарить из 200 г 12%-го раствора нитрата натрия, чтобы получить раствор, в котором массовая доля соли равна 20%. Ответ запишите с точностью до целых.
8. К 40%-ному раствору соли добавили 120 мл воды и получили раствор, в котором массовая доля воды равна 75%. Вычислите массу соли (в граммах), которая содержалась в исходном растворе. В ответ запишите целое число.
9. Составьте уравнение возможной диссоциации веществ:
Ag2O, ZnBr2, KHCO3, H3BO3, Fe2(SO4)3, Mn(NO3)2, (NH4)2S

























