Контрольная работа за I полугодие
2 вариант
11а
1. На рисунке изображена модель электронного строения атома некоторого химического элемента.
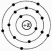
На основании анализа предложенной модели выполните следующие задания:
1) определите химический элемент, атом которого имеет такое электронное строение;
2) укажите номер периода и номер группы в Периодической системе химических элементов Д. И. Менделеева, в которых расположен этот элемент;
3) определите, к металлам или неметаллам относится простое вещество, которое образует этот химический элемент.
2. Составьте электронную формулу атомов элементов: мышьяк, висмут.
3. Периодическая система химических элементов Д. И. Менделеева – богатое хранилище информации о химических элементах, их свойствах и свойствах их соединений. Так, например, известно, что с увеличением порядкового номера химического элемента оснóвный характер оксида в периодах уменьшается, а в группах возрастает.
Учитывая эти закономерности, расположите в порядке усиления основности оксидов следующие элементы: натрий, алюминий, магний, бор. Запишите символы элементов в нужной последовательности.
4. Проследите изменение радиуса атомов в следующем ряду элементов:
Rb – Na – S – O – C – Sn – Sr
5.

6. Определите тип химической связи в следующих веществах:
Na2S, I2O7, H2O, Cu, Br2, Mg3N2, NH3
7. Вычислите массу воды (в граммах), которую необходимо выпарить из 150 г 7%-го раствора соли, чтобы получить 10,5%-ный раствор. Ответ запишите с точностью до целых.
8. Какую массу 63%-ного раствора азотной кислоты надо добавить к 122 г воды, чтобы получить 20%-й раствор? (Ответ округлите до ближайшего целого числа.)
9. Составьте уравнение возможной диссоциации веществ:
P4O10, AlF3, K2Cr2O7, H2SO3, Ca(HCO3)2, Al(OH)3, Ba(HS)2
Контрольная работа за I полугодие
2 вариант
11б
1. На рисунке изображена модель электронного строения атома некоторого химического элемента.
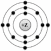
На основании анализа предложенной модели выполните следующие задания:
1) определите химический элемент, атом которого имеет такое электронное строение;
2) укажите номер периода и номер группы в Периодической системе химических элементов Д. И. Менделеева, в которых расположен этот элемент;
3) определите, к металлам или неметаллам относится простое вещество, которое образует этот химический элемент.
2. Составьте электронную формулу атомов элементов: селен, тантал.
3. Периодическая система химических элементов Д. И. Менделеева – богатое хранилище информации о химических элементах, их свойствах и свойствах их соединений, о закономерностях изменения этих свойств, о способах получения веществ, а также о нахождении их в природе. Например, известно, что с увеличением порядкового номера химического элемента в периодах электроотрицательность атомов увеличивается, а в группах – уменьшается.
Учитывая эти закономерности, расположите в порядке уменьшения электроотрицательности следующие элементы: бор, углерод, азот, алюминий. Запишите обозначения элементов в нужной последовательности.
4. Проследите изменение металлических свойств в следующем ряду элементов:
Вe – O – Sе – К – Ca – Mg – Ba
5.

6. Определите тип химической связи в следующих веществах:
SF6, FeCl2, P4, PCl5, K3N, Fe, Al2O3
7. Какую массу соли (г) надо добавить к 400 г 18%-ного раствора соли для получения раствора с массовой долей растворённого вещества 22%? (Запишите число с точность до тысячных.)
8. Вычислите массу 15%-го раствора соли, который нужно добавить к 210 г 20%-го раствора этой же соли, чтобы получить 18%-ный раствор. Ответ запишите с точностью до целых.
9. Составьте уравнение возможной диссоциации веществ:
CrO3, H2S, NaH2PO4, KBrO3, Fe(OH)3, Ba(OH)2, Cr2(SO4)3
Контрольная работа за I полугодие
2 вариант
11г
1. На рисунке изображена модель электронного строения атома некоторого химического элемента.
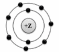
На основании анализа предложенной модели выполните следующие задания:
1) определите химический элемент, атом которого имеет такое электронное строение;
2) укажите номер периода и номер группы в Периодической системе химических элементов Д. И. Менделеева, в которых расположен этот элемент;
3) определите, к металлам или неметаллам относится простое вещество, которое образует этот химический элемент.
2. Составьте электронную формулу атомов элементов: бром, ртуть.
3. Периодическая система химических элементов Д. И. Менделеева – богатое хранилище информации о химических элементах, их свойствах и свойствах их соединений, о закономерностях изменения этих свойств, о способах получения веществ, а также о нахождении их в природе. Так, например, известно, что с увеличением порядкового номера химического элемента в периодах радиусы атомов уменьшаются, а в группах увеличиваются.
Учитывая эти закономерности, расположите в порядке уменьшения радиуса атомов следующие элементы: азот, алюминий, углерод, кремний. Запишите обозначения элементов в нужной последовательности.
4. Проследите изменение электроотрицательности в следующем ряду элементов:
Li – C – Si – Na – Al – B - Li
5.

6. Определите тип химической связи в следующих веществах:
SiF4, CuBr2, Al4C3, OF2, Na3N, PI5, Au, Si
7. Вычислите массовую долю (%) серной кислоты в растворе, образующемся при смешении 120 г 20%-ного раствора серной кислоты с 40 г 50%-ного раствора бромоводородной кислоты (Запишите число с точность до целых.)
8. Вычислите массу 15% раствора (в граммах), при разбавлении которого можно получить 240 г 7%-го раствора. Ответ запишите с точностью до целых.
9. Составьте уравнение возможной диссоциации веществ:
Cl2O7, ZnI2, KClO3, HClO4, Cr(NO3)3, Al2(SO4)3, Hg(NO3)2
Контрольная работа за I полугодие
2 вариант
11л
1. На рисунке изображена модель электронного строения атома некоторого химического элемента.
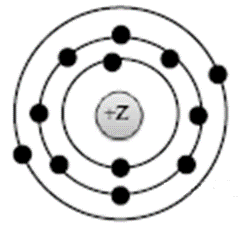
На основании анализа предложенной модели выполните следующие задания:
1) определите химический элемент, атом которого имеет такое электронное строение;
2) укажите номер периода и номер группы в Периодической системе химических элементов Д. И. Менделеева, в которых расположен этот элемент;
3) определите, к металлам или неметаллам относится простое вещество, которое образует этот химический элемент.
2. Составьте электронную формулу атомов элементов: селен, свинец.
3. Периодическая система химических элементов Д. И. Менделеева – богатое хранилище информации о химических элементах, их свойствах и свойствах их соединений. Так, например, известно, что с увеличением порядкового номера химического элемента радиусы атомов в периодах уменьшаются, а в группах увеличиваются.
Учитывая эти закономерности, расположите в порядке уменьшения радиусов атомов следующие элементы: алюминий, углерод, бор, кремний. В ответе запишите символы элементов в нужной последовательности.
4. Проследите изменение электроотрицательности в следующем ряду элементов:
Rb – Na – S – O – C – Sn – Sr
5.

6. Определите тип химической связи в следующих веществах:
P4, SnF4, AlH3, Hg, FeBr3, CCl4, Cl2O
7. Вычислите массу (в граммах) воды, которой нужно разбавить 10%-ный раствор соли массой 320 г, чтобы получить 8%-ный раствор. (Запишите число с точность до целых.)
8. Вычислите массу 5%-го раствора азотной кислоты, которую необходимо добавить к 40 г 20%-го раствора азотной кислоты, чтобы получить ее 7,5%-ный раствор. Ответ запишите в виде целого числа.
9. Составьте уравнение возможной диссоциации веществ:
FeCl3, N2O5, NH4NO3, HClO4, Ca(HCO3)2, Zn(OH)2, Cr2(SO4)3

























