Просмотр содержимого документа
«Методическая разработка лабораторной работы по химии по теме: "ПОЛУЧЕНИЕ СОЛЯНОЙ КИСЛОТЫ И ИЗУЧЕНИЕ ЕЕ СВОЙСТВ".»
ПРАКТИЧЕСКАЯ РАБОТА № 4
Тема: «ПОЛУЧЕНИЕ СОЛЯНОЙ КИСЛОТЫ И ИЗУЧЕНИЕ ЕЕ СВОЙСТВ»
Цель работы: Получить соляную кислоту. Изучить ее свойства, научиться отличать соляную кислоту и ее соли от других кислот и солей.
Оборудование: лабораторный штатив с лапкой, спиртовка, спички, пробирки, газоотводная трубка, вата.
Реактивы: NaCl (крист.), H2SO4 (конц.), AgNO3 (р-р), Mg, NaCl (р-р), CaCl2 (р-р), CuO (тв.), CuSO4(р-р), NaOH (р-р), СaCO3(тв.), вода, лакмус.
Ход работы:
1. Получение соляной кислоты
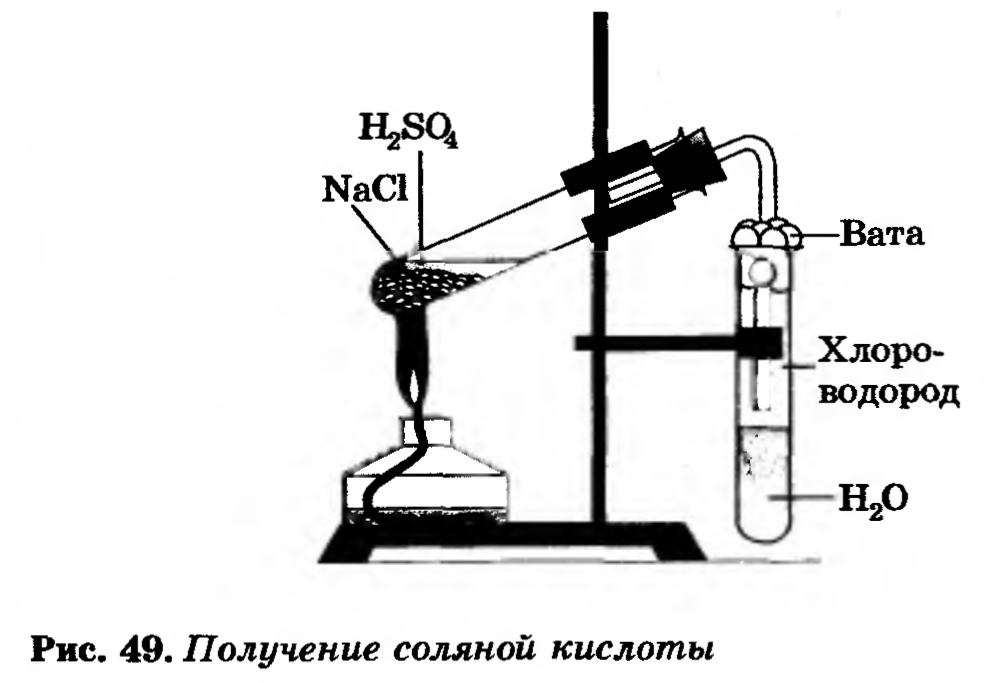
В пробирку насыпать немного поваренной соли и прилить концентрированную серную кислоту так, чтобы кислота смочила соль. Закрыть пробирку газоотводной трубкой.
Укрепить пробирку в лапке штатива (смотри рисунок).
Конец газоотводной трубки опустить в пробирку с водой так чтобы он был на расстоянии 0,5 – 1 см от поверхности воды.
Затем смесь соли и кислоты осторожно нагреть.
Внимание!
Следите за тем, чтобы газоотводная трубка не касалась воды!
Иначе воду перебросит в горячую пробирку-реактор и стекло лопнет
2. Исследование свойств соляной кислоты
1). Отношение кислоты к индикатору
В пробирку с раствором соляной кислоты HCl добавить лакмус
2). Взаимодействие с металлами
В пробирку с раствором соляной кислоты HCl добавить Mg
3). Взаимодействие с оксидами металлов
В пробирку с раствором соляной кислоты добавить горошину оксида меди CuO
Пробирку немного нагреть (не кипятить!).
4). Взаимодействие с основаниями
В пробирку со свежеосаденным гидроксидом меди (II) Cu(OH)2 1 – 2 мл раствора соляной кислоты (до растворения осадка)
5). Взаимодействие с солями
В пробирку с CaCO3 добавить раствор соляной кислоты HCl
3. Распознавание соляной кислоты и ее солей (качественная реакция на хлориды)
В пробирки с раствором соляной кислоты и хлорида натрия добавить несколько капель раствора нитрата серебра AgNO3 (качественная реакция на ион хлора Cl-)
Выполните отчет по работе
(Результаты исследования занести в таблицу)
| Название опыта | Наблюдения | Уравнение реакции (молекулярное, сокращенное ионное) | Вывод |
| 1. Получение соляной кислоты |
| | В лаборатории соляную кислоту можно получить при взаимодействии _______ и ________. |
| 2. Исследование свойств соляной кислоты 1). Отношение кислоты к индикатору |
|
|
При диссоциации соляной кислоты образуется ион _______(катион) и хлорид ион (________). |
| 2). Взаимодействие с магнием |
|
| Активные металлы вытесняют _______ из раствора соляной кислоты. |
| 3). Взаимодействие с оксидом меди (II) |
|
| Основный Оксид и кислота при взаимодействии образуют ________ и воду. |
| 4). Взаимодействие с гидроксидом меди (II) |
|
| При взаимодействии кислоты с основаниями образуется растворимая ________ и вода. |
| 5). Взаимодействие с карбонатом кальция |
|
| При взаимодействии соли и кислоты в одном сосуде – происходит__________. Реакция между солью и кислотой происходит тогда, когда может образоваться ________или выделиться___. |
| 3. Распознавание соляной кислоты и ее солей |
|
| Реактивом на хлорид ион является раствор ____________ . |
III. Вывод


















