ГАПОУ
«Оренбургский областной медицинский колледж»
Открытое занятие по дисциплине ОДП.010. ФИЗИКА
Преподаватель Кириллова С.Б.

Правила работы на занятии:
1. Работа с опорным конспектом.
2. Решение задач.
3. Самостоятельная работа.
4. Заполнение листа рефлексии.

Домашнее задание:
- Учебник Физика.11кл. Буховцев Б.Б., Мякишев Г.Я., Чаругин В.М. §§§78-79, 82-85.
- Задачи для самостоятельного решения к §85: №№1-5.
- СВР: 1.Реферативное сообщения по теме:
- «Проблемы ядерной энергетики. Защита
от радиации. Ядерная защита АЭС».
2. Решение задач по теме (опорный
конспект).

ВСПОМНИМ:
Из чего состоят все вещества?
Из чего состоят молекулы?
Что такое атом? Какая это частица?
С какими теориями строения атома вы познакомились при изучении курса физики в 9 классе ?
Так ли, в действительности, прост атом?
Как вы думаете, о чём пойдёт речь на сегодняшнем
занятии?

Быть может, эти электроны- Миры, где пять материков, Искусства, знанья, войны, троны И память сорока веков! Еще, быть может, каждый атом – Вселенная, где сто планет; Там все, что здесь, в объеме сжатом, Но также то, чего здесь нет.
В. Брюсов

Тема занятия: «Модели строения атомного ядра. Ядерные силы. Радиоактивность. Правила смещения. Закон радиоактивного распада».
Цель – доказать сложность строения
атомного ядра, используя научные данные
о строении атома,
изучить явление радиоактивности,
виды радиоактивных излучений,
закон радиоактивного распада.

План занятия:
- Модели строения атомного ядра.
- Ядерные силы.
- Физическая природа радиоактивности, виды излучений.
- Закон радиоактивного распада и его практическое применение.
- Примеры решения задач.

Слово «АТОМ» придумал более 2500 лет назад древнегреческий философ Демокрит
- В основе мира лежат два начала: АТОМЫ и пустота
- АТОМЫ- это мельчайшие неделимые частицы вещества, которые носятся в пустоте и отличаются друг от друга лишь формой, величиной и положением
- АТОМЫ численно бесконечны, вечны и неизменны

Открытия, связанные со сложным
строением вещества
В 1897 г. Уильямс Крукс открыл катодные лучи, представляющие собой поток электронов в вакуумной трубке. Английский физик Джозеф Томсон назвал частицы катодных лучей электронами.
У. Крукс
Дж. Томсон
1832-1919
1865-1940

Открытия, связанные со сложным
строением вещества

Открытия, связанные со сложным
строением вещества

Открытия, связанные со сложным
строением вещества

Модель атома Дж.Томсона
d

Модель атома Резерфорда
(планетарная модель)
d
ат
d
яд
В состав ядра атома любого химического элемента
входит атом водорода – ПРОТОН
1 1 р= 1 1 Н
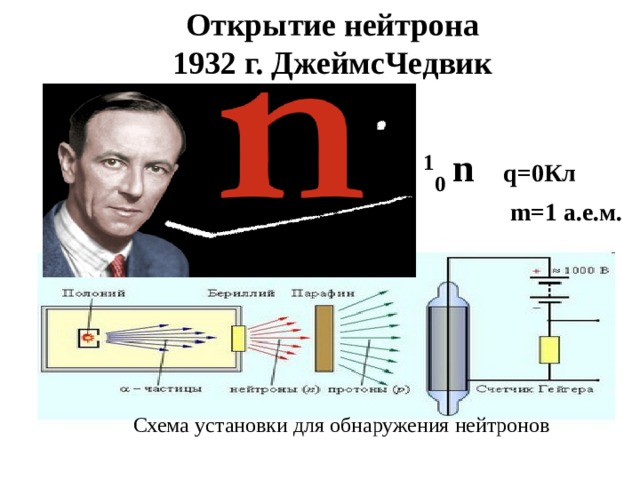
Открытие нейтрона
1932 г. ДжеймсЧедвик
1 0 n q=0Кл
m=1 а.е.м.
Схема установки для обнаружения нейтронов

Протонно-нейтронная модель
строения атомного ядра 1932 г.
Все ядра состоят из положительно заряженных
протонов и не имеющих заряда нейтронов
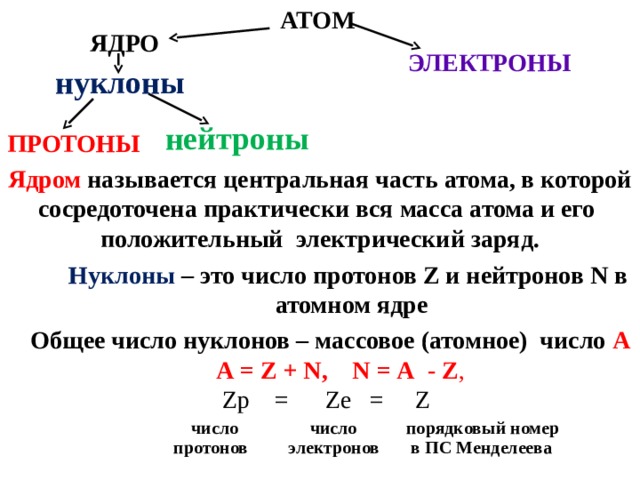
АТОМ
ЯДРО
ЭЛЕКТРОНЫ
нуклоны
нейтроны
ПРОТОНЫ
Ядром называется центральная часть атома, в которой
сосредоточена практически вся масса атома и его
положительный электрический заряд.
Нуклоны – это число протонов Z и нейтронов N в
атомном ядре
Общее число нуклонов – массовое (атомное) число А
А = Z + N, N = А - Z ,
Zp = Ze = Z
число число порядковый номер
протонов электронов в ПС Менделеева
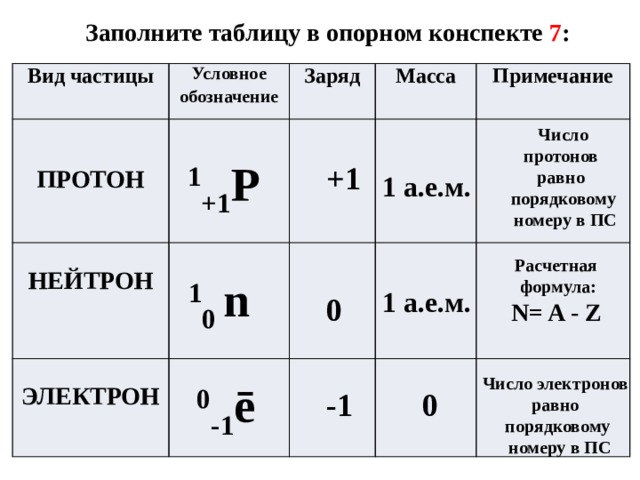
Заполните таблицу в опорном конспекте 7 :
Вид частицы
Условное обозначение
Заряд
Масса
ПРОТОН
НЕЙТРОН
Примечание
ЭЛЕКТРОН
Число протонов
равно
порядковому
номеру в ПС
1 +1 P
+1
1 а.е.м.
Расчетная
формула:
N= A - Z
1 0 n
1 а.е.м.
0
Число электронов
равно
порядковому
номеру в ПС
0 -1 ē
-1
0

Ядро химического элемента с порядковым номером Z
и массовым числом А обозначается:
А =234
Z = 92
234 92 U
Элемент
А=Z+ N
39 19 К
Zp
7
Ze
70 31 Ga
26 13 Al
N= А-Z
39
19
19
20
31
31
70
39
26
13
13
13
Заполните таблицу 8 в опорном
конспекте самостоятельно
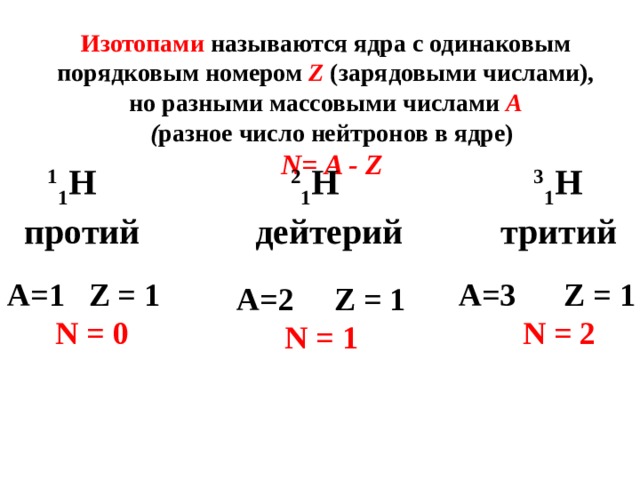
Изотопами называются ядра с одинаковым
порядковым номером Z (зарядовыми числами),
но разными массовыми числами A
( разное число нейтронов в ядре)
N= A - Z
1 1 Н 2 1 Н 3 1 Н
протий дейтерий тритий
А=1 Z = 1
А=3 Z = 1
N = 0
N = 2
А=2 Z = 1
N = 1
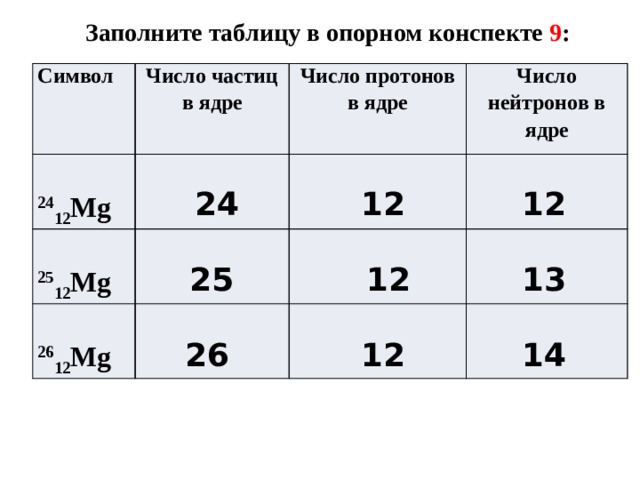
Заполните таблицу в опорном конспекте 9 :
Символ
Число частиц в ядре
Число протонов в ядре
24 12 Mg
25 12 Mg
Число нейтронов в ядре
26 12 Mg
12
24
12
25
12
13
26
12
14

ИЗОБАРАМИ называются ядра с одинаковым
массовым числом A ,
но разными зарядовыми числами Z
210 81 Tl 210 82 Pb 210 83 Bi
А=210 Z = 82
N = 128
А=210 Z = 83
N = 127
А=210 Z = 81
N = 129
Заполните таблицу 10 в опорном
конспекте самостоятельно
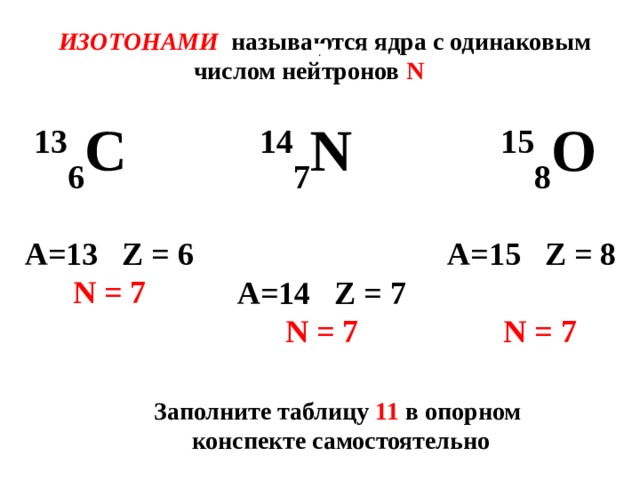
ИЗОТОНАМИ называются ядра с одинаковым
числом нейтронов N
.
13 6 С 14 7 N 15 8 O
А=13 Z = 6
А=15 Z = 8
N = 7
N = 7
А=14 Z = 7
N = 7
Заполните таблицу 11 в опорном
конспекте самостоятельно

ЭТО ИНТЕРЕСНО!
В настоящее время помимо протонно-нейтронной
модели строения атомного ядра существует еще
несколько моделей, самыми распространенными
являются:
Капельная модель
Основана на аналогии
между поведением молекул
в капле жидкости и нуклонов в ядре

Оболочечная модель
Нуклоны внутри ядра , как и электроны в атоме, заполняют энергетические уровни (оболочки), в каждой оболочке может находиться определенное число нуклонов.
Ядра с полностью заполненными оболочками называются магическими , они наиболее устойчивы к распаду, у них число Z или N равно одному из «магических» чисел:
2,8,20,28, 50, 82, 126
Ядра, у которых и Z и N одинаковые называются дважды «магическими» :
4 2 Не, 16 8 О , 40 20 Са,
48 20 Са, 208 82 Pb

ВНИМАНИЕ!!!
ПРОБЛЕМНАЯ СИТУАЦИЯ!!!!!
Почему нуклоны, имея одинаковые
положительные заряды, вопреки законам
электростатики, не отталкиваются друг от друга?

Силы , удерживающие нуклоны в ядре, называются ядерными
Свойства ядерных сил :
- самые сильные силы в природе;
- короткодействующие, заметны только на
расстояниях, сравнимыми с размерами атомного
ядра;
- не зависят от заряда, действуют одинаково между
р-р, р-n, n-n;
- являются только силами притяжения;
- обладают свойством насыщения;
- носят обменный характер: частицы в ядре обмени -
ваются виртуальными частицами – пионами:
π + , π - ,π 0 – мезонами;

Открытие радиоактивности –
одно из важнейших открытий
в ядерной физике

Антуан Анри Беккерель
(15 декабря 1852 -25 августа 1908) — французский физик, лауреат Нобелевской премии по физике и один из первооткрывателей радиоактивности
Явление радиоактивности
было открыто французским физиком Анри Беккерелем
1 марта 1896 года.

Опыт Анри Беккереля
Соли урана сами по себе без всякого внешнего воздействия испускают невидимые лучи, засвечивающие фотопластинку и проходящие через непрозрачные слои.
2 марта 1896г. Беккерель сообщил о своём открытии .

О ткрытие новых радиоактивных элементов
Лаборатория супругов Кюри


КАКОВА ПРИРОДА РАДИОАКТИВНОСТИ?
РАДИОАКТИВНОСТЬ - самопроизвольное превращение ядер одних химических элементов в ядра других химических элементов, сопровождаемое испусканием различных
частиц или ядер



Радиоактивные превращения атомных ядер
Правило смещения Содди:
сумма зарядов (массовых чисел) продуктов распада равна заряду (массовому числу) исходного ядра
А) α-распад - это распад при котором ядро испускает ядра атома гелия, при этом массовое число ядра уменьшается на 4 а.е.м., а заряд ядра уменьшается на 2е
Физический смысл распада : продукт распада смещается на 2 клетки к началу ПС Менделеева
A Z Х → A-4 Z-2 Y + 4 2 He
238 92 U → 238-4 92-2 Y + 4 2 He
238 92 U → 234 90 Th + 4 2 Hе

Радиоактивные превращения атомных ядер.
Правило смещения Содди:
сумма зарядов (массовых чисел) продуктов распада равна заряду (массовому числу) исходного ядра
Б) β -распад - это распад при котором ядро испускает быстрые электроны, при этом массовое число ядра не изменяется, а заряд ядра увеличивается на 1е
Физический смысл распада : продукт распада смещается на 1 клетку к концу ПС Менделеева
A Z Х → A Z+1 Y + 0 -1 e + 0 0 ὐ
ὐ - антинейтрино – нейтральная частица с очень малой массой , уносящая при β-распаде часть энергии

ВНИМАНИЕ!!!
ПРОБЛЕМНАЯ СИТУАЦИЯ!!!!!
Откуда в ядре берутся электроны , ведь, согласно протонно-нейтронной теории, атомные ядра
состоят из протонов и нейтронов?
Существует два вида β – распада: - β -электронный и + β -позитронный распад
Позитрон – это частица, заряд которой равен модулю заряда электрона, а масса равна массе электрона

При - β –электронном распаде нейтрон превращается в протон с испусканием
электрона и антинейтрино :
1 0 n → 1 1 p + 0 -1 e+ 0 0 V
При позитронном + β – распаде протон превращается в нейтрон, из ядра выделяется позитрон и нейтрино :
1 1 р → 1 0 n + 0 +1 e+ 0 0 υ
(нейтрино – маленький нейтрончик)
Правило смещения для позитронного + β – распада имеет вид:
A Z Х β → A Z-1 Y + 0 +1 e + 0 0 υ (υ –нейтрино )
Физический смысл распада: продукт распада смещает
ся на 1 клетку к началу ПС Менделеева

Существует третий вид превращения ядер с участием β-частиц:
К-захват : ядро поглощает один из электронов атома,
в результате чего протон
превращается в нейтрон, при этом испускается нейтрино,
Физический смысл распада: продукт распада смещает
ся на 1 клетку к началу ПС Менделеева:
A Z Х + 0 -1 e → A Z-1 Y + 0 0 υ
Примером такого распада является превращение
калия в аргон: (запишите самостоятельно)
19 40 К + 0 -1 e → 18 40 Ar + 0 0 υ (υ - нейтрино)

Радиоактивные превращения атомных ядер
γ – излучение сопровождает радиоактивный распад в том случае, если вновь образованное ядро находится в возбужденном состоянии.
Правило смещения для γ – излучения имеет вид:
A Z Х → A Z Y + 0 0 γ
Например: 238 92 U → 238 92 U + 0 0 γ

РЕШИТЕ ЗАДАЧИ :
Задача 1: Изотоп тория 230 90 Th испускает α-частицу.
Какой элемент при этом образуется?
230 90 Th → 226 88 Ra + 4 2 He
Задача 2: Изотоп тория 230 90 Th β-радиоактивен. Какой элемент образуется при распаде ядра?
230 90 Th β → 230 91 Рa + 0 -1 e
Задача 3: В какой элемент превращения уран 239 92 U после двух
β – распадов и одного α –распада?
239 92 U β → 239 93 Np β → 239 94 Pu α → 235 92 U
Задача 4: Написать цепочку ядерных превращений неона 20 10 Ne :
β, β, β, α, α, β, α, α
20 10 Ne β → 20 11 Na β → 20 12 Mg β → 20 13 Al α → 16 11 Na α → 12 9 F β
12 9 F β → 12 10 Ne α → 8 8 O α → 4 6 C

ВНИМАНИЕ!!!!
Можно ли получить золото (Au) из ртути (Hg) физическим и химическим путем? Как?

Закон радиоактивного распада:
За единицу времени всегда распадается одна и та же часть имеющихся в наличии ядер радиоактивного элемента

или: активность радиоактивных веществ убывает с течением времени:
А=
В медицине используется внесистемная единица измерения радиоактивности Кюри (Ки) – измеряющая активность
1 г чистого радия
1Ки=3,7*10 10 Бк
Для каждого вещества существует характеристика - период полураспада Т - это время , в течение которого распадается половина наличного числа радиоактивных атомов. Чем меньше период полураспада, тем быстрее протекает распад

Изотоп
Период полураспада
238 U
239 Pu
4,5 млрд. лет
14 C
24000 лет
226 Ra
5730 лет
3 H
1600 лет
12 лет
104 Tc
18 минут

Применение закона радиоактивного распада :
2) в геологии;
3) в палеонтологии;
4) в биологии

Пример решения задачи: (см. 26/1 в ОП)
Имелось некоторое количество радиоактивного серебра. Масса серебра уменьшилась в 8 раз за 810 суток. Определите период полураспада.
Решение:
m = m 0 / 2 t/T
m 0 /m =2 t/T
8 = 2 t/T
2 3 = 2 t/T
3= t/T
T=810/3=270 (cут.)
Дано:
t=810 cут.
m 0 /m=8
T-?
Ответ: 270 суток.

Решите задачу: (см. 26/2 в ОП)
Период полураспада радия 1600 лет. Через какое время число атомов уменьшится в 8 раз?
N = N 0 / 2 t/T
N 0 /N =2 t/T
8 = 2 t/T
2 3 = 2 t/T
3= t/1600
t=1600 *3=4800 (лет)
Дано:
Решение:
Т=1600 лет
N 0 /N= 8
t - ?
Ответ : 4800 лет

Закрепление:
- В чем заключается теория протонно-нейтронного
строения атомного ядра?
- Перечислите виды радиоактивных излучений.
- Какое из излучений( α, β или γ) обладает наибольшей
проникающей способностью?
- Какое явление называют радиоактивностью?
- Сформулируйте закон радиоактивного распада.
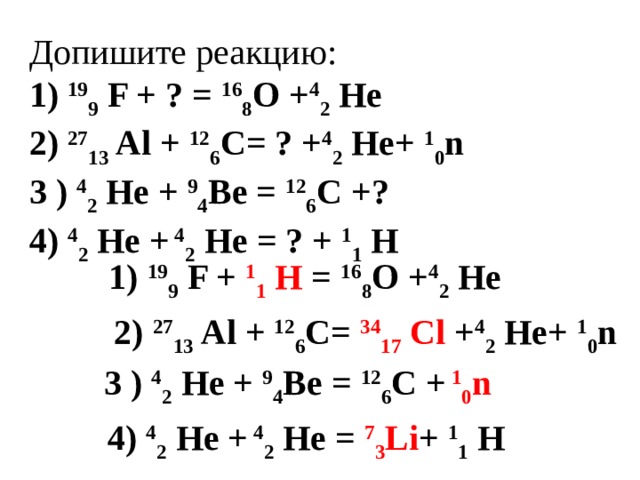
Допишите реакцию:
1) 19 9 F + ? = 16 8 О + 4 2 Нe
2) 27 13 Al + 12 6 C= ? + 4 2 Нe+ 1 0 n
3 ) 4 2 He + 9 4 Bе = 12 6 C +?
4) 4 2 He + 4 2 He = ? + 1 1 H
1) 19 9 F + 1 1 H = 16 8 О + 4 2 Нe
2) 27 13 Al + 12 6 C= 34 17 Cl + 4 2 Нe+ 1 0 n
3 ) 4 2 He + 9 4 Bе = 12 6 C + 1 0 n
4) 4 2 He + 4 2 He = 7 3 Li + 1 1 H

Самостоятельная
работа

Критерии оценивания:
6-7 правильных ответов – оценка 3 (удовлетворительно);
8-9 правильных ответов – оценка 4 (хорошо);
10 правильных ответов – оценка 5 (отлично)
Номер задания
Вариант ответа
1 вариант
1
Б
2
2 вариант
В
Г
3
В
А
4
А
А
5
Б
6
Б
Г
А
7
Г
А
8
Г
А
9
Г
В
10
Г
А
В

Биологическое действие радиационных излучений

Радиация существует на Земле около 20 миллиардов лет, т.е. с момента зарождения жизни на планете

Механизмы попадания радиационных
излучений
в организм человека:
- внутреннее облучение при вдыхании радиоактивных аэрозолей, продуктов деления (ингаляционная опасность);
- внутреннее облучение в результате потребления загрязненных продуктов питания и воды;
- контактное облучение при попадании радиоактивных веществ на кожные покровы и одежду
Применение ядерной энергии. Биологическое действие радиоактивного излучения

Заболевания, вызванные облучением:

Заболевания, вызванные облучением:
Генетические мутации

Заболевания, вызванные облучением:
Раковые заболевания

Заболевания, вызванные облучением:
Иммунные мутации

Применение радиоактивных излучений
в медицине
Вскоре после открытия радиация нашла применение в медицине. Но массовое применение радиационная диагностика приобрела спустя полвека

Рентгенологические исследования

Компьютерная томография
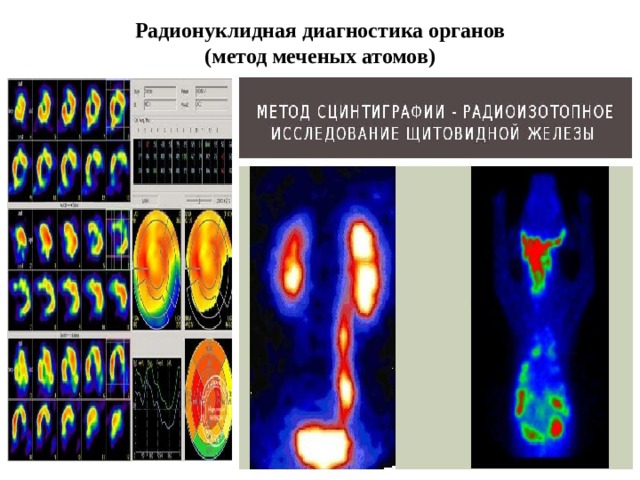
Радионуклидная диагностика органов
(метод меченых атомов)

Гамма-терапия

Протонно-нейтронная терапия

Радоновая терапия

Спасибо за
внимание!