| Алгоритм определения типа химической связи в соединениях
1. Определить, какие атомы химических элементов образуют данное соединение. Ме + неМе = ионная неМе + неМе = ковалентная а) если атомы одинаковые = ковалентная неполярная. б) если атомы разные = ковалентная полярная. Химическая связь в куске металла – металлическая.
Чем ближе друг к другу стоят атомы химических элементов, тем меньше полярность связи, которая образуется между ними.
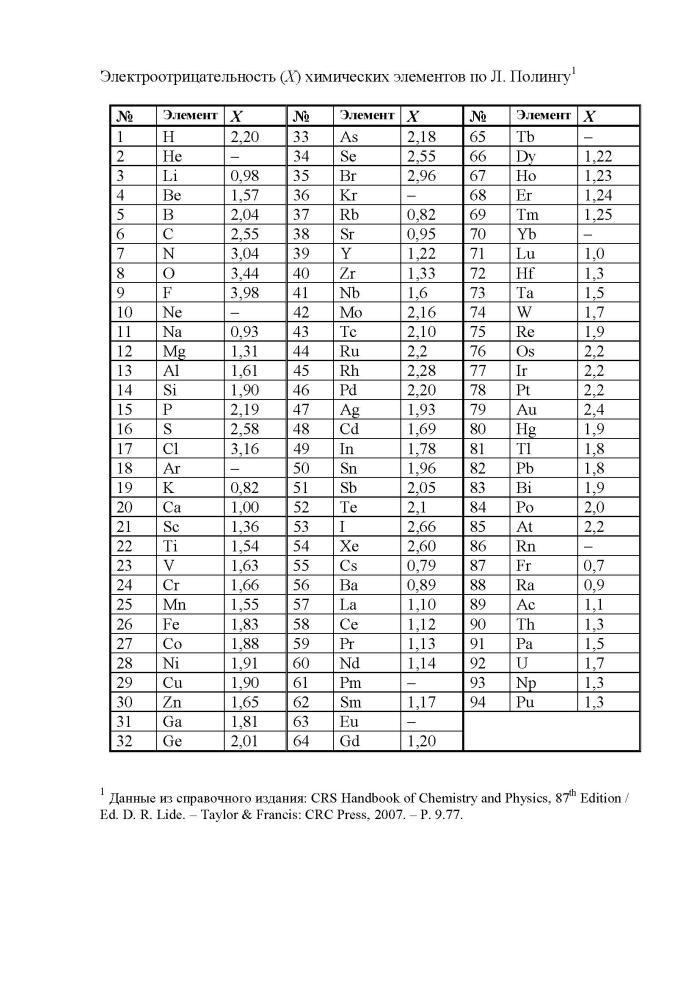
2.Определить тип химической связи можно, рассчитав разницу в электроотрицательности связанных атомов, используя таблицу Полинга (см. ниже). Например, NaCl |0,93-3,16|=2,23 – ионная. Величина берётся по модулю. ΔХ = 0 ковалентная неполярная ΔХ 0 ковалентная полярная ΔХ ≥ 1,9 ионная
| Алгоритм определения типа химической связи в соединениях
1. Определить, какие атомы химических элементов образуют данное соединение. Ме + неМе = ионная неМе + неМе = ковалентная а) если атомы одинаковые = ковалентная неполярная. б) если атомы разные = ковалентная полярная. Химическая связь в куске металла – металлическая.
Чем ближе друг к другу стоят атомы химических элементов, тем меньше полярность связи, которая образуется между ними.
2.Определить тип химической связи можно, рассчитав разницу в электроотрицательности связанных атомов, используя таблицу Полинга (см. ниже). Например, NaCl |0,93-3,16|=2,23 – ионная. Величина берётся по модулю. ΔХ = 0 ковалентная неполярная ΔХ 0 ковалентная полярная ΔХ ≥ 1,9 ионная
|
| Алгоритм определения типа химической связи в соединениях
1. Определить, какие атомы химических элементов образуют данное соединение. Ме + неМе = ионная неМе + неМе = ковалентная а) если атомы одинаковые = ковалентная неполярная. б) если атомы разные = ковалентная полярная. Химическая связь в куске металла – металлическая.
Чем ближе друг к другу стоят атомы химических элементов, тем меньше полярность связи, которая образуется между ними.
2.Определить тип химической связи можно, рассчитав разницу в электроотрицательности связанных атомов, используя таблицу Полинга (см. ниже). Например, NaCl |0,93-3,16|=2,23 – ионная. Величина берётся по модулю. ΔХ = 0 ковалентная неполярная ΔХ 0 ковалентная полярная ΔХ ≥ 1,9 ионная
| Алгоритм определения типа химической связи в соединениях
1. Определить, какие атомы химических элементов образуют данное соединение. Ме + неМе = ионная неМе + неМе = ковалентная а) если атомы одинаковые = ковалентная неполярная. б) если атомы разные = ковалентная полярная. Химическая связь в куске металла – металлическая.
Чем ближе друг к другу стоят атомы химических элементов, тем меньше полярность связи, которая образуется между ними.
2.Определить тип химической связи можно, рассчитав разницу в электроотрицательности связанных атомов, используя таблицу Полинга (см. ниже). Например, NaCl |0,93-3,16|=2,23 – ионная. Величина берётся по модулю. ΔХ = 0 ковалентная неполярная ΔХ 0 ковалентная полярная ΔХ ≥ 1,9 ионная
|