9 класс Урок № 48 Тема урока: Опыты Резерфорда. Планетарная модель атома.
Цель урока: изучить строение атома; рассмотреть фундаментальный опыт Резерфорда.
Задачи: Образовательные: Изучить планетарную модель атома. Познакомить учащихся с гипотезой Томсона и фундаментальным опытом Резерфорда. Изучить строение атома.
Планируемые результаты:
Развивающая: Коррекция мышления на основе анализа и синтеза.
Воспитательные: Показать значение опытных фактов. Продолжить формирование познавательного интереса учащихся.
предметные: - познакомить учащихся с гипотезой Томсона и фундаментальным опытом Резерфорда;
метапредметные: - продолжить формирование: умения анализировать, обобщать, составлять конспекты, выделять главные мысли; умения работать в группе; способствовать развитию речи, мышления учащихся;
личностные: - создать личностную ситуацию успеха, вести коллективный поиск по сбору материала о истории открытия сложности строения атома, создать условия для развития у школьников умения структурировать информацию; способствовать формированию интереса к предмету, воспитанию коммуникативных качеств учащихся.
Тип урока: урок изучения нового материала.
Оборудование: компьютер, проектор, графические задания, портреты ученых, модели атомов Томсона и Резерфорда, наглядные пособия.
Ход урока.
1.Оргмомент, постановка цели урока.
2. Актуализация знаний.
- Какие заряды существуют в природе?
- Каким образом они взаимодействуют друг с другом?
-Физика –это наука о чем?
-Что мы знаем о природе?
-Какие физические явления вы знаете?
- Какие явления изучаем сейчас ? Какие заряды мы знаем?
-Какие электрические приборы мы изучили?
-Качественный вопрос по теме электризация
-Как надо зарядить тело ,чтоб рисунок В соответствовал правильному ответу. Почему? -Изменим ситуацию на интерактивной доске. Как теперь зарядить надо тело? рисунок С. Почему ?
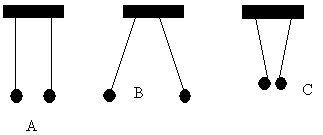
-Посредством чего происходит взаимодействие зарядов?
-Мы можем электрическое поле увидеть ,пощупать?
-Какие вещества называются проводниками? Непроводниками?
2. Изучение нового материала.
1896г. -Дж.Дж.Томсон - выдающийся ученый, директор знаменитой Кавендишской лаборатории, лауреат Нобелевской премии, открыл электрон.
Первая достаточно разработанная модель атома была предложена английским физиком Дж. Дж. Томсоном, открывшим электрон. Согласно этой модели вещество в атоме несет положительный заряд и равномерно заполняет весь объем атома. Электроны “вкраплены” в атом. Первая модель атома сыграла положительную роль. Но она требовала доказательств.

1911г. - Э. Резерфорд ставит опыт по рассеянию альфа-частиц. Пучок aльфа-частиц пропускался через тонкую золотую фольгу. Золото было выбрано как очень пластичный материал, из которого можно получить фольгу толщиной практически в один атомный слой. Чтобы проверить гипотезу Дж. Дж. Томсона необходимо провести эксперимент, что и сделал Э. Резерфорд. Он решил проникнуть внутрь атома с помощью α-частиц, которые имели положительный заряд, массу почти в 7300 раз большую чем масса электрона и очень большую скорость (около 20000км/c). С точки зрения Резерфорда α-частицы должны были легко "пробить" атом и тем самым доказать справедливость модели атома Томсона.
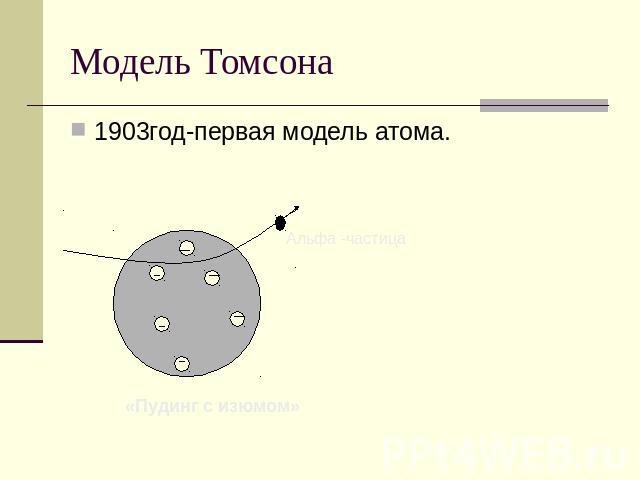

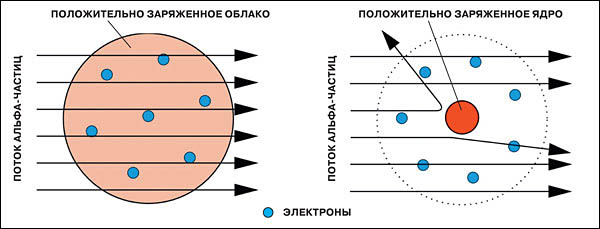
Если бы атом был устроен так, как предполагал Дж.Томсон, то Э.Резерфорд увидел бы следующую картину: α- частицы пробивают атом и практически не отклоняясь пролетают сквозь него.
Схему экспериментальной установки Резерфорда вы видите на рисунке.
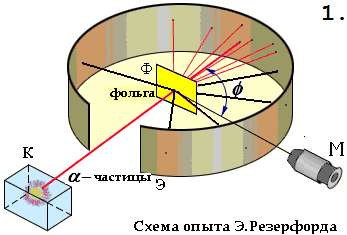
В цилиндрическом сосуде с небольшим отверстием находился радиоактивный препарат, испускавший поток α-частиц. Они попадали на золотую фольгу и, проходя через нее, ударялись о люминесцирующий экран. В местах удара частиц на экране возникали вспышки света.
То, что некоторые α-частицы отскакивали от фольги назад, противоречило модели Томсона. Результаты эксперимента настолько удивили Резерфорда, что он воскликнул: "... неправдоподобно так же, как если бы вы выстрелили пятнадцатифунтовым снарядом в папиросную бумагу, а снаряд отскочил бы обратно и убил бы вас самих".
Приблизительные размеры ядра: около 10-14 м. Это число оказалось примерно в 10 000-100 000 раз меньше размеров самого атома. Поэтому свободное пространство в модели атома Резерфорд "заполнил" электронами Он, в частности, говорил, что атом "состоит из центрального электрического заряда, сосредоточенного в точке и окруженного однородным сферическим распределением противоположного электричества равной величины".
Итак, Резерфорд предложил планетарную модель атома. Согласно этой модели, в центре атома располагается положительно заряженное ядро, в котором сосредоточена почти вся масса атома. Атом в целом нейтрален. Вокруг ядра, подобно планетам, вращаются под действием кулоновских сил со стороны ядра электроны. Находиться в состоянии покоя электроны не могут, так как они упали бы на ядро.
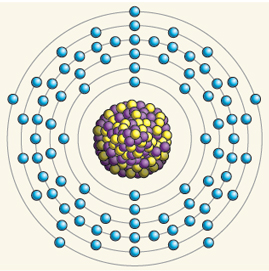
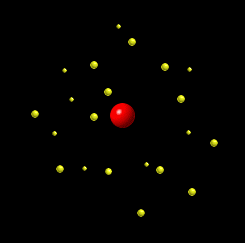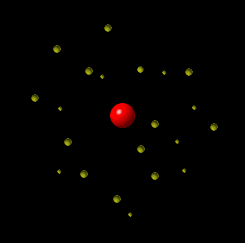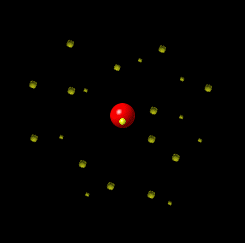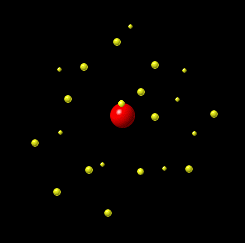
Опыт показал, что положительный заряд атома сконцентрирован в очень малом объеме - ядре, а между ядрами атомов существуют большие промежутки.
Резерфорд показал, что модель Томсона находится в противоречии с его опытами.
Резерфорд шел к своему открытию строения атома в течение 5 лет. Долгих пять лет проводил он опыты по исследованию строения атома.
Размеры. Атом: 10-10 м; ядро: 10-10 – 10-14 м. Практически вся масса атома сосредоточена в ядре- 99,95 %. Из опытов следует, что ядро и отталкивает альфа-частицу, причем тем сильнее, чем ближе к ядру она проходит. По соотношению между общим числом частиц и числом отклонившихся на определенные углы частиц рассчитывается размер ядра и заряд ядра. Оказалось, что радиус ядра имеет порядок 10 - 12 см (10 - 14 м). Заряд же ядра положителен и определяется формулой q = Z•e, где Z - порядковый номер элемента в периодической системе, а е - модуль заряда электрона”.
Строение всех атомов зашифровано в периодической системе химических элементов. Порядковый номер химического элемента показывает электрический заряд ядра атома Z , этот заряд численно равен сумме протонов в ядре атома; т.к. атом в целом электрически нейтральная частица, то суммарный положительный заряд атома равен суммарному отрицательному заряду, следовательно, равен числу электронов в оболочке атома. Чтобы вычислить число нейтронов в ядре из массового числа атома вычитаем заряд ядра: N=A-Z
Физминутка. Зарядка для глаз
3.Закрепление материала.
- С какой целью проводился опыт Резерфорда?
- Пользуясь рисунком расскажите, как проводился опыт Резерфорда по рассеянию α- частиц?
- Какие результаты были получены в ходе опыта?
- Каковы вывода Резерфорда?
- Что представляет атом согласно ядерной модели, выдвинутой Резерфордом?
- Каковы размеры атома и ядра?
- По рисунку расскажите, как проходят α- частицы сквозь атомы вещества? Почему?
4. Выполнение тестовой работы https://multiurok.ru/tests/opyty-rezerforda-planetarnaia-model-atoma.html
5. Подведение итогов. Рефлексия.
6. Домашнее задание: §21



































