
11/10/18
Алкены
ХИМИЯ - 10
Автор: Кунова Г.В. - учитель химии ГОАОУ «ЦОРиО»
г. Липецк

11/10/18
- К непредельным относят углеводороды, содержащие в молекулах кратные связи между атомами углерода .
- Свойство «непредельности» связано со способностью этих веществ вступать в реакции присоединения , прежде всего водорода, с образованием предельных, или насыщенных, углеводородов – алканов.
- Какую пользу получит аудитория от презентации: взрослых учащихся больше интересует предмет, если они знают, почему и насколько он важен для них.
- Уровень знаний докладчика по теме: кратко укажите свои профессиональные успехи в этой области или объясните, почему участникам интересно будет вас послушать.
- По названию первого представителя гомологического ряда – этилена – алкены называют этиленовыми углеводородами.

11/10/18
- Орбитали атомов углерода, между которыми имеется двойная связь, находятся в состоянии sp 2 -гибридизации.
- Это означает, что в гибридизации участвуют одна s- и две p-орбитали , а одна p-орбиталь остаётся негибридизованной.
- Перекрывание гибридных орбиталей приводит к образованию σ-связи , а за счёт негибридизованных p-орбиталей соседних атомов углерода образуется вторая, π-связь.
Вывод: двойная связь состоит из одной σ- и одной π-связи.

11/10/18
- Оси гибридных орбиталей атомов, образующих двойную связь, находятся в одной плоскости, а орбитали, образующие π-связь , располагаются перпендикулярно плоскости молекулы.
- Двойная связь (0,132 нм) короче одинарной, а её энергия больше, т. е. она является более прочной. Тем не менее наличие подвижной, легко поляризуемой π-связи приводит к тому, что алкены химически более активны, чем алканы, и способны вступать в реакции присоединения.

11/10/18

11/10/18
1) изомерия углеродного скелета:
2) изомерия положения двойной связи:
11/10/18
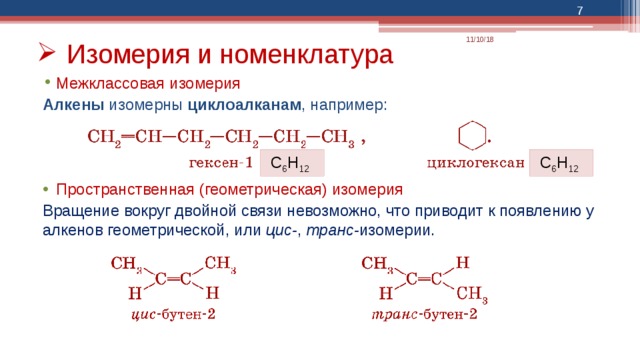
Алкены изомерны циклоалканам , например:
- Пространственная (геометрическая) изомерия
Вращение вокруг двойной связи невозможно, что приводит к появлению у алкенов геометрической, или цис- , транс- изомерии.
С 6 Н 12
С 6 Н 12

11/10/18
Номенклатура алкенов, разработанная ИЮПАК, схожа с номенклатурой алканов.
1. Определения главной цепи – самой длинной цепочки атомов углерода в молекуле. Главная цепь должна содержать двойную связь.
2. Нумерация атомов главной цепи начинается с того конца, к которому ближе находится двойная связь.
Если по расположению двойной связи нельзя определить начало нумерации атомов в цепи, то его определяет положение заместителей так же, как для предельных углеводородов.
3. Формирование названия. В конце названия указывают номер атома углерода, у которого начинается двойная связь, и суффикс, обозначающий принадлежность соединения к классу алкенов, -ен.
5-метилгексен-2

11/10/18
Получение алкенов
Рассмотрим основные способы получения алкенов
- в промышленности
- в лаборатории

11/10/18
- Получение – в промышленности
В процессе термического крекинга предельных углеводородов наряду с образованием алканов происходит образование алкенов, например:
- Дегидрирование предельных углеводородов.
При пропускании алканов над катализатором (Pt, Ni, Cr2O3) при высокой температуре (400—600 °С) происходит отщепление молекулы водорода и образование алкена.
11/10/18
- Получение – в лаборатории
- Дегидратация спиртов (отщепление воды).
Воздействие водоотнимающих средств (H 2 SO 4 , Al 2 O 3 ) на одноатомные спирты при высокой температуре приводит к отщеплению молекулы воды и образованию двойной связи:

11/10/18
- Получение – в лаборатории
- Дегидрогалогенирование (отщепление галогеноводорода).
При взаимодействии галогеналкана с щёлочью в спиртовом растворе образуется двойная связь в результате отщепления молекулы галогеноводорода:
Реакция идёт по правилу Зайцева:

11/10/18
- Получение – в лаборатории
При действии цинка или магния на дибромпроизводное алкана происходит отщепление атомов галогенов, находящихся при соседних атомах углерода, и образование двойной связи:

11/10/18
Химические свойства алкенов
- Реакции присоединения
- Реакции полимеризации
- Реакции окисления

11/10/18
Отличительной чертой представителей непредельных углеводородов - алкенов является способность вступать в реакции присоединения.
Алкены способны присоединять водород в присутствии катализаторов гидрирования — металлов — платины, палладия, никеля:

11/10/18
- Галогенирование (присоединение галогенов).
Взаимодействие алкена с бромной водой или раствором брома в органическом растворителе (CCl 4 ) приводит к быстрому обесцвечиванию этих растворов в результате присоединения молекулы галогена к алкену и образования дигалогеналканов:
- Признак реакции – обесцвечивание бромной воды.
Качественна реакция на кратную
углерод-углеродную связь С=С

11/10/18
- Гидрогалогенирование (присоединение галогеноводорода):
Эта реакция подчиняется правилу Марковникова:
?

11/10/18
- Гидратация (присоединение воды).
Гидратация алкенов приводит к образованию спиртов.
При присоединении воды к этену образуется первичный спирт –
этиловый спирт:
При гидратации пропена или других алкенов образуются вторичные или третичные спирты:

11/10/18
- Реакция полимеризации – особый случай реакции присоединения:
Реакции полимеризации веществ, содержащих двойную связь, используют для получения различных высокомолекулярных соединений:

11/10/18
- Алкены горят в кислороде с образованием CO 2 и H 2 O:
- Алкены легко окисляются под действием водного раствора перманганата калия до двухатомных спиртов:
Качественна реакция на кратную углерод-углеродную связь С=С

11/10/18
- Алкены широко используются в химической промышленности как сырьё для получения разнообразных органических веществ и материалов.
- Этен - исходное вещество для производства этанола, этиленгликоля, эпоксидов, дихлорэтана.
Большое количество этена перерабатывается в полиэтилен , который используется для изготовления упаковочной плёнки, посуды, труб, электроизоляционных материалов.
- Из пропена получают глицерин, ацетон, изопропиловый спирт, растворители.
Полимеризацией пропена получают полипропилен, который по многим показателям превосходит полиэтилен: имеет более высокую температуру плавления, химическую устойчивость.
В настоящее время из полимеров - аналогов полиэтилена производят волокна, обладающие уникальными свойствами. Так, например, волокно из полипропилена - одно из самых прочных синтетических волокон.
Материалы, изготовленные из этих волокон, являются перспективными и находят всё большее применение в разных областях человеческой деятельности.

11/10/18







































