
СПИРТЫ

СПИРТЫ
C x H y (OH) n
Спиртами называются органические вещест-ва, молекулы которых содержат одну или несколько гидроксильных групп, связанных с углеводородным радикалом.
ОН- функциональная группа – это группа атомов, характерная для данного класса соединений, обуславливающая физические и химические свойства веществ этого класса.
- Спиртами называются органические вещест-ва, молекулы которых содержат одну или несколько гидроксильных групп, связанных с углеводородным радикалом. ОН- функциональная группа – это группа атомов, характерная для данного класса соединений, обуславливающая физические и химические свойства веществ этого класса.

Классификация спиртов
1
3
2
По характеру атома углерода, с которым связанна гидроксильная группа
По количеству гидроксильных групп
По характеру углеродного радикала

Классификация спиртов
По характеру углеродного радикала
Title
Add your text
СПИРТЫ
СН 2 -ОН
CH 3 -CH 2 -CH 2 -OH
Предельные
С 6 Н 5 - CH 2 -OH
Ароматические
CH 2 = CH - CH 2 - OH
Непредельные

R ( OH ) x
Алканолы
Алкенолы
Фенолы
Алкинолы
Циклоалконолы
По характеру углеводородного радикала, с которым связана гидроксильная группа классификация спиртов совпадает с классификацией углеводородов.

Классификация спиртов
по количеству гидроксильных групп
Title
Add your text
СПИРТЫ
CH 2 - CH-CH 2 -OH
I I I
OH OH OH
Трехатомные
(Глицерин)
CH 3 -CH 2 -CH 2
I
OH
Одноатомные
(Этиловый спирт)
CH 2 - CH-CH 2 -OH
I I
OH OH
Двухатомные
(Этиленгликоль)

Классификация спиртов
по характеру атома с которым связана гидроксильная группа
Title
Add your text
СПИРТЫ
CH 3
I
CH 3 -C- С H 3
I
OH
Третичные
(2-метилпропанол-2)
CH 3 -CH 2 -CH 2
I
OH
Первичные
(бутанол - 1)
CH 3 - CH 2 -CH-OH 3
I
OH
Вторичные
(бутанол - 2)

Гомологический ряд
CH 3 - OH - метан ол
Метиловый спирт
Этиловый спирт
C 2 H 5 - OH - этан ол
Пропиловый спирт
СН 3 -СН 2 -СН 2 -ОН - пропан ол
Бутиловый спирт
СН 3 -СН 2 -СН 2 -СН 2 -ОН - б утан ол
Алканолы образуют гомологический ряд общей формулы C n H 2n+1 OH ( n= 1,2,3,: N) . Названия алканолов по систематичес-кой номенклатуре строятся из названий соответствующих ал- канов путём добавления суффикса «ол»

CH3 - OH - метанол
C2H5 - OH - этанол

Изомерия спиртов
Для алканолов характерны три вида изомерии:
изомерия положения гидроксильной
группы в углеродной цепи
Алканы
изомерия углеродного скелета.
А также межклассовая изомерия с простыми эфирами

Изомерия положения гидроксильной группы в углеродной цепи
CH 3 -CH 2 -CH 2 -OH пропанол
н -пропиловый спирт
CH 3 -CH-CH
l
OH
пропанол-2
(изопропиловый спирт)

Изомерия углеродного скелета
CH 3 -CH 2 -CH 2 -CH 2 -OH бутанол-1 ( н -бутиловый спирт)
CH 3 -CH-CH 2 -OH
l
CH 3
2- метилпропанол-1
(изобутиловый спирт)
Первым из спиртов, для которого характерны оба вида изомерии, является бутанол

Физические свойства спиртов
Алканолы являются бесцветными жидкостями или кристаллическими веществами с характерным запахом. Первые члены гомологического ряда имеют приятный запах, для бутанолов и пентанолов запах становится неприятным и раздражающим. Высшие алканолы имеют приятный ароматный запах.

Температура кипения
Температура кипения спиртов
Название спирта
Температура кипения
Формула
64,7
Метиловый (метанол)
СН 3 ОН
С 2 Н 5 ОН
78,3
Этиловый(этанол)
97,2
Пропиловый (пропанол)
С 3 Н 7 ОН
117,7
Бутиловый (бутанол-1)
С 4 Н 9 ОН
С 5 Н 11 ОН
Амиловый (пентанол-1)
137,8

Высокая температура кипения спиртов объясняется значительным межмолекулярным взаимодействием – ассоциацией молекул, возможность которой объясняется полярностью связи О–Н и неподелёнными электронными парами атомов кислорода. Такое взаимодействие называют водородной связью

Химические свойства спиртов
Реакции окисления
Реакция замещения атомов водорода группы ОН
Реакция дегидратации (отщепления молекулы воды)
Реакция замещения атомов водорода ОН группы
Для алканолов характерно 4 типа реакций:

Реакция замещения водорода -ОН группы
С 2 Н 5 ОН + Na → C 2 H 5 ONa + H 2
C 2 H 5 ONa + H 2 O → C 2 H 5 OH + NaOH
Как слабые кислоты алканолы могут реагировать со щелочными металлами. Образующиеся при этом металлические производные спиртов называются алкоголятами .

Реакция замещения –ОН группы
Наибольшее практическое значение из реакций второго типа имеют реакции замещения гидроксильной группы на галогены. Данная реакция может осуществляться при действии на алканолы различных галогеноводородных кислот

Реакция дегидратации
Для алканолов характерно два типа реакции дегидратации:
- внутримолекулярная
и
- межмолекулярная
При внутримолекулярной дегидратации обра- зуются алкены, при межмолекулярной - простые эфиры.

Внутримолекулярная дегидратация алканолов может осуществляться при нагревании их с избытком концентрированной H 2 SO 4 при темпе- ратуре 150-200 º С или при пропускании спиртов над нагретыми твёрдыми катализаторами.

При более слабом нагревании этилового спирта с серной кислотой образуется диэтиловый эфир. Это летучая, легко воспламеняющаяся жидкость. Диэтиловый эфир относится к классу простых эфиров – органических веществ, молекулы которых состоят из двух углеводородных радикалов, соединённых посредством атома кислорода. Общая формула R – O - R

Реакции окисления
Кислородсодержащие органические вещества, как и углеводороды, горят на воздухе или в кислороде с образованием паров воды и углекислого газа. Горение спиртов – сильно экзотермическая реакция, поэтому они могут быть использованы в качестве высококалорийного топлива.
C n H 2n+1 OH+O 2 nCO 2 +(n+1)H 2 O+ Q

Окисление первичных спиртов до карбоновых кислот протекает при действии HNO 3 или перманганата калия в щелочной среде.
Окисление вторичных спиртов приводит к образованию соответствующих кетонов.
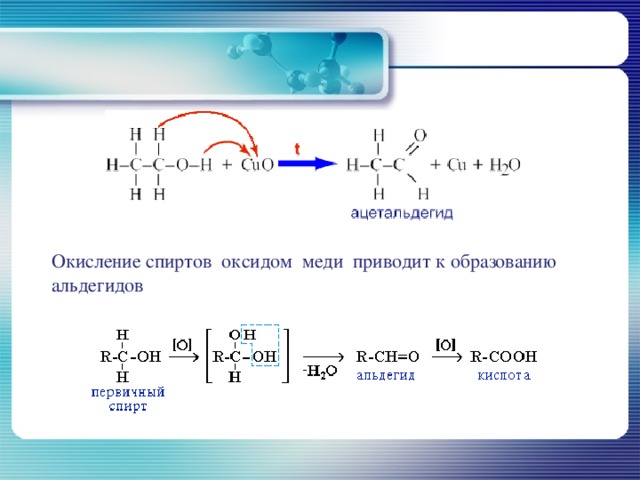
Окисление спиртов оксидом меди приводит к образованию альдегидов

Способы получения
Получение из алкенов
22

Способы получения
Получение из галогенпроизводных
22

Способы получения
Получение из оксосоединений
22

Метанол и этанол
Метанол получают гидрированием оксида углерода ( II ) СО. В настоящее время разработан способ получения метанола частичным восстановлением углекислого газа. При этом используется более дешёвое углеродсодержащее сырьё, но требуется большой объём водорода.
250-350 0 C, 5-30M Па
СН 3 ОН
CO+2H 2
ZnO+ZnCr 2 O 4
CH 3 OH+H 2 O
С O 2 +3H 2
t 0
кат

Наиболее распространённым методом получения этанола является ферментативное расщепление моносахаридов.
зимаза
(С 6 H 10 O 5 ) n +nH 2 O
C 6 H 12 O 6
2С 2 Н 5 OH+2CO 2

Мировое производство мета-нола составляет около 10 мил-лионов тонн в год, этанола производится примерно на порядок больше. Метанол и этанол применяются в качестве растворителей и сырья в орга-ническом синтезе. Кроме того этанол используют в пищевой промышленности и в медицине.

Применение
CH 3 OH
Производство формальдегида, медикаментов.
C 2 H 5 OH
Получение уксусной кислоты, медикаментов, красителей, растворителей, горючего для двигателей и т.д.
C 5 H 11 OH
В парфюмерии ; как реагент для определения жирности молочных продуктов.
C 16 – C 20
Антикоррозийные смазки
C 18 – C 20
Медицинские препараты
www.themegallery.com

Влияние алкоголя на организм

Пивной алкоголизм
Пиво по-разному влияет на мужской и женский организмы:
- Выделяется метилтестостерона,
- Расширяется таз,
- Разрастаются грудные железы,
- У женщин возрастает вероятность заболевания раком грудной железы.

Изменение клеток мозга
- Алкоголь действует на нейроны, вызывая эйфорию, является наркотиком.
- Мозг сопротивляется действию депрессантов, изменяя клеточную оболочку.
- После того как мозг освободился от алкоголя, приспособившееся клетки некоторое время не могут нормально функционировать. Вот почему наутро после выпивки свет кажется невыносимо ярким, а звук громким.

Влияние спиртного на органы человека
Кровь . Алкоголь угнетает продукцию тромбоцитов, а также белых и красных кровяных телец. Итог : малокровие, инфекции, кровотечения.
Сердце . П овышение уровня холестерина в крови, стойкая гипертонию и дистрофию миокарда, дегенерация мышц.

Мозг
Алкоголь замедляет циркуляцию крови в сосудах мозга, приводя к постоянному кислородному голоданию его клеток, в результате чего наступает ослабление памяти и медленная психическая деградация.

Кишечник
Постоянное воздействие алкоголя на стенку тонкого кишечника приводит к изменению структуры клеток, и они теряют способность полноценно всасывать питательные вещества и минеральные компоненты, что заканчивается истощением организма алкоголика.

Печень
Учитывая, что 95% всего поступающего в организм алкоголя обезвреживается в печени, ясно, что этот орган страдает от алкоголя больше всего: возникает воспалительный процесс (гепатит), а затем и рубцовое перерождение (цирроз).
Печень не пьющего человека
Печень пьющего человека

Поджелудочная железа
Больные, страдающие алкоголизмом, в 10 раз больше подвержены вероятности заболеть диабетом, чем непьющие: алкоголь разрушает поджелудочную железу.

Кожа и желудок
Пьющий человек почти всегда выглядит старше своих лет: его кожа очень скоро теряет свою эластичность и стареет раньше времени.
Алкоголь подавляет продукцию муцина, выполняющего защитную функцию по отношению к слизистой желудка, что приводит к возникновению язвенной болезни.
Рак желудка
Рак кожи

Запомни
Водородная связь – это связь между атомом водорода одной молекулы и атомами с большой электоотрицательностью ( О, F , N , Cl ) другой моле-кулы.
Реакция этерификации – взаимодействие спир-тов с органическими и неорганическими кислотами с образованием сложных эфиров.



























































