Просмотр содержимого документа
«Презентация к уроку в 7 классе "Химическое количество вещества"»

МОЛЬ – ЭТО ТАКОЕ КОЛИЧЕСТВО ВЕЩЕСТВА, В КОТОРОМ СОДЕРЖИТСЯ 6 ∙10 23 ЧАСТИЦ (молекул или атомов) ЭТОГО ВЕЩЕСТВА.

N = N A ∙ n , где N – число молекул N A – постоянная Авогадро, молек./моль n – количество вещества, моль
и N A = N / n
Следовательно, n = N / N A

МАССА 1 МОЛЬ ВЕЩЕСТВА НАЗЫВАЕТСЯ ЕГО МОЛЯРНОЙ МАССОЙ, обозначается М и измеряется в г/моль.

1 моль Fe весит 56г
М( Fe ) = 56 г/моль
1 моль S весит 32г
M ( S ) = 32 г/моль
1 моль Na Cl весит 59г
M ( NaCl ) = 59 г/моль
1 моль CuSO 4 весит 1 60 г
M ( CuSO 4 ) = 1 60 г/моль

n = m / M
и, следовательно, m = n ∙ M
и M = m / n

Задача 1.
Найти массу 24 ∙10 23 молекул озона.
Задача 2.
Сколько молекул содержится в 111г
гидроксида кальция Ca ( OH ) 2 ?
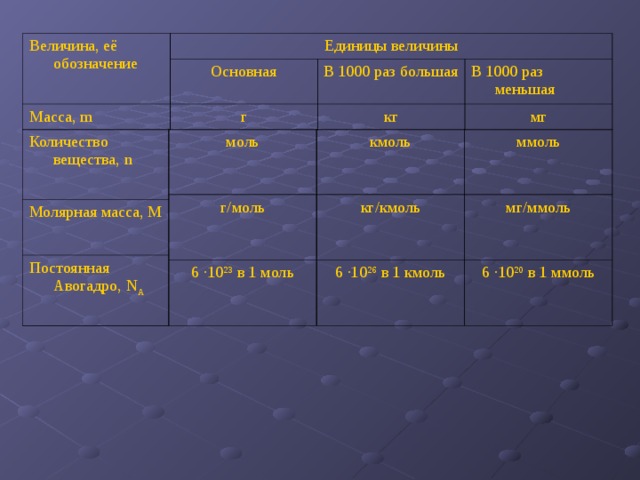
Величина, её обозначение
Единицы величины
Основная
Масса, m
В 1000 раз большая
г
В 1000 раз меньшая
кг
мг
Количество вещества, n
Молярная масса, М
Постоянная Авогадро, N A
моль
кмоль
г/моль
ммоль
кг/кмоль
6 ∙ 10 23 в 1 моль
6 ∙10 26 в 1 кмоль
мг/ммоль
6 ∙10 20 в 1 ммоль

1. Сколько молекул кислорода содержится в 2 моль его?
Какую массу будет иметь это количество кислорода?
2. Какую массу имеют 5 кмоль водорода?
Сколько молекул водорода содержится в этом его количестве?
3. Сколько весят 3∙10 20 молекул воды?

























