
1,2, 18 задание
Учитель: БОУ г. Омска «СОШ №86»
Демонстрационный вариант контрольных измерительных материалов основного государственного экзамена 2021 года по ХИМИИ Инструкция по выполнению работы
Экзаменационная работа состоит из двух частей, включающих в себя 24 задания. Часть 1 содержит 19 заданий с кратким ответом, часть 2 содержит 5 заданий с развёрнутым ответом. На выполнение экзаменационной работы по химии отводится 3 часа (180 минут). Ответы к заданиям 1–19 записываются в виде последовательности цифр (чисел) или числа. Ответ запишите в поле ответа в тексте работы, а затем перенесите в бланк ответов № 1. К заданиям 20–23 следует дать полный развёрнутый ответ, включающий в себя необходимые уравнения реакций и расчёты. Ответы на задания записываются на бланке ответов № 2. Задание 24 предполагает выполнение эксперимента под наблюдением экспертов. К выполнению задания 24 следует приступать после выполнения участником экзамена задания 23 и не ранее чем через 30 минут после начала экзамена. При выполнении работы Вы можете пользоваться Периодической системой химических элементов Д.И. Менделеева, таблицей растворимости солей, кислот и оснований в воде, электрохимическим рядом напряжений металлов и непрограммируемым калькулятором. При выполнении заданий можно пользоваться черновиком. Записи в черновике, а также в тексте контрольных измерительных материалов не учитываются при оценивании работы. Баллы, полученные Вами за выполненные задания, суммируются. Постарайтесь выполнить как можно больше заданий и набрать наибольшее количество баллов. После завершения работы проверьте, чтобы ответ на каждое задание в бланках ответов № 1 и № 2 был записан под правильным номером.

1. Выберите два высказывания, в которых говорится о железе как о химическом элементе. 1) Железо реагирует с хлором. 2) Железо быстро ржавеет во влажном воздухе. 3) Пирит является сырьём для получения железа. 4) Гемоглобин, содержащий железо, переносит кислород. 5) В состав ржавчины входит железо. Запишите номера выбранных ответов.
Ответ: 45

- Выберите два высказывания, в которых говорится о фосфоре как о химическом элементе:
-
- 1) Молекула фосфина состоит из трёх атомов водорода и одного атома фосфора
- 2) Фосфор входит в состав смеси, наносимой на стенку спичечной коробки
- 3) Фосфор имеет несколько аллотропных модификаций
- 4) Фосфор входит в состав растительных и животных белков
- 5) Чёрный фосфор обладает полупроводниковыми свойствами
Ответ: 14

- Выберите два высказывания, в которых говорится о водороде как о химическом элементе:
-
- 1) Водород входит в состав большинства органических соединений
- 2) Водород — самый лёгкий газ
- 3) Водородом заполняют воздушные шары
- 4) Водород содержится в вулканических газах
- 5) Молекула метана содержит четыре атома водорода
Ответ: 15

- Выберите два высказывания, в которых говорится о галлии как о химическом элементе:
-
- 1) Галлий — мягкий хрупкий металл серебристо-белого цвета с синеватым оттенком
- 2) Существование галлия было научно предсказано Д. И. Менделеевым
- 3) Чистый галлий плавится на руке человека
- 4) Галлием заполняют термометры (вместо ртути) для измерения высоких температур
- 5) В состав полупроводниковых материалов часто входит галлий
Ответ: 25

- Выберите два высказывания, в которых говорится о барии как о химическом элементе.
-
- 1) В земной коре содержится 0,05 % бария.
- 2) Барий плавится при температуре 710 °С.
- 3) Зелёная окраска пламени — «визитная карточка» бария, даже если он присутствует в микроскопических количествах.
- 4) Барий используют в качестве геттера — поглотителя остатков газов в вакуумных приборах.
- 5) Барий самовоспламеняется от удара, легко разлагает воду.
Ответ: 13

- Выберите два высказывания, в которых говорится о фторе как о простом веществе.
-
- 1) Кремний и древесный уголь самовоспламеняются во фторе.
- 2) В состав зубной эмали входит до 0,02 % фтора.
- 3) Фтор ядовит.
- 4) Во фреонах фтор работает на «индустрию холода».
- 5) Пластмассы, содержащие фтор, характеризуются химической и термической устойчивостью.
-
Ответ: 13

- На приведённом рисунке изображена модель атома химического элемента. Запишите в поле ответа номер периода и номер группы, в которых расположен химический элемент, модель которого изображена на рисунке.
Решение. На приведённом рисунке изображена модель атома, имеющего два электронных слоя (т. е. располагающегося во втором периоде) и 6 валентных электронов (т. е. располагающегося в VIA группе).
Ответ: 26.

На приведённом рисунке изображена модель атома химического элемента. Запишите в поле ответа номер периода и номер группы, в которых расположен химический элемент, модель которого изображена на рисунке. (Для записи ответа используйте арабские цифры.)
Ответ: 25.

- На приведённом рисунке изображена схема строения электронных оболочек атома. Запишите в поле ответа номер периода и номер группы, в которых расположен химический элемент, схема строения которого изображена на рисунке.
Решение. На приведённом рисунке изображена схема строения атома, имеющего три электронных слоя (т. е. располагающегося в третьем периоде) и 3 валентных электрона (т. е. располагающегося в IIIA группе).
Ответ: 33.

- На приведённом рисунке изображена модель атома химического элемента. Запишите в поле ответа номер периода и номер группы, в которых расположен химический элемент, модель которого изображена на рисунке.
Решение. На приведённом рисунке изображена модель атома, имеющего три электронных слоя (т. е. располагающегося в третьем периоде) и 3 валентных электрона (т. е. располагающегося в IIIA группе).
Ответ: 33.

- На приведённом рисунке изображена схема строения электронных оболочек атома. Запишите в поле ответа номер периода и номер группы, в которых расположен химический элемент, схема строения которого изображена на рисунке.
Решение. На приведённом рисунке изображена схема строения атома, имеющего три электронных слоя (т. е. располагающегося в третьем периоде) и 5 валентных электронов (т. е. располагающегося в VA группе).
Ответ: 35.

- Запишите в поле ответа число электронных оболочек и количество валентных электронов фосфора.
Решение. Число электронных оболочек атома химического элемента равно номеру его периода в Периодической системе Д. И. Менделеева, а число валентных электронов — номеру группы (для главных подгрупп). Фосфор расположен в третьем периоде, VA группе.
Ответ: 35.

- Запишите в поле ответа номер периода и номер группы химического элемента, атом которого в основном состоянии содержит 8 электронов.
Решение. Число электронов атома в основном состоянии равно числу протонов в ядре и равно порядковому номеру химического элемента в Периодической системе Д. И. Менделеева. 8-й элемент — кислород, находится во втором периоде, в VIA группе.
Ответ: 26.

- Запишите в поле ответа номер периода и номер группы химического элемента, атом которого в основном состоянии содержит 18 электронов.
Решение. Число электронов атома в основном состоянии равно числу протонов в ядре и равно порядковому номеру химического элемента в Периодической системе Д. И. Менделеева. 18-й элемент — аргон, находится в третьем периоде, в VIIIA группе.
Ответ: 38.

- Запишите в поле ответа число электронов в основном состоянии и количество электронных оболочек химического элемента, ядро которого содержит 5 протонов.
Решение. Число электронов атома в основном состоянии равно числу протонов в ядре и равно порядковому номеру химического элемента в Периодической системе Д. И. Менделеева. 5-й элемент — бор, расположенный во втором периоде. Номер периода равен числу электронных оболочек.
Ответ: 52.

- Массовая доля кислорода в нитрате железа(II) равна
-
- 1) 26,7%
- 2) 34,2%
- 3) 53,3%
- 4) 64,6%
Решение.
Формула нитратa железа(II) Fe(NO3)2 : . Его молярная масса: M = 56 + 14·2 + 16·6 = 180, поэтому
W = 16·6·100/180 = 53,3%.

- Задания Д19 На какой диаграмме распределение массовых долей элементов соответствует количественному составу сульфита натрия?
Решение.
Формула сульфита натрия: Na2SO3
Его молярная масса: M = 23·2 + 32 + 16·3 = 126, поэтому
W = 23·2·100/126 = 36,5%,
W = 32·100/126 = 25,4%,
W = 100 - 36.5 - 26.4 = 38,1%.
Правильный ответ указан под номером 1.
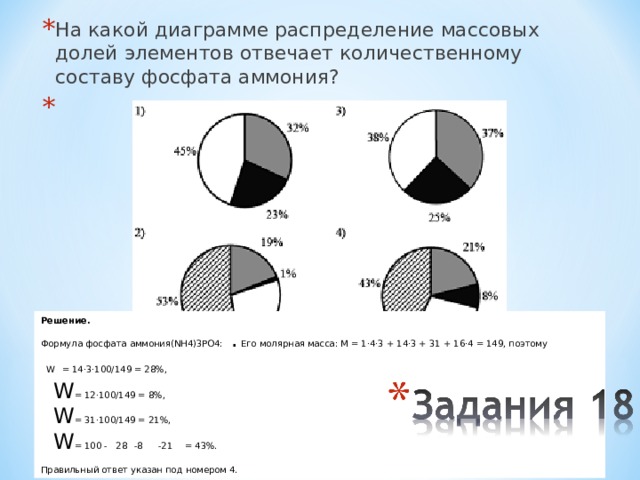
- На какой диаграмме распределение массовых долей элементов отвечает количественному составу фосфата аммония?
Решение.
Формула фосфата аммония (NH4)3PO4 : . Его молярная масса: M = 1·4·3 + 14·3 + 31 + 16·4 = 149, поэтому
W = 14·3·100/149 = 28%,
W = 12·100/149 = 8%,
W = 31·100/149 = 21%,
W = 100 - 28 - 8 - 21 = 43%.
Правильный ответ указан под номером 4.

- Литература
- https://chem-oge.sdamgia.ru/test?a=catlistwstat





































