«СТРОЕНИЕ АТОМА» 8 КЛАСС ВАРИАНТ 1
Часть А. Тест
1. Определите элемент со схемой распределения электронов в атоме 2, 8, 4:
а) Mg; б) Si; в) Cl; г) S.
2. Максимальное число электронов на третьем энергетическом уровне:
а) 14; б) 18; в) 8; г) 24.
3. Максимальное число электронов на р-орбиталях:
а) 2; б) 6; в) 10; г) 14.
4. Укажите химический элемент, атомы которого имеют электронную формулу
1s22s22p63s23p1:
а) Na; б) P; в) Al; г) Ar.
5. Сколько орбиталей в атоме водорода, на которых находятся электроны?
а) 1; б) 2; в) 3; г) 4.
6. Атом какого химического элемента содержит три протона?
а) B; б) P; в) Al; г) Li.
7. Атом какого химического элемента имеет заряд ядра +22?
а) Na; б) P; в) О; г) Ti.
8. Число нейтронов в атоме марганца равно:
а) 25; б) 29; в) 30; г) 55.
9.Даны два химических элемента А и В. Известно, что в атоме элемента А в основном состоянии находится 14 электронов, а в атоме элемента В — 3 протона.
а) Используя Периодическую систему химических элементов Д. И. Менделеева, определите химические элементы А и В.
б) Укажите номер периода и номер группы в Периодической системе химических элементов Д. И. Менделеева, в которых расположен каждый элемент.
в) Установите, металлом или неметаллом являются простые вещества, образованные этими химическими элементами.
г) Составьте формулы высших оксидов, которые образуют элементы А и В.
«СТРОЕНИЕ АТОМА» 8 КЛАСС ВАРИАНТ 2
1. Определите элемент со схемой распределения электронов в атоме 2, 8, 8:
а) Na; б) P; в) Al; г) Ar.
2. Максимальное число электронов на четвертом энергетическом уровне:
а) 14; б) 32; в) 26; г) 18.
3. Максимальное число электронов на s-орбиталях:
а) 2; б) 6; в) 10; г) 14.
4. Укажите химический элемент, атомы которого имеют электронную формулу
1s22s22p63s23p5:
а) Mg; б) P; в) Cl; г) Si.
5. Сколько орбиталей в атоме гелия, на которых находятся электроны?
а) 1; б) 2; в) 3; г) 4.
6. Атом какого химического элемента содержит десять электронов?
а) S; б) H; в) Ne; г) Li.
7. Атом какого химического элемента имеет заряд ядра +35?
а) Ni; б) Pt; в) Br; г) Te.
8. Число нейтронов в атоме цинка равно:
а) 65; б) 22; в) 30; г) 35.
9. аны два химических элемента А и Б. Известно, что в атоме элемента А содержится 19 электронов, а в атоме элемента Б — 16 протонов.
а. Используя Периодическую систему химических элементов Д. И. Менделеева, определите химические элементы А и Б.
б. Укажите номер периода и номер группы в Периодической системе химических элементов Д. И. Менделеева, в которых расположен каждый элемент.
в. Установите, металлом или неметаллом являются простые вещества, образованные этими химическими элементами.
г. Составьте формулы высших оксидов, которые образуют элементы А и Б.
Часть Б.
1.Определите число протонов в ядре атома для элемента, находящегося в Периодической системе химических элементов Д.И.Менделеева:
А) в 3-м периоде, 7 группе, главной подгруппе, Б) в 3-м периоде, 1 группе, главной подгруппе,
В) в 4-м периоде, 2 группе, главной подгруппе,
2.Назовите элемент в атоме которого имеется:
А) 14 нейтронов и 13 электронов Б) 16 нейтронов и 15 электронов В) 2 нейтрона и 2 электрона
3.Определите число протонов и нейтронов в ядре атома элемента:
А) с порядковым номером 26 и массовым числом 56 Б) с порядковым номером 19 и массовым числом 39
В) с порядковым номером 20 и массовым числом 40
4.Заполните пустые клеточки в таблице:
|
| Элемент | Z (пор.№) | Число р+ | Число ē | Число n0 | А (массовое число) |
| 1 |
|
|
|
| 28 | 51 |
| 2 | Ca |
| 20 |
| 20 |
|
| 3 |
|
|
| 18 | 22 |
|
| 4 | K | 19 |
|
|
| 39 |
| 5 |
|
| 10 |
| 10 |
|
5.На рисунке изображена модель электронного строения атома некоторого химического элемента.
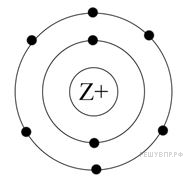 На основании анализа предложенной модели выполните следующие задания:
На основании анализа предложенной модели выполните следующие задания:
1) определите химический элемент, атом которого имеет такое электронное строение;
2) укажите номер периода и номер группы в Периодической системе химических элементов Д.И. Менделеева, в которых расположен этот элемент;
3) определите, его атомную массу.
Часть Б
1.Определите число протонов в ядре атома для элемента, находящегося в Периодической системе химических элементов Д.И.Менделеева:
А) в 2-м периоде, 3 группе, главной подгруппе Б) в 2-м периоде, 4 группе, главной подгруппе
В) в 2-м периоде, 7 группе, главной подгруппе
2. Назовите элемент в атоме которого имеется:
А) 14 нейтронов и 14 электронов Б) 26 нейтронов и 22 электрона В) 22 нейтрона и 18 электронов
3. Определите число протонов и нейтронов в ядре атома элемента:
А) с порядковым номером 3 и массовым числом 7 Б) с порядковым номером 21 и массовым числом 45
В) с порядковым номером 18 и массовым числом 40
4. Заполните пустые клеточки в таблице:
|
| Элемент | Z (пор.№) | Число р+ | Число ē | Число n0 | А (массовое число) |
| 1 |
|
|
|
| 39 | 70 |
| 2 | Zn |
| 30 |
| 35 |
|
| 3 |
|
|
| 16 | 16 |
|
| 4 | Mg | 12 |
|
|
| 24 |
| 5 |
|
| 2 |
| 2 |
|
5.На рисунке изображена модель электронного строения атома некоторого химического элемента.
 На основании анализа предложенной модели выполните следующие задания:
На основании анализа предложенной модели выполните следующие задания:
1) определите химический элемент, атом которого имеет такое электронное строение;
2) укажите номер периода и номер группы в Периодической системе химических элементов Д.И. Менделеева, в которых расположен этот элемент;
3) определите, его атомную массу.







 На основании анализа предложенной модели выполните следующие задания:
На основании анализа предложенной модели выполните следующие задания:









