Министерство здравоохранения Республики Мордовия
Государственное бюджетное профессиональное
образовательное учреждение
Республики Мордовия
«Саранский медицинский колледж»
И.В. Кузнецова
сборник практических работ
по МДК 02.02. Контроль качества лекарственных средств
Учебно – методическое пособие
Разработано для студентов медицинских колледжей,
обучающихся по специальности 33.02.01 «Фармация»

Саранск
2022г
Составитель:
Преподаватель ГБПОУ Республики Мордовия «Саранский медицинский колледж» И.В. Кузнецова.
Рецензент:
Сычева Т.С. –директор ГБПОУ Республики Мордовия «Саранский медицинский колледж»
Кузнецова И.В.
Сборник практических работ по МДК 02.02. Контроль качества лекарственных средств: метод.пособие/ И.В. Кузнецова. – Саранск: СМК, 2022. – 14 с.
Данное пособие составлено согласно требований ФГОС.
Пособие предназначено для студентов четвертого курса средних медицинских учебных заведений, обучающихся по специальности 33.02.01 «Фармация».
Материал рассмотрен и утверждён на заседании цикловой методической комиссии (протокол № от «___» ________ 2022 г.) и на заседании методического совета (протокол № ___ от «____» ______ 2022 г.)
АЛГОРИТМ ПРОВЕДЕНИЯ ВНУТРИАПТЕЧНОГО КОНТРОЛЯ КАЧЕСТВА ЛЕКАРСТВЕННЫХ СРЕДСТВ
1.ПИСЬМЕННЫЙ КОНТРОЛЬ.
Проверяют соответствие записей в паспорте письменного контроля прописи в рецепте, правильности произведенных расчетов.
2.ОПРОСНЫЙ КОНТРОЛЬ.
1. Проводится после изготовления фармацевтом не более 5-ти лекарственных форм.
2.Провизор называет первый входящий в лекарственную форму ингредиент, а в сложных лекарственных формах указывает и его количество.
3.Фармацевт затем называет все взятые им ингредиенты и их количество. Если взят концентрат или полуфабрикат, то называет также их состав и количество.
3. ОРГАНОЛЕПТИЧЕСКИЙ КОНТРОЛЬ.
1.внешний вид лекарственной формы,
2.цвет,
3.запах
4.отсутствие механических включений
4.ФИЗИЧЕСКИЙ КОНТРОЛЬ:
1.общий объем лекарственной формы,
2.находят отклонения по объему,
3.проверяют качество укупорки,
4.сравнивают с допустимыми нормами отклонений.
5.ХИМИЧЕСКИЙ КОНТРОЛЬ:
1.качественный анализ,
2.количественный анализ,
3.производят необходимые расчеты содержания ингредиентов.
6.КОНТРОЛЬ ПРИ ОТПУСКЕ.
1. Проверяют состояние упаковки ЛС, соответствие ее физико-химическим свойствам и лекарственной форме.
2. Оформление этикетки, соответствие ФИО больного, возраста, номера рецепта.
3. Соответствие копий рецептов прописям рецептов.
Внутриаптечный контроль жидких лекарственных форм также предусматривает проверку специфических показателей качества:
ОТСУТСТВИЕ МЕХАНИЧЕСКИХ ВКЛЮЧЕНИЙ.
Под механическими включениями подразумевают посторонние подвижные нерастворимые вещества, кроме пузырьков газа, случайно присутствующих в растворах.
Проверяют их путем легкого встряхивания и перевертывания вверх дном с последующим наблюдением за раствором в прямом и отраженном свете. Если в растворе содержатся взвешенные частицы, то они при этом опускаются вниз и попадают в поле зрения.
Растворы, содержащие частицы, заметные невооруженным глазом должны быть повторно процежены или профильтрованы.
ГЕРМЕТИЧНОСТЬ УКУПОРКИ.
Осуществляется после переворачивания флакона с жидкой лекарственной формой вверх дном. При этом жидкость не должна протекать через пробку.
ПРОВЕРКА ОБЩЕГО ОБЪЕМА.
Производится тем же цилиндром и другой измерительной посудой, с помощью которой готовили растворы.
ХИМИЧЕСКИЙ КОНТРОЛЬ ЖИДКИХ ЛЕКАРСТВЕННЫХ ФОРМ.
Жидкие лекарственные формы подвергаются химическому контролю в зависимости от состава и назначения; качественному или полному химическому.
1.КАЧЕСТВЕННЫЙ КОНТРОЛЬ
Качественному контролю подвергаются лекарственные формы, изготовленные по индивидуальным рецептам или требованиями ЛПУ выборочно, но не менее 10% от общего числа рецептов.
Особое внимание обращается на лекарственные формы:
- для детей, особенно новорожденных;
- применяемые в глазной практике;
- содержащие ядовитые и наркотические вещества.
2.ОБЯЗАТЕЛЬНЫЙ ПОЛНЫЙ ХИМИЧЕСКИЙ АНАЛИЗ.
Обязательному полному химическому анализу подвергаются растворы кислоты хлороводородной для внутреннего применения, атропина сульфата, ртути дихлорида и серебра нитрата.
Результаты качественного и полного химического контроля регистрируются в журналах.
В журнал заносятся также случаи неудовлетворительного изготовления лекарственных средств, обнаруженные при контроле качества их изготовления в аптеке провизорами-аналитиками центра по контролю качества лекарственных средств. Выявленный брак изымается для повторного анализа с составлением акта изъятия и объяснительной записки. Лекарственное средство изготавливается заново, проверяется.
КАЧЕСТВЕННЫЙ АНАЛИЗ жидких лекарственных форм заключается в определении подлинности медикамента или отдельных ингредиентов, входящих в состав лекарственной формы.
КОЛИЧЕСТВЕННЫЙ АНАЛИЗ жидких лекарственных форм заключается в определении количественного содержания вещества, входящего в состав лекарственной формы, рефрактометрическим, объемным или другими методами.
ВНУТРИАПТЕЧНЫЙ КОНТРОЛЬ МАЗЕЙ И ЛИНИМЕНТОВ.
МАЗИ- мягкая лекарственная форма, предназначенная для нанесения на кожу, раны или слизистые оболочки. Мази состоят из основы и лекарственного вещества, равномерно распределенных в ней.
По типу дисперсных систем различают мази гомогенные (сплавы, растворы, суспензионные, эмульсионные и комбинированные), а в зависимости от консистентных свойств – собственно мази, пасты, кремы, гели и линименты.
Мази в зависимости от состава и назначения подвергаются обязательным и выборочным видам контроля и химическому контролю.
ОПРЕДЕЛЕНИЕ ОДНОРОДНОСТИ СМЕШЕНИЯ.
К различным мазям ГФ предъявляют различные требования к степени их однородности, что определяет неодинаковые методы установления однородности.
Однородность устанавливается органолептически
МАЗИ ТИПА СПЛАВА, либо ТИПА РАСТВОРОВ – в ступке или в баночке для отпуска, шпателем снимают верхний слой на 1-1,5 см. и на сформированной поверхности не должно быть темных или цветных разводов.
ЕСЛИ МАЗЬ ТИПА СУСПЕНЗИЙ:
1. Однородность устанавливают путем растирания между пальцев, не должно ощущаться крупинок не растертого порошка.
2. На тыльной стороне левой ладони наносят некоторое количество мази и растирают пальцами правой руки.
ФИЗИЧЕСКИЙ КОНТРОЛЬ.
Вначале взвешивают пустую банку, затем после приготовления мази и заполнения, банку взвешивают с мазью. По разности между массой пустой банки находят массу мази. Затем находят отклонения и сравнивают их с приказом N751н.
ХИМИЧЕСКИЙ КОНТРОЛЬ
Обычно сначала производят отделение от основы. Это отделение производят или органическими растворителями, которые извлекают основу, при этом лекарственные вещества не растворяются; или же растворителями, которые извлекают лекарственные вещества, не извлекая основы. При извлечении из мази лекарственных веществ очень часто пользуются химическими свойствами этих веществ. Например, окись ртути извлекают соляной кислоты и т.д.
КОЛИЧЕСТВЕННЫЙ АНАЛИЗ лекарственных веществ, входящих в мазь, можно производить и без отделения основы; например, в цинковой мази окись цинка можно и определить весовым путем после сжигания навески.
В целом анализ мази зависит от свойств, входящих ингредиентов.
КОНТРОЛЬ КАЧЕСТВА ПОРОШКОВ
Контроль осуществляется в 2 этапа:
После приготовления
Письменный (составление паспорта письменного контроля)
Органолептический (цвет, запах, однородность, сыпучесть, отсутствие посторонних механических включений)
Полный химический (качественный и количественный анализ действующих веществ)
После расфасовки ·
Физический (общая масса, отклонение в массе данной серии)
Качественный
Контроль при отпуске (оформление этикеток, наличие предупредительных надписей, номер серии, срока годности)
4 курс 7 семестр
Практическое занятие 1
Контроль качества лекарственных средств, производных спиртов и альдегидов.
Пример: Провести полный внутриаптечный анализ рецепта.
Проведение обязательных видов внутриаптечного контроля лекарственной формы:
Rp: Hexamethylentetramini 0,25
D.t.d. №12
S.по 1 порошку 3 раза в день
1.1 Письменный контроль
Проверка правильности оформления паспорта письменного контроля.
Паспорт письменного контроля (обратная сторона)
Гексаметилентетрамина 3,0
0,25*12 = 3,0
mобщ = 3,0
Паспорт письменного контроля (лицевая сторона)
Дата ____ № Рецепта _____
Hexamethvlentetramini 3,0
Приготовил:____ (подпись)
Проверил _____ (подпись)
№ анализа ______
1.2 Органолептический контроль
Состоит в проверке внешнего вида, запаха и специфических показателей качества порошков: сыпучести и однородности. Для определения сыпучести порошок осторожно пересыпают с одной капсулы в другую. Порошок должен быть сухим, сыпучим. Не должно наблюдаться образования комочков массы и ее прилипания к капсуле. Однородность порошков проверяют до разделения массы на дозы. Для определения однородности порошок собирают в центр капсулы и осторожно надавливают на него головкой пестика. На образующейся поверхности не должно наблюдаться отдельных частиц, блесток. Порошок рассматривают на расстоянии 25 см от глаза. Проверка однородности порошков проводится выборочно, но в течение рабочего дня у каждого фармацевта. Результаты контроля регистрируются в журнале.
1.3 Физический контроль
Выборочно проверяют количество и массу отдельных доз (не менее, чем у трех порошков).
Количество доз: 12
m= 0,25
Доп.отк = ± 10%
Результаты контроля регистрируются в журнале.
1.4 Контроль при отпуске:
В соответствии с физико-химическими свойствами порошки гексаметилентетрамина завернуты в капсулы из парафинированной или вощеной бумаги (могут гидролизоваться во влажном воздухе) и помещены в бумажный пакет;
Основная этикетка «Внутреннее» с обозначением «Порошки». Предупредительная надпись: «Беречь от детей». На этикетке указаны наименование и местонахождение аптеки, номер рецепта, фамилия и инициалы больного, способ применения (по 1 порошку 3 раза в день), дата, цена, срок годности.
Номер рецепта и фамилия больного на рецепте соответствуют номеру и фамилии на этикетке.
Лицо, отпускающее лекарственное средство, ставит подпись на обратной стороне рецепта.
Химический контроль
2.1 Подлинность
1) Кислотный гидролиз и доказательство составных частей
При нагревании с разведенной серной кислотой выделяется формальдегид, который обнаруживается по запаху.
(CH2)6N4+ 2H2S04+ 6Н20 = 6НСO + 2(NH4)2S04
Затем добавляют избыток щелочи и снова нагревают. Появляется запах аммиака.
(NH4)2S04+ 2NaOH = Na2S04+ 2NH3+ 2Н20
2) Реакция образования ауринового красителя
При нагревании препарата с концентрированной серной и салициловой кислотами образуется красное окрашивание (ауриновый краситель).
(CH2)6N4+ 2H2S04+ 6Н20 = 6НСO+ 2(NH4)2S04

ауриновый краситель
2.2 Количественное определение
Метод нейтрализации. Прямое титрование.
0,05г препарата растворяют в 1 мл воды и титруют 0,1 моль/л раствором хлористоводородной кислоты в присутствии смешанного индикатора (2 капли метилового оранжевого и 1 капля метиленового синего) до перехода зеленого окрашивания в фиолетовое.
(CH2)6N4+ НС1 = (CH2)6N4* НС1
Находим титр.
T(в-ва) m(в-ва) , T(в-ва) Сн (в-ва) Мэ (в-ва) , г/мл.
v(р-ра) 1000
Т= 0,1*140,186 = 0,014 г/мл, т.е
1000
1 мл 0,1 моль/л раствора НС1 соответствует 0,014 г гексаметилентетрамина
Vориент = m = 0,05 = 3,57 мл
T 0,014
Где,
m - минимальная навеска, взятая на титрование
Т - титр рабочего раствора по определяемому веществу
m = V*K*T*A
а
А— масса одного порошка (одной дозы)
а - минимальная навеска, равная 0,05
V - объём титранта, фактически пошедший на титрование
Самостоятельная работа
Задание: Провести полный внутриаптечный контроль качества лекарственных средств. Записать в тетради разбор рецептов по вышеизложенному алгоритму. Рецепт написать на латинском языке.
Возьми: Раствора формальдегида 10% 100 мл
Смешай. Дай. Обозначь. Для дезинфекции.
Возьми: Раствора спирта этилового 70% 50 мл
Дай таких доз №1 флакон.
Обозначь. Для растирания кожи.
Возьми: Раствора гексаметилентетраамина 40% 5 мл
Дай таких доз №5
Обозначь. Внутримышечно по 5 мл 1 раз в день.
Закрепление полученных знаний:
Решение ситуационных задач.
Приведите уравнения реакций количественного определения гексаметилентетрамина (М=140,19 г/моль) титрованием хлороводородной кислотой по смешанному индикатору (название, формулы, соотношение индикаторов в смешанном индикаторе, переход окраски в точке конца титрования). Рассчитайте содержание гексаметилентетрамина, если на титрование навески массой 0,1405 г затрачено 10,2 мл 0,1 моль/л раствора хлороводородной кислоты (К=0,99).
Рассчитайте содержание гексаметилентетрамина (%), если к навеске массой 0,1236 г добавлено 50,0 мл 0,1моль/л (Fэ = ½ Н2SO4) раствора серной кислоты (К=1,01), а на титрование ее избытка затрачено 15,6 мл 0,1 моль/л раствора натрия гидроксида (К=0,99).
Практическое занятие 2
Контроль качества лекарственных средств, производных углеводов и простых эфиров.
Пример:
Провести полный внутриаптечный анализ рецепта.
Проведение обязательных видов внутриаптечного контроля лекарственной формы:
Rp: Solutionis Glucоsae 5% - 100,0
Sterillis!
Da. Signa: детское (по 1 столовой ложке 2 раза в день – ребенку 1 месяц)
1.1. Письменный контроль:
Паспорт письменного контроля (обратная сторона)
Воды очищенной для инъекций 50 мл
Глюкоза 5,5г
Воды очищенной для инъекций до 100 мл
Паспорт письменного контроля (лицевая сторона)
Дата ____ № Требования _____
Aquae purificata pro injectionibus 50ml
Glucosum 5,5
Aquae purificata pro injectionibus ad 100 ml
Приготовил:____ (подпись)
Проверил _____ (подпись)
№ анализа ______
1.2. Органолептический контроль:
Прозрачный раствор без запаха, без механических включений, сладкого вкуса.
1.3. Контроль при отпуске:
На стерильном флаконе из нейтрального стекла должна быть этикетка «Внутреннее» с обозначением:
- фамилии больного, соответствия № на рецепте, квитанции, и рецептурного журнала;
- наименования лекарственного средства, его концентрации и объема;
- даты изготовления, срока годности 30 дней, № анализа;
- предупредительных этикеток: «Хранить в темном прохладном месте», «Беречь от детей».
2. Проведение полного химического анализа.
2.1. Проведение качественного анализа (реакции идентичности) глюкозы
1) В пробирку помещают 1 мл раствора, прибавляют несколько капель раствора серебра нитрата и 5-6 капель 10% раствора аммиака. Постепенно образуется серый осадок.
C6H12O6 +2Ag(NH3)2OH = 2Ag↓ + C6H9O7 + 2NH3 + H2O
2) В пробирку помещают 1 мл раствора, прибавляют несколько капель реактива Фелинга. Нагревают. Образуется красный осадок.
C6H12O6 + (C8H8O12NaK)2Cu = C6H9O7Na + 4C4H4O6NaK + Cu(OH)2 + 2H2O
2Cu(OH)2 = Cu2O↓+2H2O
2.2. Количественное определение: Рефрактометрия:
Определение можно провести с помощью рефрактометрических таблиц с использованием фактора, который для всех концентраций составляет 0,00142.
Расчет массовой доли вещества в растворе проводится по формуле:
Х(%) =  , X(г) =
, X(г) = 
где n – показатель преломления раствора;
no – показатель преломления растворителя;
F – фактор – для всех концентраций глюкозы составляет 0,00142.
n = 1,3401 no = 1,333
Х(%) = = 5%
= 5%
Х(г) =  = 0,05 г в 1 мл
= 0,05 г в 1 мл
Вычисления фактического и допустимого отклонения в лекарственной форме. Допустимая норма отклонения по пр. №751н в массе отдельных ингредиентов в жидких лекарственных формах составляет ± 4%.
Это обозначает, что количество вещества в растворе может находится в пределах от 4,8% до 5,2%.
Способ вычисления
5г – 100%
Х = 4%
Х=0,2г
Произвести расчет фактического отклонения по количественному содержанию вещества в лекарственной форме.
Сделать вывод о качестве лекарственной формы.
Самостоятельная работа обучающихся
Задание: Провести полный внутриаптечный контроль качества лекарственных средств. Записать в тетради разбор рецептов по вышеизложенному алгоритму. Рецепт написать на латинском языке.
Возьми: Раствора глюкозы 40% 200 мл
Простерилизуй!
Обозначь. Внутривенно по 10 мл.
Возьми: Мази Димедрола 0,3 - 15,0
Дай. Обозначь. На пораженные участки кожи.
Закрепление полученных знаний:
Решение ситуационных задач.
Для количественного определения димедрола в порошках, берем на титрование 1 порошок (а=0,21г), растворяем его в, приблизительно, 2 мл. воды, добавляем 2 капли фенолфталеина и титруем 0,1 Н раствором NaOH до розового окрашивания. Сделать вывод о качестве лекарственной формы, если на титрование пошло – 0,82 мл 0,1 Н раствора NaOH.
2. Произвести расчеты концентрации раствора глюкозы, используя показатели преломления – 1,3607
Для расчета используют формулу
С%=  ,
,
где n – показатель преломления исследуемого раствора;
n0 – показатель преломления воды (1,333)
F – фактор преломления. F=0,00142
Практическое занятие 3
Контроль качества лекарственных средств, производных карбоновых кислот и аминокислот.
Контроль качества лекарственных средств, производных аминоспиртов.
Пример:
Внутриаптечный контроль лекарственной формы:
Rp: Кислоты аскорбиновой 0,2
Глюкозы 0,3
D.t.d. №10
S. по 1 порошку.
1. Пропись анализируемой лекарственной формы на латинском языке.
Rp.: Acidi ascorbinici 0,2
Glucosi 0,3
D.t.d. №10
S. по 1 порошку.
1.1 Письменный контроль
1.2. Органолептический контроль лекарственной формы (агрегатное состояние, цвет, однородность)
Однородный белый порошок без запаха.
2. Химический контроль
2.1. Подлинность
1) 0,05 г лекарственной формы растворить в 2 мл воды и добавить 2 капли раствора AgNO3;

Определение аскорбиновой кислоты=Образуется серый осадок металлического серебра.
2) Около 0,05 г лекарственной формы растворить в 2 мл воды и прибавить 2 мл реактива Фелинга и нагреть до кипения; обратить внимание на выпавший осадок.
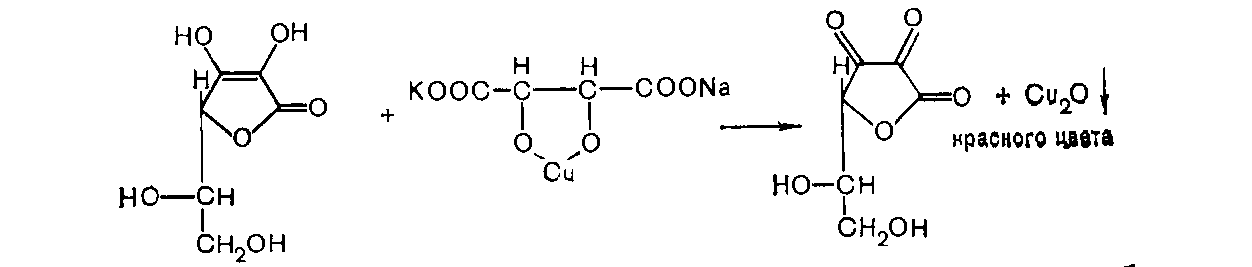
Выпадает кирпично-красный осадок меди (I) оксида.
2.2 Количественное определение
Для количественного определения кислоты аскорбиновой в порошках берем на титрование 0,1 г лекарственной формы (точная навеска), растворяем в 2мл воды и титруем 0,1Н раствором йода до желтого окрашивания.
Метод анализа-йодометрический, индикатор – крахмал. Титруют 0,1 Н раствором йода.

Сделать вывод о качестве лекарственной формы, если на титрование пошло 4,5 мл раствора йода
W=V*T*р
а,
где Т=0,0088 г/мл
W=(4,5*0,0088*0,3):0,1=0,12
Норма допустимого отклонения в массе навески отдельных веществ по приказу №751н ±15%.
15% от 0,1=0,015
Допустимое отклонение [0,085-0,115].
Вывод: Лекарственная форма изготовлена неудовлетворительно.
Самостоятельная работа обучающихся:
Задание: Провести полный внутриаптечный контроль качества лекарственных средств. Записать в тетради разбор рецептов по вышеизложенному алгоритму. Рецепт написать на латинском языке.
Возьми: Раствора кальция глюконата 10% - 200,0
Дай. Обозначь. По 1 ст. ложке 3 раза в день.
Возьми: Раствора кислоты аскорбиновой 5% - 1 мл.
Дай таких доз №20 в ампулах.
Обозначь. По 1мл внутримышечно 2 раза в день.
Возьми: Таблетки Глютаминовой кислоты 0,25 №20
Дай. Обозначь. По 1 г 2-3 раза в день.
Возьми: Раствора кислоты аминокапроновой для инъекций 5% - 100 мл
Дай. Обозначь. Внутривенно.
Возьми: Раствора эфедрина гидрохлорида 2% - 10,0
Дай. Обозначь. Капли для носа. По 5 капель в каждую ноздрю.
Возьми: Раствора адреналина гидрохлорида 0,1% - 1 мл
Дай таких доз № 10 в ампулах
Обозначь. Подкожно 1 раз в день.
Закрепление изученного материала.
Приведите уравнения реакций количественного определения глютаминовой кислоты методом алкалиметрии. Рассчитайте содержание глютаминовой кислоты (М.м.=147,1) в одной таблетке, если на титрование 0,261 г порошка растертых таблеток пошло 16,7 мл 0,1 М раствора натрия гидроксида (К=1,01). Средняя масса таблетки (Р) равна 0,264 г.
Приведите уравнение реакции количественного определения аскорбиновой кислоты (М.м.=176,1) методом йодатометрии. Рассчитайте содержание аскорбиновой кислоты, если на титрование навески 0,1012 г было израсходовано 11,2 мл 0,0167 М раствора калия йодата (К=1,0).






















