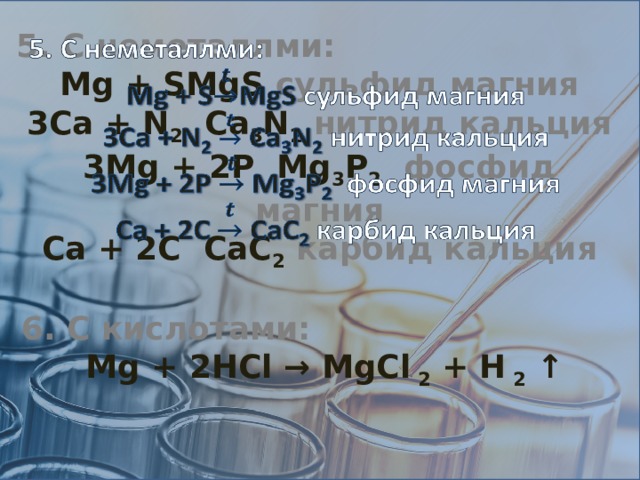Просмотр содержимого документа
«Щелочноземельные металлы»

Щелочноземельные
металлы

Малое число электронов (1-3) на внешнем энергетическом уровне.
Сравнительно большие радиусы атомов.
Внешние электроны значительно
удалены от ядра и слабо
с ним связаны, поэтому они легко отрываются от атома
Be
Mg
Ca
Sr
Ba
Ra
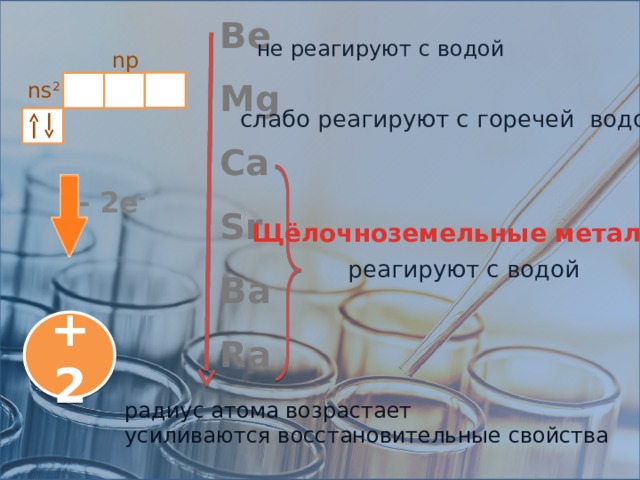
не реагируют с водой
np
ns 2
слабо реагируют с горечей водой
- 2e -
Щёлочноземельные металлы
реагируют с водой
+2
радиус атома возрастает
усиливаются восстановительные свойства

кальций
магний
стронций
барий

Минералы магния
MgCO 3 ·CaCO 3 – доломит
MgCO 3 - магнезит
KCl · MgCl 2 · 6H 2 O – карналлит

Минералы кальция
CaCO 3 - кальцит
СaSO· 2H 2 O - гипс
3Ca 3 (PO 4 ) 2 ·CaF 2 - апатит

Получение Са и Мg
электролиз расплава СaCl 2 или MgCl 2
СaCl 2 Ca + Cl 2
алюмотермический метод
4CaO + 2Al 3Ca + CaO · Al 2 O 3

ХИМИЧЕСКИЕ СВОЙСТВА Са и Мg
Mg + O 2 = 2MgO
2. с галогенами
Ca + Br 2 = CaBr 2
3. C водой:
Mg + H 2 O MgO + H 2 ↑
Ca + 2H 2 O → Ca(OH) 2 + H 2 ↑
4. с водородом
Ca + H 2 CaH 2
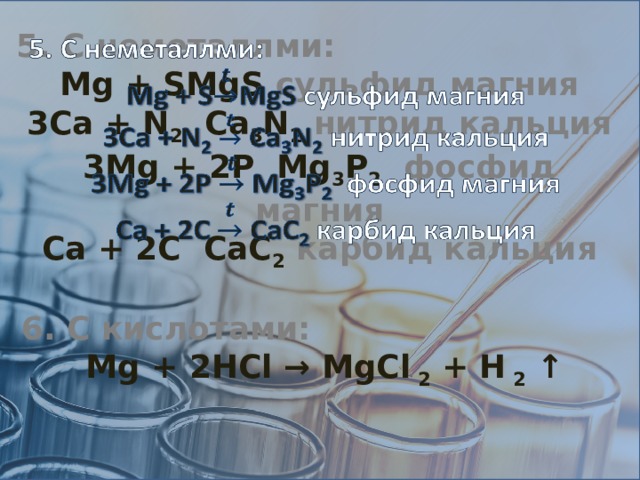
5. C неметаллми:
Mg + SMgS сульфид магния
3Ca + N 2 Ca 3 N 2 нитрид кальция
3Mg + 2P Mg 3 P 2 фосфид магния
Ca + 2C CaC 2 карбид кальция
6. C кислотами:
Mg + 2HCl → MgCl 2 + H 2 ↑
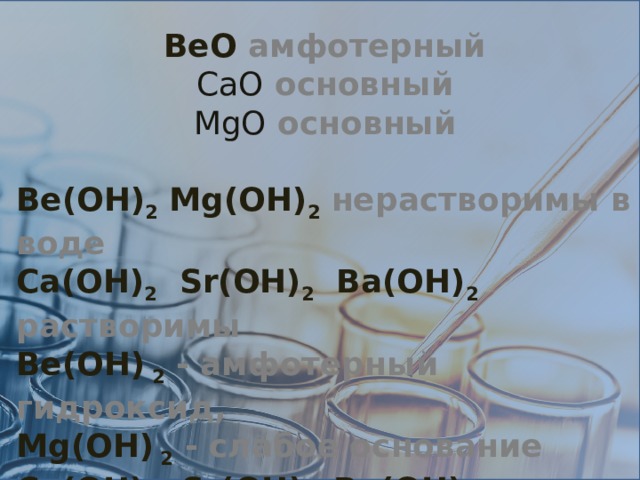
BeO амфотерный
CaO основный
MgO основный
Be(OH) 2 Mg(OH) 2 нерастворимы в воде
Ca(OH) 2 Sr(OH) 2 Ba(OH) 2 растворимы
Be(OH) 2 - амфотерный гидроксид,
Mg(ОH) 2 - слабое основание
Ca(OH) 2 Sr(OH) 2 Ba(ОH) 2 сильные основания

Жёсткость воды — это комплекс свойств воды связанных содержанием в ней Ca 2+ и Mg 2+
1) в котлах и трубах образует накипь
2) ухудшает моющие свойства мыла
3) усиливает коррозию металлов
4) в жесткой воде плохо разваривается мясо

Жёсткость воды
ВРЕМЕННАЯ ПОСТОЯННАЯ
КАРБОНАТНАЯ НЕКАРБОНАТНАЯ
Ca(HCO 3 ) 2 , Mg(HCO 3 ) 2
CaCl 2 , MgSO 4 , CaSO 4
добавление соды
CaCl 2 + Na 2 CO 3 CaCO 3 ↓+ 2NaCl
кипячение
Ca(HCO 3 ) 2 CaCO 3 ↓+ CO 2 + H 2 O
добавление соды
Ca(HCO 3 ) 2 + Na 2 CO 3 CaCO 3 ↓+ 2NaHCO 3