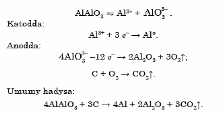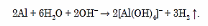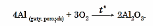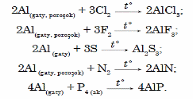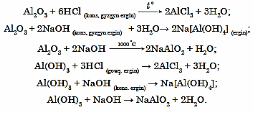Tema: Alýuminiý.
Meýilnamasy:
1.Alýuminiýniň açylyşy.
2.Alýuminiýniň fiziki häsiýetleri.
3.Alýuminiýniň himiki häsiýetleri.
4.Alýuminiýniň izotoplary.
5.Alýumininiň alnyşy.
6.Alýuminiýniň ulanylyşy.
7.Alýuminiý elementiniň önümleri.
Alýuminiý erkin halynda kümüş ýalpyldyly ýeňil metaldyr. Onuň birnäçe artykmaçlygy bardyr: ýeňil, elektrik toguny we ýylylygy oňat geçirýär, howada zaýalanmaýar, daşy ýalpyldap duransoň owadan, maýyşgaklygy temperatura görä az üýtgeýär. Alýuminiý metalyny mehaniki taýdan işläp we ondan folga ýasap bolýar. Onuň splawlarynyň hiç biri- de beýleki materiallaryň berkliginden we çydamlylygyndan pes däldir. Alýuminiý elementi ilkinji gezek daniýaly alym Ersted tarapyndan açyldy. Erkin halyndaky alýuminiý elementiniň we onuň emele getiren
splawlarynyň hem-de birleşmeleriniň durmuşda ähmiýeti uludyr. Alýuminiý ilkinji gezek onuň birleşmelerinden gaýtarmak usuly bilen alnan bolsa, häzirki wagtda ol elektroliz usuly bilen alynýar(«Elektroliz» temasyna seret). Günbatar Türkmenistanda alýuminiý öndürmek üçin senagat ähmiýetli alýunit mineraly bardyr. Alýunitiň düzüminde25% çemesi alýuminiý oksidi Al2O3 bolup, beýleki minerallardan saýlap alnandan soň, ony kriolit Na3[AlF6] bilen garýarlar.
Şol maddalaryň bellibir mukdar gatnaşygynda alnan garyndysynyň(1:9) eremek temperaturasy (1000 °C) arassa alýuminiý oksidiniň eremek temperaturasyna(2050°C) garanda müňlerçe gradus
pes bolýar Şonda elektroliz etmek üçin harçlanan energiýa azalýar, netijede, ahyrky alynýan önümiň özüne düşýän gymmaty peselýär.
Alýuminiý oksidiniň elektrolizi şol bir wagtda hem elektrotermiki, hem elektrohimiki hadysadyr.
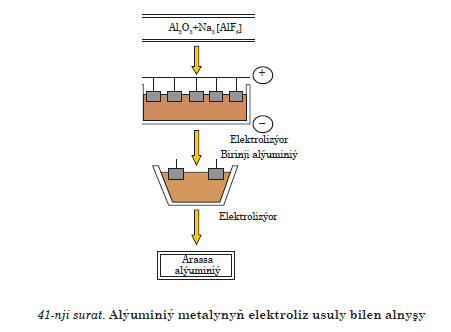
Şonda elektrik togunyň täsirinde garyndy ilki suwuk hala geçýär. Şeýlelikde, elektrodlaryň üstünde geçýän okislenme- gaýtarylma reaksiýasy netijesinde katodyň üstünde alýuminiý bölünip çykýar. Anodyň üstünde bolsa bölünip çykýan kislorod anodyň materialy bilen(kömür) reagirleşip, reaksiýa netijesinde uglerod(IV) oksidi bölünip çykýar(41-nji surat). Şonda
geçýän termik dissosiasiýany hem-de katod we anod hadysalaryny şeýle göz öňüne getirmek bolar:
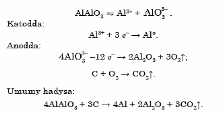
Alýuminiý metallaryň elektrohimiki güýjenme hatarynda öňde ýerleşýändigine (aktiwligine) garamazdan, howada durnuklydyr. Onuň şeýle bolmagyna emele gelýän oksid gatlagynyň dykyzlygynyň ýokarydygy sebäp bolýar. Eger-de oksid gatlagyny haýsydyr bir gaty jisim bilen gyryp aýyrsak, onda ol bada-bat täzeden emele gelýär. Haçanda, oksid gatlagynyň emele gelmegine mümkinçilik berilmese, mysal üçin, ol gyzgyn aşgaryň erginine salynsa, onda ol suw bilen özara reagirleşýär. Şonda ol suwuň düzüminden wodorody gysyp çykarýar:
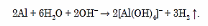
Ýokary temperaturada alýuminiý köp metallaryň we metal däl elementleriň oksidlerini gaýtaryp bilýär. Mysal üçin:
Cr2O3 + 2Al → Al2O3 + 2Cr;
8Al + 3Fe3O4 → 4Al2O3 + 9Fe.
Kyn suwuk hala geçýän metallary almagyň şu metallotermik usulyna alýuminotermiýa diýilýär. Ol reaksiýalar netijesinde köp mukdarda energiýa ýylylyk görnüşinde bölünip çykýar. Şonda reaksiýalaryň önümleri suwuk halyndaky ýagdaýda emele gelýärler.
Alýuminiý gyzdyrylanda howada ýanýar. Şonda alýuminiý oksidi emele gelýär:
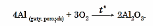
Alýuminiý ýokary temperaturada (200–1200°C) galogenler, kükürt, azot, fosfor ýaly metal däl elementler bilen reagirleşýär. Şonda alýuminiý elementiniň beýleki elementler bilen birleşmeleri emele gelýärler:
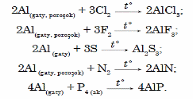
Alýuminiý çylşyrymly maddalaryň birnäçesi bilen hem reagirleşýär. Şonda ol aşgaryň gatnaşmagynda suwuň we kislotalaryň erginlerinden wodorody gysyp çykarýar. Duzlaryň
erginleri bilen reaksiýalarynda bolsa, metallaryň elektrohimiki güýjenme hatarda özünden yzky hatarda ýerleşen metallaryň birleşmeleriniň erginini gysyp çykarýar:

Alýuminiý elementiniň möhüm birleşmelerine alýuminiý oksidi, alýuminiý gidroksidi we duzlary degişlidirler.
Alýuminiý oksidi Al2O3 ýokary temperaturada suwuk hala geçýän, (2050°C) ak reňkli gaty maddadyr. Suwda eremeýär. Alýuminiý gidroksidi ak reňkli, suwda eremeýän gaty maddadyr. Alýuminiý oksidine we alýuminiý gidroksidine amfoterlik häsiýetleri mahsusdyr (VII synpyň «Himiýa» kitaby. «Amfoterlilik» diýen tema seret).
Ýagny olar kislota hem-de aşgarlar bilen reagirleşip, iki ýagdaýda hem duz we suw emele getirýärler:
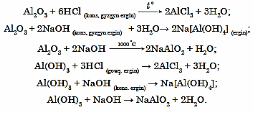
Alýuminiý duzlary esaslar bilen reagirleşýärler. Netijede, suwda eremeýän ak reňkli alýuminiý gidroksidiniň çökündisi emele gelýär:
АlСl3 + 3NaOH (gowş. ergin) → Аl(ОН)3↓+ 3NaCl;
АlСl3 + 4NaOH (kons. ergin) → Na[Al(OH)4]↓ + 3NaCl;
АlСl3+ 3(NH3 • H2O) (kons. sowuk ergin) → Al(OH)3↓ + 3NH4Cl.
Bu reaksiýalar alýuminiý ionynyň hil reaksiýasy hökmünde hem ulanylýar. Gyzdyrylanda alýuminiý gidroksidi we alýuminiý nitraty dargaýarlar:
2Аl(ОН)3 (gaty) → Аl2О3 (gaty) + 3H2O(suwuk) (575 °C);
4Al(NO3)3 (ergin) → 2Аl2О3 (gaty)+ 12NO2 (gaz)+ 3H2O(bug).
(150–200 °С)
Alýuminiý duzlary suw erginlerinde alýuminiý kationy boýunça gidrolizleşýärler:
Al3+ + 3H2O → Al(OH)3 + 3H+ (pH
Alýuminiý tehnikada ähmiýetli metaldyr. Ol halk hojalygynda ulanylýan dürli splawlary almakda giňden peýdalanylýar. Alýuminiý metalynyň dýuralýumin, silumin ýaly splawlary ýeňil we berk bolup, olar uçar, gämi ýasamakda we gurluşyklarda giňden peýdalanylýar. Alýuminiý elektrik geçiriji simleri ýasamakda, korroziýa garşy örtükleri almakda, ýüz görülýän aýnalary ýasamakda, alýuminotermiki usul bilen beýleki metallary öndürmekde ulanylýar.
Alýuminiý elementiniň möhüm birleşmeleriniň biri bolan alýuminiý sulfaty Al2(SO4)3 Türkmenabadyň himiýa kärhanasynda öndürilýär we ol suwy arassalamak işinde giňden peýdalanylýar. Alýuminiý oksidinden ybarat bolan tebigy we emeli rubin mineralynyň sagadyň podşipniklerini ýasamakda we kwant elektrotehnikasynda lazer şöhlelerini almakda ähmiýeti uludyr.