
КГБПОУ «Красноярский колледж
отраслевых технологий и предпринимательства»
Преподаватель: Буркаль Екатерина Валентиновна
Красноярск 2017

их растворы или расплавы НЕ ПРОВОДЯТ электрический ток
их растворы или расплавы ПРОВОДЯТ электрический ток
Вид химической связи
Ковалентная неполярная
или мало полярная
Ионная или ковалентная
сильно полярная

C оли
Кислоты
Щёлочи
HCl, H 3 PO 4
H 2 SO 4
KOH, NaOH
Ba(OH) 2
Na 2 SO 4 ,
KCl, Ca(NO 3 ) 2
Органические вещества
Метан CH 4
Сахар C 12 H 22 O 11
Оксиды
Газ, осадок, вода
NO, Na 2 O
CaO

процесс растворения электролитов сопровождается образованием заряженных частиц, способных проводить электрический ток.
С. А. Аррениус.
Процесс появления гидратированных ионов в водном растворе называется электролитической диссоциацией (С. Аррениус, 1887 г.) .


- Все вещества по их способности проводить электрический ток в растворах или расплавах делятся на электролиты и неэлектролиты .

- В растворах электролиты диссоциируют ( распадаются) на положительные и отрицательные ионы.
Процесс распада электролита на ионы в растворе или расплаве называется электролитической диссоциацией.
:
:
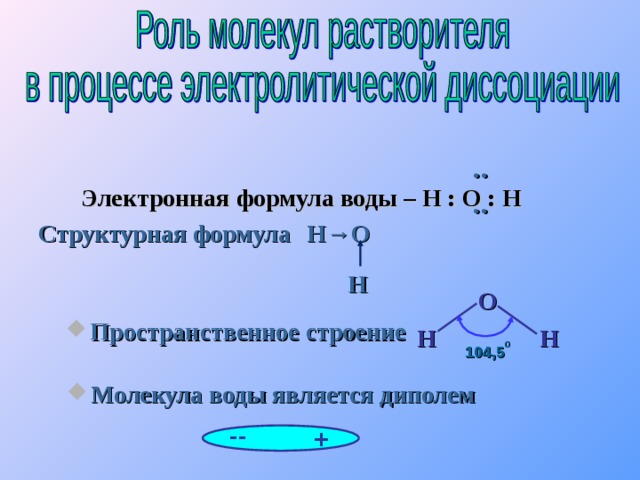
Электронная формула воды – Н : О : Н
Структурная формула Н →О
Н
- Пространственное строение
O
H
H
- Молекула воды является диполем
104,5 0
--
+

1.Ориентация молекул воды.
2.Гидратация.
3. Разрыв ионной связи.
4.Перемещение гидратированных ионов в раствор.

- Ориентация молекул воды.
- Гидратация.
- Перемещение гидратиро- ванных ионов в раствор.

- Ориентация.
- Гидратация.
- Ионизация.
- Диссоциация.

- Ориентация.
- Гидратация.
- Ионизация.
- Диссоциация.

- Ориентация.
- Гидратация.
- Ионизация.
- Диссоциация .

- Причиной диссоциации электролита является его взаимодействие с молекулами воды, т.е. его гидратация

NaCl+mH 2 O Na + (H 2 O) x +Cl - (H 2 O) y
NaCl Na + +Cl -
HCl+mH 2 O H + (H 2 O) x +Cl - (H 2 O) y
HCl H + +Cl -

Двухосновные
H 2 SO 4 , H 2 CO 3 , H 2 S, H 2 SiO 3
Одноосновные
HClO 4 , HNO 3 , HCl, HBr
Четырёхосновные
H 4 P 2 O 7 , H 4 SiO 4
Трёхосновные
H 3 PO 4 , H 3 BO 3
С точки зрения ТЭД, кислотами называются электролиты, которые в водном растворе диссоциируют на ионы водорода и ионы кислотных остатков.

HCl = H + + Cl -
HNO 3 = H + + NO 3 -
HClO 4 = H + + ClO 4 -
Кислоты – это электролиты, которые диссоциируют на катионы водорода и анионы кислотного остатка.

Na 2 SO 4 = 2Na + + SO 4 2-
AlCl 3 = Al 3+ + 3Cl -
Fe 2 (SO 4 ) 3 = 2Fe 3+ + 3SO 4 2-
С точки зрения ТЭД, средними солями называются электролиты, которые в водном растворе диссоциируют на ионы металла и ионы кислотного остатка..
 2 H 2 SO 3 H + + HSO 3 - Сильный электролит H 2 SO 4 H + + HSO 4 - 1 HSO 4 - H + + SO 4 2 - 2 1 2 H 2 SO 4 2 H + + SO 4 2 - Многоосновные кислоты диссоциируют ступенчато. Каждая последующая степень протекает хуже предыдущей. " width="640"
2 H 2 SO 3 H + + HSO 3 - Сильный электролит H 2 SO 4 H + + HSO 4 - 1 HSO 4 - H + + SO 4 2 - 2 1 2 H 2 SO 4 2 H + + SO 4 2 - Многоосновные кислоты диссоциируют ступенчато. Каждая последующая степень протекает хуже предыдущей. " width="640"
Электролит средней силы
H 2 SO 3 H + + HSO 3 - 1
HSO 3 - H + + SO 3 2- 2
1 2
H 2 SO 3 H + + HSO 3 -
Сильный электролит
H 2 SO 4 H + + HSO 4 - 1
HSO 4 - H + + SO 4 2 - 2
1 2
H 2 SO 4 2 H + + SO 4 2 -
Многоосновные кислоты диссоциируют ступенчато. Каждая последующая степень протекает хуже предыдущей.

Двухкислотные
Ca(OH) 2 , Ba(OH) 2 , Fe(OH) 2
Однокислотные
NaOH, KOH, NH 4 OH
Трёхкислотные
Fe(OH) 3 , Al(OH) 3 , Cr(OH) 3 ,
С точки зрения ТЭД, основаниями называются электролиты, которые в водном растворе диссоциируют на ионы металла и гидроксид ионы .

NaOH = Na + + OH -
Ba(OH) 2 = BaOH + + OH - → Ba 2+ + 2OH -
KOH = K + + OH -
Основания – это электролиты, которые диссоциируют на катионы металла и анионы гидроксогрупп

NaCl = Na + + Cl -
KNO 3 = K + + NO 3 -
Al 2 (SO 4 ) 3 = 2Al 3+ + 3SO 4 2-
Соли – это электролиты, которые диссоциируют на катионы металла или аммония NH 4 + и анионы кислотных остатков.

Классификация солей
средние
кислые
основные
Образованы катионами
металла и анионами
кислотного остатка
Кроме металла
и кислотного
остатка содержат гидроксогруппу
Кроме металла
и кислотного
остатка содержат
водород

NaHSO 4 Na + + HSO 4 - 1
HSO 4 - H + + SO 4 2 - 2
1 2
NaHSO 4 Na + + HSO 4 -
С точки зрения ТЭД, кислыми солями называются электролиты, которые в водном растворе диссоциируют на ионы металла , ионы кислотного остатка и образуют ионы водорода .

- Под действием тока положительные ионы движутся к катоду и называются катионы , а отрицательные – к аноду и называются анионы .

Ba(OH)Cl = BaOH + + Cl - 1
BaOH - Ba 2+ + OH - 2
1 2
С точки зрения ТЭД, основными солями называются электролиты, которые в водном растворе диссоциируют на ионы металла , ионы кислотного остатка и образуют гидроксид ионы.
 30% " width="640"
30% " width="640"
Не все электролиты в одинаковой мере диссоциируют на ионы
Слабые электролиты
3%
Электролиты средней силы
3% 30%
Сильные электролиты
30%

100%
100%
0
0
моль / л
100 0
График зависимости степени электролитической диссоциации от концентрации
График зависимости степени электролитической диссоциации от температуры
 30% Средние водорастворимые соли NaCl, K 2 SO 4 , Ba(NO 3 ) 2 итд; Гидроксиды щелочных и щелочноземельных металлов : LiOH – CsOH, Ca(OH) 2 – Ba(OH) 2 ,; Минеральные кислоты : H 2 SO 4 , HNO 3 , HClO 3 , HClO 4 , HBrO 3 , HJO 3 , HCl, HBr, HJ " width="640"
30% Средние водорастворимые соли NaCl, K 2 SO 4 , Ba(NO 3 ) 2 итд; Гидроксиды щелочных и щелочноземельных металлов : LiOH – CsOH, Ca(OH) 2 – Ba(OH) 2 ,; Минеральные кислоты : H 2 SO 4 , HNO 3 , HClO 3 , HClO 4 , HBrO 3 , HJO 3 , HCl, HBr, HJ " width="640"
Сильные электролиты
30%
- Средние водорастворимые соли NaCl, K 2 SO 4 , Ba(NO 3 ) 2 итд;
- Гидроксиды щелочных и щелочноземельных металлов : LiOH – CsOH, Ca(OH) 2 – Ba(OH) 2 ,;
- Минеральные кислоты : H 2 SO 4 , HNO 3 , HClO 3 , HClO 4 , HBrO 3 , HJO 3 , HCl, HBr, HJ

Электролиты средней силы
3% 30%
H 3 PO 3 , H 3 PO 4 , H 4 P 2 O 7 , H 2 SO 3 , HF, HClO 2 , Fe(OH) 2 ,

Слабые электролиты
3%
- Органические кислоты: HCOOH, CH 3 COOH, C 2 H 5 COOH
- Минеральные кислоты: HNO 2 , HClO, H 2 CO 3 , H 2 SiO 3 , H 3 BO 3 , H 3 PO 3 , H 2 S
- Гидроксиды малоактивных металлов: Cu(OH) 2 , Fe(OH) 3 , Al(OH) 3 , Cr (OH) 3 ,
- Гидроксид аммония: NH 4 OH

- Свойства растворов электролитов определяются свойствами тех ионов, которые они образуют при диссоциации.

Условия протекания реакции ионного обмена
Реакции в растворах электролитов протекают до конца если:
- Образуется или растворяется осадок;
- Выделяется газ;
- Образуется малодиссоциирующее вещество (например Н 2 О)

Образование
осадка



Образование H 2 O
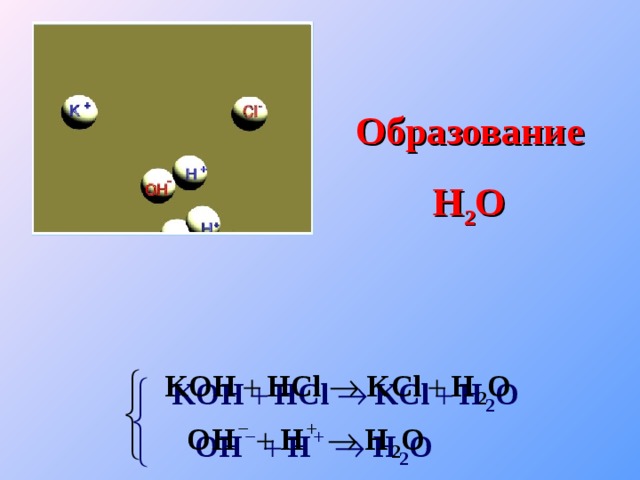
Образование
Н 2 О







Алгоритм составления ионных уравнений

Ва (ОН) 2 + 2Н 3 РО 4 =
AgNO 3 + NaCl =
BaCl 2 + Na 2 SO 4 =
NH 4 Cl + NaOH =
K 2 CO 3 + 2HNO 3 =
Na 2 CO 3 +H 2 SO 4 =
NaOH + HCl =
CuSO 4 + NaOH =
K 2 CO 3 + HCl =
H 2 SO 4 + BaCl 2 =























 2 H 2 SO 3 H + + HSO 3 - Сильный электролит H 2 SO 4 H + + HSO 4 - 1 HSO 4 - H + + SO 4 2 - 2 1 2 H 2 SO 4 2 H + + SO 4 2 - Многоосновные кислоты диссоциируют ступенчато. Каждая последующая степень протекает хуже предыдущей. " width="640"
2 H 2 SO 3 H + + HSO 3 - Сильный электролит H 2 SO 4 H + + HSO 4 - 1 HSO 4 - H + + SO 4 2 - 2 1 2 H 2 SO 4 2 H + + SO 4 2 - Многоосновные кислоты диссоциируют ступенчато. Каждая последующая степень протекает хуже предыдущей. " width="640"







 30% " width="640"
30% " width="640"

 30% Средние водорастворимые соли NaCl, K 2 SO 4 , Ba(NO 3 ) 2 итд; Гидроксиды щелочных и щелочноземельных металлов : LiOH – CsOH, Ca(OH) 2 – Ba(OH) 2 ,; Минеральные кислоты : H 2 SO 4 , HNO 3 , HClO 3 , HClO 4 , HBrO 3 , HJO 3 , HCl, HBr, HJ " width="640"
30% Средние водорастворимые соли NaCl, K 2 SO 4 , Ba(NO 3 ) 2 итд; Гидроксиды щелочных и щелочноземельных металлов : LiOH – CsOH, Ca(OH) 2 – Ba(OH) 2 ,; Минеральные кислоты : H 2 SO 4 , HNO 3 , HClO 3 , HClO 4 , HBrO 3 , HJO 3 , HCl, HBr, HJ " width="640"



























