Тест "Строение атома. Периодическая система. Электронные схемы и формулы"
Инструкция по проведению теста: внимательно прочитайте вопрос, выберите правильные ответы.
Тест:
1. Определите формулу основания данного элемента Na (Na2O, NaOH, NaO, Na(OH)2 ).
2. Выберите формулу оксида хлора: ( ОCl2, ClОН, Cl2О7 ).
3. Найдите из перечисленных элементов инертные газы: ( He, Ne, F, Cl, Li, Na).
4. Продолжите фразу "атом состоит из..."
а) положительно заряженных электронов и отрицательно заряженного ядра;
б) положительно заряженных протонов и нейтрально заряженных нейтронов;
в) положительно заряженного ядра и отрицательно заряженных электронов;
г) положительных и отрицательных ионов.
5. Выберите, что соответствует количеству электронов у химического элемента в периодической системе:
а) порядковый номер элемента в периодической системе;
б) группа в которой находится химический элемент;
в) период в котором находится химический элемент;
г) по атомной массе химического элемента.
6. Определить химический элемент, который может иметь 8 протонов: (Li, О, C, N).
7. Определите химический элемент, который находится в 3 группе, 3 периода и имеет 14 нейронов: (Si, Na, Mg, Al).
8 . Выберите, какой тип орбитальней изображен на рисунке: (s- орбиталь, p-орбиталь, d-орбиталь, f-орбиталь).
. Выберите, какой тип орбитальней изображен на рисунке: (s- орбиталь, p-орбиталь, d-орбиталь, f-орбиталь).
9. Изотопы — атомы одного химического элемента с:
а) разной атомной массой;
б) имеющие равное число электронов (е), протонов (p), но разное число нейтронов (n);
в) имеющие равное число электронов (е), протонов (p), нейтронов (n).
10. Число энергетических уровней в атоме равно:
а) номеру элемента;
б) номеру группы;
в) номеру периода.
11. У элементов 2 периода заполняется второй уровень, который максимально вмещает:
а) 2 электрона;
б) 4 электрона;
в) 6 электронов;
г) 8 электронов.
1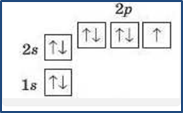 2. Выберите химический элемент, соответсвующий графической формуле:
2. Выберите химический элемент, соответсвующий графической формуле:
(Be, F. Fe, P).
13. Выберите химический элемент в электронной формуле:

(S. Si, Mg, Al).
14. Определить элемент по схеме электронного строения атома:

а) Cl;
б) S;
в) F.
15.Число валентных электронов равно:
а) номеру группы;
б) номеру элемента;
в) номеру периода.







 . Выберите, какой тип орбитальней изображен на рисунке: (s- орбиталь, p-орбиталь, d-орбиталь, f-орбиталь).
. Выберите, какой тип орбитальней изображен на рисунке: (s- орбиталь, p-орбиталь, d-орбиталь, f-орбиталь).  2. Выберите химический элемент, соответсвующий графической формуле:
2. Выберите химический элемент, соответсвующий графической формуле: 











