«Алюминий как химический элемент и простое вещество. Физические и химические свойства алюминия. Применение алюминия»
Учитель химии
высшей категории Жмака Л.В
Цели урока:
Познакомиться с химическим элементом – алюминием и образованным им
простым веществом.
Продолжить конкретизацию знаний учащихся о свойствах металлов на примере
алюминия, формировать умения давать характеристику элемента по его
положению в периодической системе химических элементов Д.И. Менделеева, на
основе строения атома объяснять физические и химические свойства металла,
прогнозировать его применение.
Продолжать формирование умений наблюдать, сравнивать, делать выводы.
Развивать познавательную деятельность учащихся.
Тип урока – медиа урок – усвоение новых знаний
Оборудование урока: периодическая система химических элементов, алюминиевая фольга, алюминиевая проволока, коллекции «металлы и сплавы, алюминий и его сплавы»
Ход урока
Активизация опорных знаний
Беседа с классом: что мы знаем об алюминии. В процессе беседы учащиеся рассказывают об алюминии, где применяется. Но главный вопрос, который нужно поставить как проблемный «Почему этот металл называют металлом века» Какие свойства алюминия являются наиболее важными и находят применение в народном хозяйстве.
(раскрыть цель урока)
Изучение нового материала
Нахождение элемента в периодической системе (слайд 1)

Нахождение в природе (слайд 2)
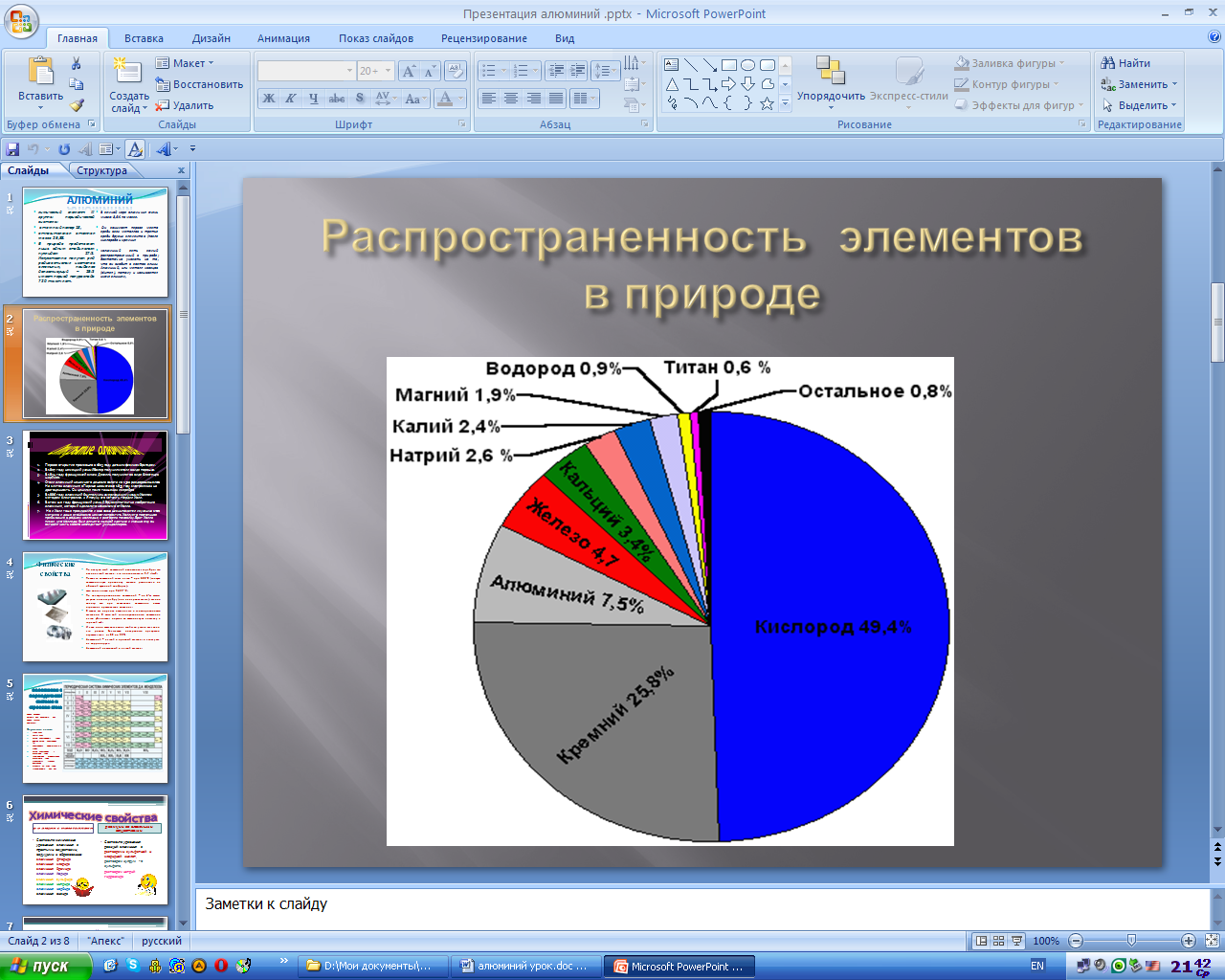
Задание I.Рассмотрите диаграмму «Распространение элементов в природе». Определите, какое место занимает Al среди других элементов.
Задание II. Рассмотрите образцы природных соединений, сравните их по твердости, прочности, цвету. Запишите формулы и названия природных соединений алюминия.
Открытие алюминия (слайд 3)

Задание. Познакомьтесь с историей открытия элемента.
Физические свойства алюминия.
Лабораторный опыт
Рассмотрите выданные образцы металла.
Ответьте на вопросы: « Какими свойствами обладает Al? Что привлекло внимание огромного круга промышленников, учёных, государственных деятелей?».
Сделайте вывод. Алюминий – металл серебристо- белого цвета, лёгкий ( q- 2,7 г./ см.3), плавится при температуре 6600С. обладает хорошей ковкостью, пластичностью, электрической проводимостью и теплопроводностью, легко поддаётся обработке, образует лёгкие и прочные сплавы.
Учащиеся обобщают свои выводы и просматривают (слайд 4)

Положение элемента в периодической системе и строение атома
В помощь слайд (5)

Задание I Учащиеся выполняют самостоятельно задания по основным вопросам характеристики химического элемента
Задание II. Сделайте вывод об активности элемента и прогноз на химические свойства.
Химические свойства алюминия.
В помощь (слайд 6,7)


Учащиеся дали прогноз на активность химического элемента и его свойства -
способность взаимодействовать с неметаллами (свойство типичного металла)
Задание I Просмотрите слайд и убедитесь в своих знаниях. Напишите уравнения,
отражающие химические свойства металла алюминия.
Задание II Чем обусловлено проявление алюминием амфотерных свойств. Составьте
уравнения реакций алюминия с хлоридной кислотой и калием гидроксидом.
Закрепление знаний
Беседа с учащимися на закрепление химических свойств.
Можно ли варить борщ в алюминиевой посуде?
Какую роль для металла выполняет оксидная пленка алюминия?
Почему, когда нагревать алюминиевую проволоку над пламенем, алюминий не капает?
Почему при комнатной температуре алюминиевая проволока не изменяет своего цвета?
Почему алюминиевую посуду нельзя мыть содой?
Известно, что концентрированные сульфатная и нитратная кислоты перевозятся в алюминиевых цистернах. Почему?
Вы помните, как горят бенгальские свечи, как вы думаете, какое вещество в них присутствует?
Обобщение знаний
Беседа с учащимися.
Рассмотрев свойства алюминия, ответьте вопрос: «Почему алюминий называют металлом будущего?»
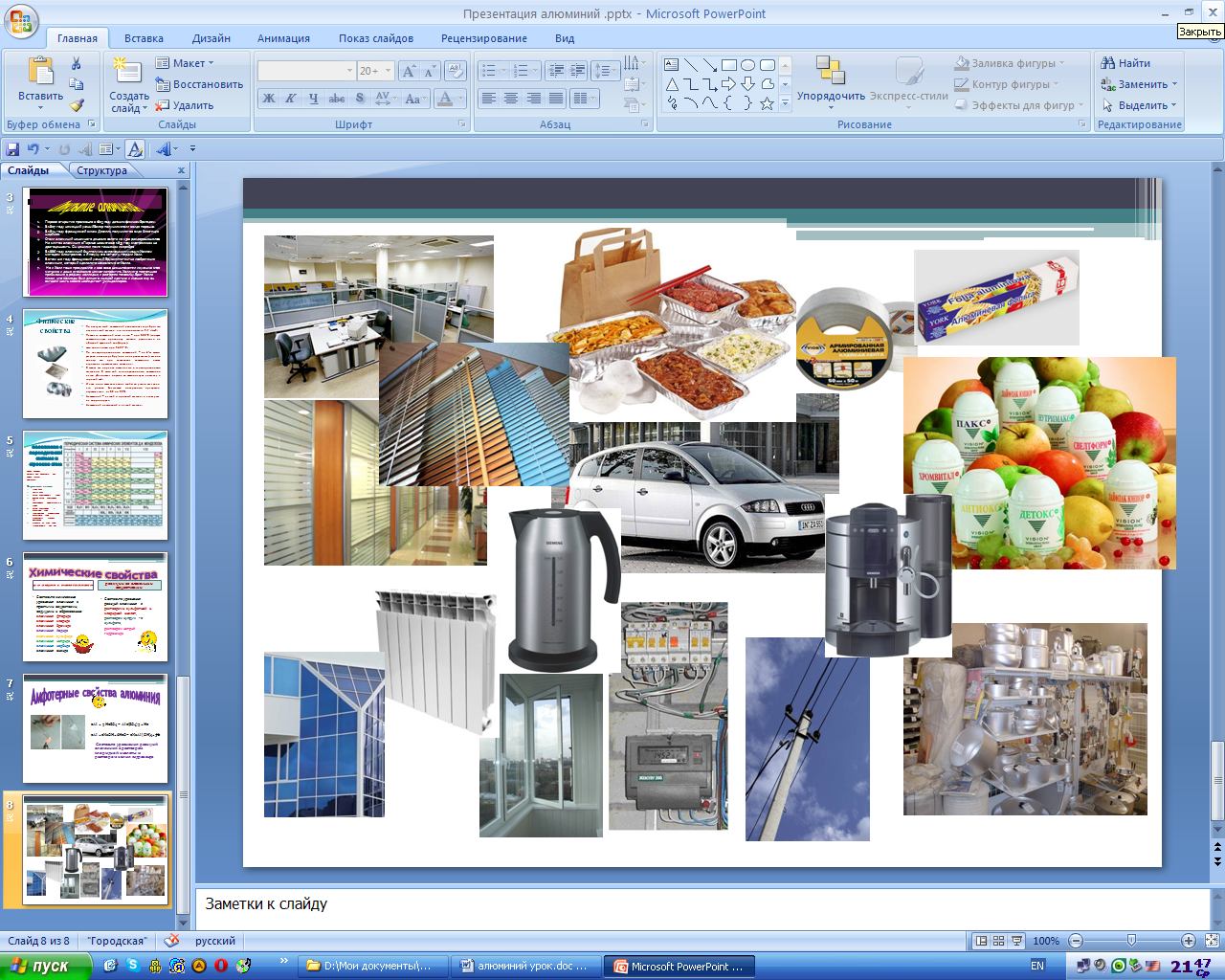
Для закрепления знаний на применение алюминия посмотреть (слайд 8)
и ответить на вопрос, какие направления применения алюминия вы выделите (электрика, дизайн, тара и упаковка, фармацевтика, строительство, транспорт, машиностроение)
Подведение итогов
V. Домашнее задание: