УРОК- ИГРА В 8 КЛАССЕ.
Тема: «ТИПЫ ХИМИЧЕСКИХ РЕАКЦИЙ».
Цель урока: повторить классификацию веществ, типы химических реакций и признак их классификации, научить учащихся применять полученные знания о типах химических реакций на практике – составлять уравнения химических реакций, определять типы химических реакций.
Задачи:
Образовательные: систематизировать знания учащихся о классификации веществ, типах химических реакций, продолжить формирование умений наблюдать, записывать уравнения и предвидеть продукты химических реакций, продолжить формирование умения при написании реакций обмена, применения условий течения реакций между растворами до конца, подготовить учащихся к пониманию обратимых и необратимых реакций, теории электролитической диссоциации.
Развивающие: совершенствовать умения школьников при составлении химических уравнений, при выполнении лабораторных опытов; совершенствовать умения учащихся сравнивать и обобщать; развивать память, устойчивое внимание, самостоятельное мышление, умение слушать и слышать другого человека; развивать аналитическое мышление.
Воспитательные: продолжить формирование диалектико-материалистического мышления учащихся.
Форма учебного процесса: классный урок.
Тип урока: урок обобщения и систематизации знаний учащихся.
Вид урока: урок- игра.
Оборудование: таблица «Угадай слово», шифровки, карточки с заданиями, лист для суперигры «Крестик - Нолики».
На столе учителя: разбавленный раствор серной кислоты, раствор гидроксида натрия, фенолфталеин, штатив с пробирками.
На столах учащихся: штатив с 3-мя пронумерованными пробирками (№№ 1, 2, 3), растворы разбавленной серной кислоты, хлорида магния, карбоната натрия, гидроксида натрия, фенолфталеин; схема-конспект урока, условные знаки поездов (красный кружок и зеленый треугольник); «Наградной лист», анкеты для учащихся.
Химия – это область чудес, в ней скрыто счастье человечества, величайшие завоевания разума будут сделаны именно в этой области. (М.Горький)
ХОД УРОКА.
Организационный момент.
Приветствие.
Сообщение темы, цели урока, мотивация учения учащихся.
Все что нас окружает состоит из веществ. Кажется, что они живут своей жизнью, таинственной и непостижимой. Взаимодействуя, они изменяют свои свойства и состав. Без химических реакций невозможна жизнь и все многообразие веществ. И задача человека, изучив этот мир, постараться использовать полученные знания во благо.
Сегодня мы продолжим знакомство с этим удивительным и волшебным миром.
Учитель: Чтобы узнать о чём мы будем говорить, отгадайте загадку:
Она идет,
она прошла!
Никто не скажет,
что пришла!
| Учащиеся: Учитель: какие ассоциации возникают у вас , когда слышите слово «реакция» | - Химическая реакция Р Е А К Ц И Я |
| Учитель: | - Тема нашего урока «Типы химических реакций» |
|
Учитель: | - Сегодня на уроке мы должны систематизировать все полученные вами знания о химических реакциях, их типах и условиях протекания, для того, чтобы в дальнейшем вы могли правильно описывать химические свойства веществ, а также предсказывать возможности их получения, ведь нас с вами окружают вещества и постоянно происходящие с ними изменения, кроме того, хорошо овладев этой темой, для вас не составит труда осуществлять цепочки химических превращений, решать всевозможные химические задачи.
- А для этого мы с вами совершим восхождение к вершинам знаний. - Чтобы гору перейти и к вершине нам дойти Нужно многое постичь, надо много сил вложить: Не бояться отвечать и вопросы задавать Уравнения химических реакций писать, Знать, как их отличать, Все задания выполнять, друг у друга проверять. Цель свою тогда достигнем – О типах реакций все постигнем!
- Девиз нашего урока – «Достичь вершины – не свалиться в пропасть!»
- Итак, в путь! Желаю удачи! - Чтобы достичь цели, т.е. добраться до вершины горы, мы должны преодолеть 5 этапов: Шифровка. Угадай слово. Реши проблему Химический букет. Химический снегопад. |
Обобщение и систематизация понятий.
Этап – «Шифровка». (работа парами)
| Учитель: | - Первый этап называется «Шифровка», и т.к. мы только начинаем выполнять восхождение в горы, то этот этап пройдем парами. На каждой парте лежит шифровка. Посмотрите на нее внимательно. |
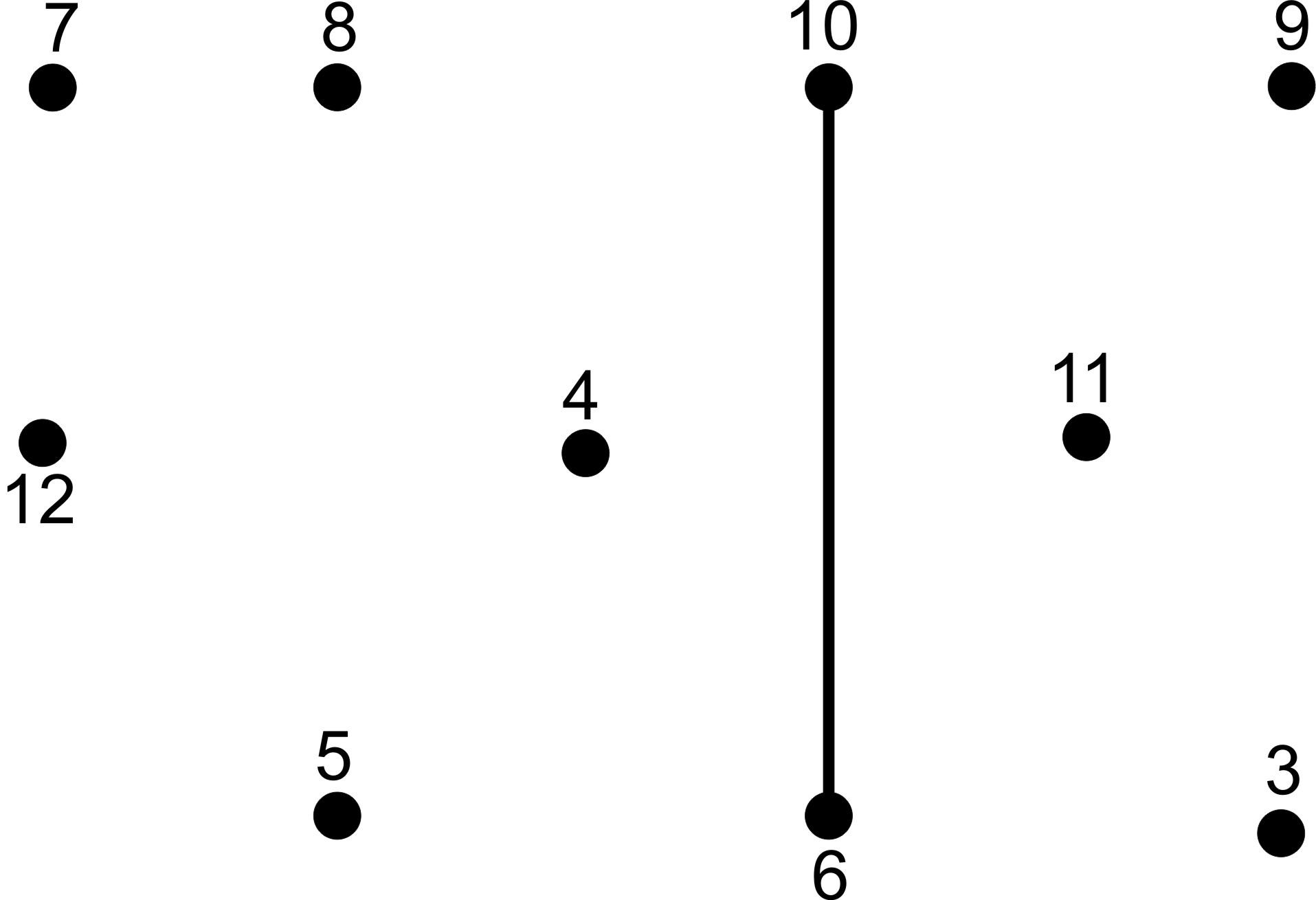
| Задание: | в верхней части листа записаны уравнения химических реакций, в нижней – беспорядочно расставлены точки с цифрами; каждой цифре соответствует сумма коэффициентов в вышенаписанных уравнениях реакций. Ваша задача: расшифровать замаскированный химический элемент. Для этого необходимо по порядку уравнивать химические реакции, подсчитывать сумму коэффициентов в уравнении, находить соответствующие точки и последовательно, с помощью маркеров, соединять их друг с другом. Если вы правильно выполните задание, то узнаете, какой химический элемент спрятался за цифрами. |
Шифровка № 1.
|
Ba + O2 → BaO
Fe(OH)3 + HCl → FeCl3 + H2O
Na + S → Na2S
Fe + O2 → Fe3O4 |
5
8
4
6
| 
|
Шифровка № 2.
|
C + O2 → CO2
CH4 → C2H2 + H2
Ca + HCl → CaCl2 + H2
K + S → K2S |
3
6
5
4 | 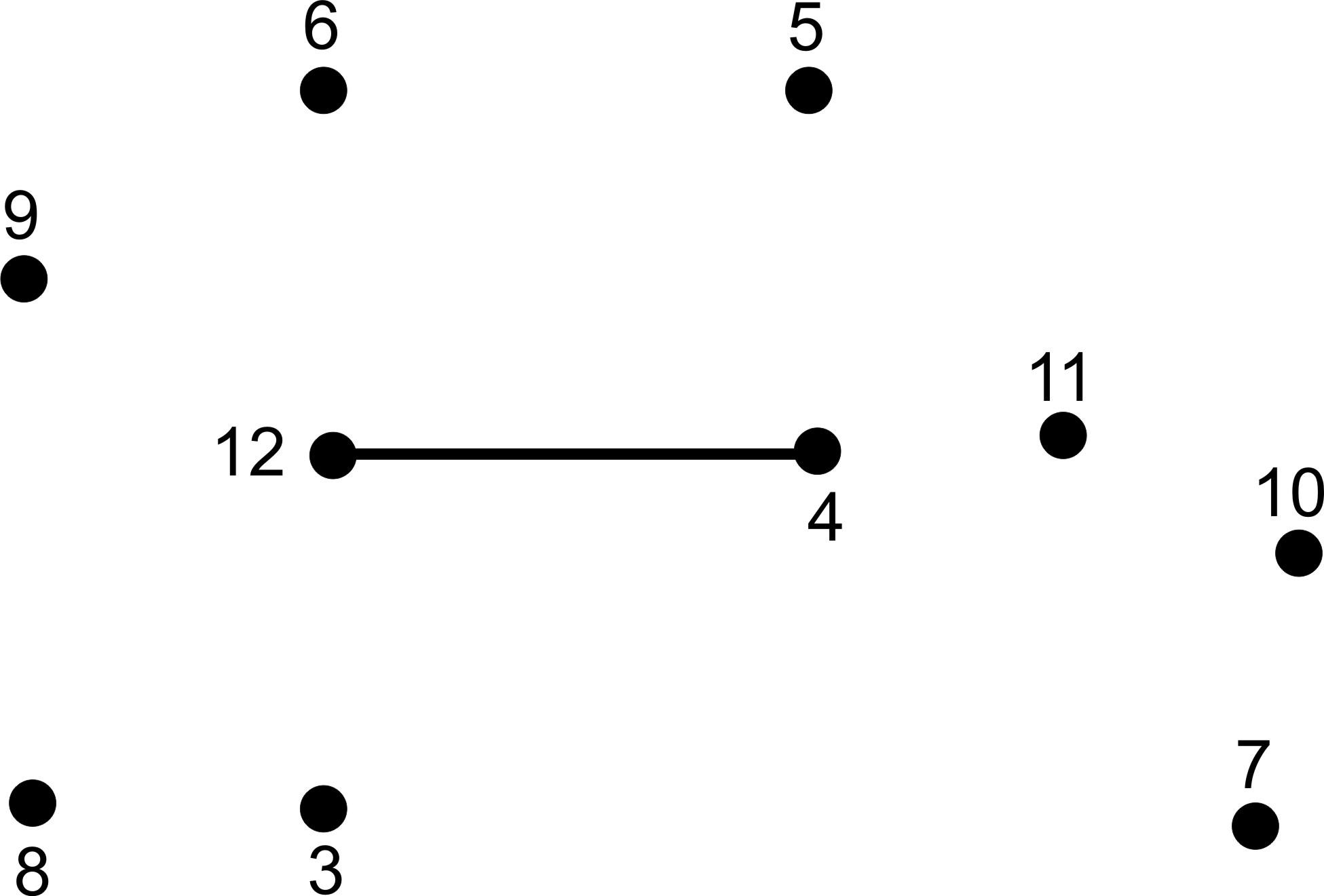
|
Шифровка № 3.
|
HNO3 + CaO → Ca(NO3)2 + H2O
Fe + O2 → Fe2O3
BaO + H2SO4 → BaSO4 + H2O
Fe + Cl2 → FeCl3 |
5
9
4
7 | 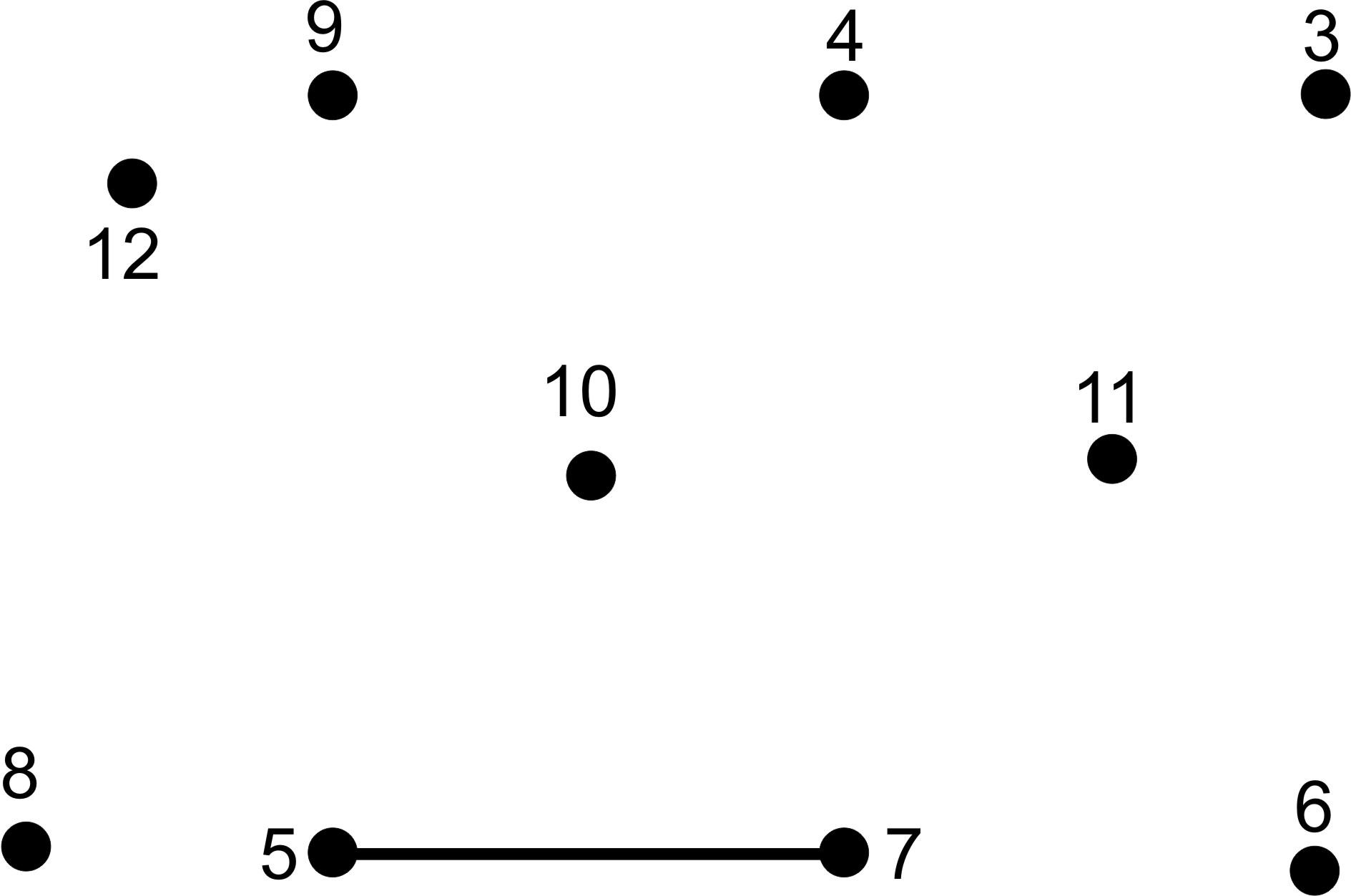
|
(проверка заданий: Шифровка № 1 – N, № 2 – P, № 3 – O/
| Учитель: | - Итак, первый этап позади.
|
Этап – «Угадай слово».
| Учитель: | - А теперь перейдем ко второму этапу.
- Химических реакций известно в мире много И каждая в отдельности важна, поверьте мне. Реакции мы делим на типы очень строго Какие это типы? Поведайте вы мне. |
| Учащиеся: | - 4 типа химических реакций – реакции соединения, разложения, замещения, обмена.
|
| Учитель:
| - Что называется реакцией соединения, разложения, замещения, обмена? |
|
| Учащиеся: | отвечают на поставленные вопросы.
|
|
| Учитель: | - Давайте выполним следующее задание.
|
|
| Задание: | к какому типу химических реакций нужно отнести уравнения, приведенные в таблице. Таблица «Угадай слово» есть в схеме – конспекте урока. Необходимо правильно определить тип химической реакции, найти соответствующую букву, из букв сложить слово. |
|
Таблица «Угадай слово».
| Уравнения реакций | Типы химических реакций |
| соеди- нения | разло- жения | заме- щения | обмена |
| Mg + 2HCl → MgCl2 + H2 | Б | В | П | З |
| 2Fe(OH)3 → Fe2O3 + 3H2O | Г | И | К | Д |
| 2Ca + O2 → 2CaO | С | Ж | С | Ф |
| K3PO4 + 3AgNO3 → Ag3PO4↓ + 3KNO3 | Н | У | Т | Ь |
| 2HgO → 2Hg + O2 | А | М | Р | П |
| Br2 + 2KI → 2KBr + I2 | Ш | Л | О | И |
(1 человек работает у доски, остальные на своих местах. Ответ: ПИСЬМО)
| Учитель: | - Ребята поднимите сигнальные карточки вверх: у кого получилось слово «ПИСЬМО» - зеленые треугольники. - Друзья, вы правильно определите типы химических реакций, и мы получили название третьего этапа нашего путешествия.
- Мы преодолели второй этап. 3этап- Реши проблему. №1: Жилец из квартиры №26 решил помочь освободиться жильцу из квартиры №29 из его хлорида, но сам попал в западню. Почему? Чтобы ответить на этот вопрос, проведем опыт. Опустим в пробирку с раствором хлорида меди (II) железный гвоздь (на нитке). Соблюдаем правила техники безопасности при работе в химической лаборатории (беседа по Т.Б.) Напишите уравнения реакции,определите тип реакции и поставьте коэффициенты. №2:Царь зовет к себе Стрельца – удалого молодца, И дает ему поручение государственного значения: «Чтоб я стал опять богат, нужен мне алюминия сульфид. Ночь даю тебе подумать, утром буду ждать доклад. Не смогешь – кого винить? Должен я тебя казнить. Запиши себе названье, чтоб со страху не забыть». Напишите в тетради формулу сульфида алюминия, уравнения реакции его получения. Укажите тип реакции. №3 О каких веществах идет речь в отрывке из стихотворения С.Щипачева «Читая Менделеева»? «Ты знаешь газ легчайший – водород. В соединенье с кислородом – это Июньский дождь от всех своих щедрот, Сентябрьские туманы на рассвете!» Напишите формулы данных веществ. Составьте уравнение реакции разложения. Назовите каждое вещество.
|
|
|
|
№4
|
| - Основание и кислота – Два непримиримых врага, Сразу вступают в реакцию, Название которой – нейтрализация. Соль и Н2О нам получить дано.
- Но сначала…… |
| «Хамелеон» |
|
| Учитель: | - Ребята, сейчас вы увидели животного, вы узнали его? Что вы можете о нем рассказать?
|
| Учащиеся: | - Хамелеон, изменяет свою окраску от внешних условий.
|
| Учитель: | - А как вы думаете, почему я его вам сейчас показал? Какие химические вещества, подобно хамелеону меняют свою окраску? Как они называются?
|
| Учащиеся : | - Индикаторы – лакмус, фенолфталеин, метиловый оранжевый.
|
| Учитель: | - А теперь вернемся к реакции нейтрализации и я продемонстрирую ее вам, а чтобы вам наглядно была видна эта реакция, я буду использовать индикатор фенолфталеин. Фенолфталеин в нейтральной, а также в кислой среде – бесцветный, а в щелочной –малиновый.
|
| Демонстрация: | NaOH + фенолфталеин + H2SO4 → обесцвечивание раствора Химик правила обмена не забудет никогда: В результате – непременно будет газ или вода, Выпадет осадок – вот тогда порядок!
|
| Учащиеся: | Записывают уравнение реакции.
|
| Учитель: | - Итак, третий этап позади, - Но прежде чем, мы перейдем к 4 этапу, я предлагаю немного отдохнуть и устроить «Стрельбу глазами».
|
| Задание: | «Стрельба глазами». В периодической системе найдите самый сильный элемент – неметалл. (F) Переведите свой взгляд влево, на элемент, стоящий в том же периоде в 3 группе. (B) Переведите взгляд вниз, на самый сильный металл. (Fr) Переведите взгляд вверх и вправо, на элемент, образующий вещество, которое поддерживает горение. (O) Переведите взгляд вниз и влево, на элемент, который образует металл, содержащееся в градусниках. (Hg) Переведите взгляд вверх и вправо, на элемент с относительной атомной массой 35,5. (Cl) Переведите взгляд вниз и влево, на элемент, давший группе элементов название «лантаноиды». (La) Переведите свой взгляд вверх и вправо, на самый электроотрицательный элемент. (F) Переведите свой взгляд вниз и влево, на элемент, который образует драгоценный металл желтого цвета. (Au)
|
| Учитель: | - Мы немного отдохнули, впереди нас ждет четвертый этап. |
Этап – Химический букет.
В форме цветов записаны формулы веществ:
| Формула | АВ | А | В | СД | С | Д | СВ | АД |
| Количество цветков | 4 | 4 | 4 | 4 | 4 | 4 | 4 | 4 |




АВ СД СВ АД
















А В С Д












| Учитель: | - На химической поляне Чудо – формулы цветут Соберем давайте с вами Из цветов букеты тут.
|
| Задание: | из химических цветов собрать соответствующие букеты химических реакций.
|
|
| (по одному ученику приглашать к доске составлять «букеты», остальные на своих местах записывают схемы реакций в своих схемах – конспектах) |
На доске и в схемах – конспектах записано:
| Название «букета» | Уравнения из химических «цветов» |
| Реакция соединения |
|
| Реакция разложения |
|
| Реакция замещения |
|
| Реакция обмена |
|
| Учитель: | - Вот и четвертый этап позади. |
Установление общих закономерностей.
| Учитель: | - Друзья! Мы почти достигли цели. Впереди последний этап – Химический снегопад. |
5. Этап – «Химический снегопад»(или « К вершинам гор»)
| Учитель: | - Снег идет, и снег кружится Он ковром везде ложится Приглашаю всех я вас Поиграть в снежки сейчас, (Есть у нас большой завод –
Он продукцию дает.
А над ним труба дымит –
Небо синее коптит.
Жить под ней - сплошная мука!
Но поможет нам наука:
Чтобы снять противогаз,
Обезвредить нужно газ.) - Ребята, мы с вами сейчас повторили и обобщили тему «Типы химических реакций» и я предлагаю вам оценить себя с помощью снежинок. - Но снежки, друзья мои, у нас необыкновенные – химические. На снежинках разного цвета написаны задания разной степени трудности. Вы должны выбрать для себя задания либо на оценку «3», либо – на «4», либо – на «5». Тексты с заданиями у вас записаны в схемах-конспектах. |
«Синяя снежинка» - задание на «3»
Расставьте коэффициенты в уравнениях химических реакций, укажите типы химических реакций.
| Уравнение реакции | Тип химической реакции |
| а) Al + Cr2O3 → Al2O3 + Cr |
|
| б) Li + N2 → Li3N |
|
| в) K2S + CuCl2 → CuS↓ + KCl |
|
| г) N2O → N2 + O2 |
|
«Голубая снежинка» - задание на «4»
Допишите уравнения реакций, расставьте коэффициенты, укажите типы химических реакций.
| Уравнение реакции | Тип химической реакции |
| а) Ca + Cl2 → |
|
| б) HNO3 + Cu(OH)2 → |
|
| в) Mg + TiCl4 → |
|
| г) AgBr → |
|
«Белая снежинка» - задание на «5»
Допишите практически осуществимые уравнения реакций, расставьте коэффициенты, укажите типы химических реакций.
| Уравнение реакции | Тип химической реакции |
| а) Mg + O2 → |
|
| б) Fe3O4 + Al → |
|
| в) H3PO4 + HCl → |
|
| г) Ba(OH)2 + H2SO4 → |
|
| д) H2O → |
|
| Учитель: | - Кто желает у доски выполнить задания на «5», «4», «3»? (желающие учащиеся работают у доски, остальные на своих местах в схеме конспекте)
|
|
| Учитель: | - Вот и все!
- Мы достигли цели! Кто-то из вас пришел к вершине «горы» без поражений, а кто-то был почти у края пропасти. Теперь давайте посмотрим, что же за сюрприз нас ожидает. (на вершине горы – 2 конверта «СЮРПРИЗ», «СУПЕРПРИЗ»)
(вскрыть конверт с «Сюрпризом», в котором находятся кружочки с изображением отметок «3», «4», «5») - Ребята, покажите свои наградные листы. А теперь обмениваем заработанные вами аурики на оценки: 3 аурика – одна «5»; 2 аурика – одна «4». (раздать оценки)
|
|
| Учитель: | - А теперь, ребята, вспомните, какие слова были произнесены мною в самом начале урока?... «на горе вас ждет сюрприз, там еще и суперприз…»
- Итак, суперигра! Принять участие в ней может тот, кто имеет не менее одной пятерки.
- Суперприз на горе, Кто рискнет своей пятеркой, Тот получит сразу две!
(вскрыть пакет «Суперприз», прочитать задание. |
|
|
|
| Задание СУПЕРИГРЫ: | суперигра – «Крестик-нолик»; за 30 секунд необходимо найти выигрышный путь, состоящий из уравнений реакций замещения |
| Fe2O3 + H2 → H2O + Fe | NO2 + H2O + O2 → HNO3 | AgNO3 → Ag + NO2 + O2 |
|
| Cl2 + KI → KCl + I2 | Na2SO4 + BaCl2 → BaSO4↓ + NaCl | Zn + O2 → ZnO |
|
| Al + HCl → AlCl3 + H2↑ | Cu(OH)2 → CuO + H2O | HCl + Zn → ZnCl2 + H2 |
|
Домашнее задание.
| Учитель:
| - В ваших схемах – конспектах записано домашнее задание, которое вы должны выполнить к следующему уроку. Если вас устраивает оценка «3», то вы выполняете задание на «3», если «4», то соответственно – на «4», и тоже самое на «5» |
В схемах-конспектах:
Ты - молодчина! И в это поверь:
Открыта тобой в мир химии дверь.
Надеемся все мы, что лет через пять,
Прекрасным ученым сможешь ты стать.
Домашнее задание:
Задание на «3»
Расставьте коэффициенты в уравнениях химических реакций, укажите типы химических реакций.
| Уравнение реакции | Тип химической реакции |
| а) Al + O2 → Al2O3 | реакция |
| б) MnO2 + H2 → Mn + H2O | реакция |
| в) H2O2 → H2 + O2 | реакция |
| г) HNO3 + Fe(OH)3 → Fe(NO3)3 + H2O | реакция |
Задание на «4»
Допишите уравнения реакций, расставьте коэффициенты, укажите типы химических реакций.
| Уравнение реакции | Тип химической реакции |
| а) AgI → | реакция |
| б) MgO + H2SO4 → | реакция |
| в) Al + HCl → | реакция |
| г) Na + Cl2 → | реакция |
Задание на «5»
Допишите практически осуществимые уравнения реакций, расставьте коэффициенты, укажите типы химических реакций.
| Уравнение реакции | Тип химической реакции |
| а) HNO3 + Mg(OH)2 → | реакция |
| б) FeCl3 + Zn → | реакция |
| в) CH4 → | реакция |
| г) KOH + Ca(OH)2 → | реакция |
| д) Ba + O2 → | реакция |
Подведение итогов.
| Учитель: | - Друзья, сегодня на уроке мы систематизировали ваши знания по теме «Типы химических реакций». И я думаю, что в дальнейшем вам не составит труда описывать химические свойства веществ, осуществлять цепочки химических превращений, решать задачи. - Спасибо вам за хорошую, плодотворную и интересную работу. - И чтобы узнать ваше мнение о сегодняшнем уроке, я прошу вас заполнить анкеты, лежащие на ваших столах. Анкета для учеников. Уважаемый коллега! Ответь, пожалуйста, на нижеперечисленные вопросы. Постарайся, чтобы твои ответы были искренними, честными и полными.
Твое отношение к сегодняшнему уроку (выбери вариант ответа): а) отличный, интересный, захватывающий; б) хороший, содержательный, заставляющий работать; в) нормальный обычный; г) скучный, работа без интереса; д) бесполезный, совсем не интересный. е) твой вариант ответа ____________________________________ ________________________________________________________
Вспомни тему урока. ________________________________________________________
Какая цель стояла перед тобой на уроке. ________________________________________________________ ________________________________________________________
Каков был план урока. ________________________________________________________ ________________________________________________________
Какие события, факты, закономерности, формулы, явления, правила ты усвоил на уроке. ________________________________________________________ ________________________________________________________ ________________________________________________________
Чему новому ты научился на уроке. ________________________________________________________ ________________________________________________________ ________________________________________________________
Какие были главные мысли на уроке? ________________________________________________________ ________________________________________________________ ________________________________________________________
Какие ранее полученные знания ты использовал на уроке. ________________________________________________________ ________________________________________________________ ________________________________________________________
Какую оценку за работу на уроке ты бы поставил себе? ________
Какую оценку за работу на уроке ты бы поставил учителю? ____
Спасибо за сотрудничество! |
- 12 -

































