Урок 59 8 класс
Тема: Распространение электронов по энергетическим уровням
Задачи урока:
1. Научиться распределять электроны по энергетическим уровням
2. Выучить закономерность размещения электронов по энергетическим уровням.
3. Изучить основные понятия.
Ход урока
1. Ознакомится с параграфом 53
2. Ребята, откройте свои тетради и запишите:
22 апреля
Домашняя работа
Распределение электронов по энергетическим уровням
Электрон вращается вокруг ядра атома с невообразимой скоростью. Так, за 1 секунду он делает столько оборотов вокруг ядра атома, сколько оборотов делает пропеллер самолета вокруг оси за 5–5,5 лет непрерывной работы двигателя. Пропеллер самолета образует «облако», находящееся в одной плоскости, а электрон образует объемное облако – электронное облако, форма и размер которого зависят от энергии электрона.
Если обозначить точками все вероятные места нахождения электрона в атомном пространстве за некоторое время, то совокупность этих точек будет представлять собой электронное облако.
Электронное облако – это модель, которая описывает состояние (движение) электрона в атоме.
Электронное облако не имеет строго очерченных границ и плотность его неравномерна.
Часть атомного пространства, в котором вероятность нахождения электрона наибольшая (~90%), называется орбиталью.
Таблицу переносим в тетради!
| Виды электронных орбиталей | Форма орбитали в пространстве | Количество орбиталей в атоме. Условное обозначение орбитали – клетка:
|
| s – орбиталь (электронное облако s – электрона) | 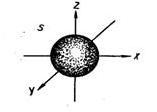
сфера (шар) | Электронное облако такой формы может занимать в атоме одно положение (условное обозначение) |
| p – орбиталь (электронное облако p – электрона) | гантель (восьмёрка) | Электронное облако такой формы может занимать в атоме три положения вдоль осей координат пространства x, y и z. (условное обозначение)
|
| d – орбиталь (электронное облако d – электрона) | четырёхлепестковая форма | Все d-орбитали (а их может быть уже пять) одинаковы по энергии, но по-разному расположены в пространстве. Да и по форме, напоминающей перевязанную лентами подушечку, одинаковы только четыре.
А пятая - вроде гантели, продетой в бублик. (условное обозначение) |
| f – орбиталь (электронное облако f – электрона) | сложная форма | Электронное облако такой формы может занимать в атоме семь положений. (условное обозначение) |
Условное обозначение электрона – стрелка, направленная вверх ↑ (электрон вращается вокруг собственной оси по часовой стрелке) или стрелка, направленная вниз ↓ (электрон вращается вокруг собственной оси против часовой стрелки).
Число электронов в атоме определяют по порядковому номеру
О – 8 электронов, S – 16 электронов.
На одной орбитали могут находиться только ДВА электрона, которые вращаются вокруг своей оси в противоположных направлениях (по часовой стрелке и против часовой стрелке) – электроны с противоположными спинами:
Cледовательно, на s – орбитали максимально может разместиться два электрона (s2); на p – орбитали максимально может разместиться шесть электронов (p6) на d – орбитали максимально может разместиться десять электронов (d10); f – четырнадцать электронов (f14).
III. Располагаясь на различных расстояниях от ядра, электроны образуют электронные слои (энергетические уровни) – каждому слою соответствует определённый уровень энергии.
Условное обозначение уровня - скобка:
)
Число энергетических уровней определяют по номеру периода, в котором находится химический элемент
О – 2 уровня, S – три уровня.
3. Разберем примеры:
Формулы отражающие строение атома H +1 )1e
– схема строения атома, отображает распределение электронов по энергоуровням.
+1 Н 1s1
– электронная формула, отображает число электронов по орбиталям.
+1 Н
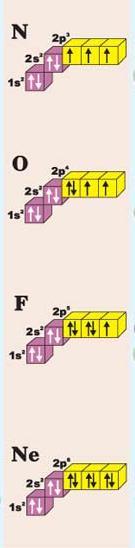
- электронно-графическая формула – показывает распределение электронов по орбиталям и отображает спин электрона.
4. Домашнее задание:
Выучить параграф 53, распределить электроны по энергетическим уровням таких элементов: хлор, бериллий, кальций, медь.



















