Просмотр содержимого документа
«Атомның күрделілігі»

Атырау облысы
Қызылқоға ауданы
Қаракөл орта мектебінің
химия пәні мұғалімі
Усенгалиева Гулхан
Атомның күрделілігі


15 қараша
§21Атомның күрделілігі

Атом сөзінің мағынасы, шығу себебі қандай?
Атом құрылысының ашылу тарихы

Физика пәніне шолу
Демокрит, Эпикур, Аристотель ,Джордано Бруно
Алғаш рет денелердің барлығы да өте кішкентай бөлшектерден тұрады деген көзқарас ертедегі эллада елінде қалыптасты. Оның негізін салушы-грек ғұламасы Демокрит (б.э.б. 460-370). Ол кез келген денені ұсақтап бөле отырып, ең соңында бөлінбейтін бөлшек-атомды(грекше атомос-бөлінбейтін) алуға болады деді. Мыс алманы.
Демокриттің идеясын Эпикур (б.з.б 341-270)одан әрі дамытты. Олда Демокрит сияқты «атомдар өздерінің пішіні мен көлеміне және салмағына және салмағына қарай әртүрлі болады» деп қорытты. Джордано Бруно (1548-1600) заттардың атомдардан тұратынын қорғаумен өтті.

Джозеф Джон Томсон (18 желтоқсан 1856- 30 тамыз 1940) ағылшын физигі, физикадан Нобель сыйлығының лауреаты 1906 жыл
Томсон моделі. Атомның алғашқы моделін ұсынған, электронды ашқан - атақты ағылшын физигі Дж. Дж. Томсон болды. Томсонның ойынша, атомның оң заряды атомның көлемін түгел жайлайды және осы көлемде тұрақты тығыздықпен тарайды. Ең қарапайым атом - сутегі атомы, радиусы, 10 -8 см-ге жуық оң зарядталған шар, оның ішінде электрон орналасады. Күрделірек атомдарда оң зарядталған шардың ішінде бірнеше электрондар болады, сөйтіп, атом жүзім салып пісірген нан сияқты, ондағы жүзімдер электрон рөлін атқарады.


Ол қасиет тек уранға ғана тән емес кейбір басқа да элементтерде (радий мен полоний)болатынын Мария және Пьер Кюрилер тәжірибе жүзінде анықтап ,бұл құбылысқа радиоактивтілік деген атау берді.

Егер ядро құрамындағы протон саны өзгерсе атом қандай өзгеріске ұшырайды?
Табиғатта радиоактивтілік нәтижесінде атомдар өзгеріске ұшырайтыны белгілі болғаннан кейін осындай реакцияларды ғылыми зерттеу институттарында жүргізе бастады.
Бұл үдеріс жасанды радиоактивтілік деп аталады.
Бұл типті реакциялардың кәдімгі химиялық
реакциялардан айырмашылығы-
бір элемент басқа бір элементке айналады

Семей ядролық полигонының жабылғанына 25 жыл

Эрнест Резерфорд (30 тамыз 1871 г. – 19 қазан 1937 г.) химияданНобель сыйлығының иегері 1908 жыл

- 1911 жылы ағылшын ғалымы Э. Резерфорд α –бөлшегімен металдың өте жұқа қаңылтырын атқылап атомның ортасында оң зарядталған бөлшек –ядро бар екендігін анықтап ,атом құрылысының «планетарлық» моделін ұсынды.
- Резерфорд атомының құрылысын Күн жүйесіне ұқсатты. Күн жүйесiндегi планеталар оған тартылып айналғаны сияқты, электрондар да ядроға тартылып оны айнала қозғалады. Осындай ұқсастығы үшiн Резерфорд ұсынған модельдi планетарлық модель деп атаған.
- Бұл модель бойынша атомның ортасында оң зарядталған ядро бар, ал оны электрондар айналып жүреді. Электрон теріс зарядталған ең кіші бөлшек, оның заряды өлшем бірлігі ретінде қабылданған.

Атом ядросының құрамы қандай?
Атомдардың құрылысының қысқаша түрде жазылуы
8 О(8р8 n) 8 e
16
Д. Д. Иваненко (совет ғалымы) және В. Гейзенберг (немецкий ғалымы) 1932 ж протон мен нейтроннан тұрады деген болжамды дамытты.
Нейтрон санын қалай есептейміз?
Мысалы: Натрий атомы үшін
11р+12 n=23
А r= N+Z
Ar – элементтің салыстырмалы атомдық массасы. Z – протондар саны. N – нейтрондар саны.

Химиялық элемент ядросындағы нейтрон саны
өзгерсе атом қандай өзгерісте болады?
8
9
10
Ядроларында протон саны бірдей бірақ массалары әр түрлі, белгілі бір элементті құрайтын атомдар – изотоптар деп атайды. (Изотоп грекше «Бір орынға орналасушы» деген мағынаны білдіреді).

Есептер шығара білеміз бе?
ω( 16 О): ω( 17 О) : ω( 18 О) = 99,759 % : 0,037 %: 0,20 4 %
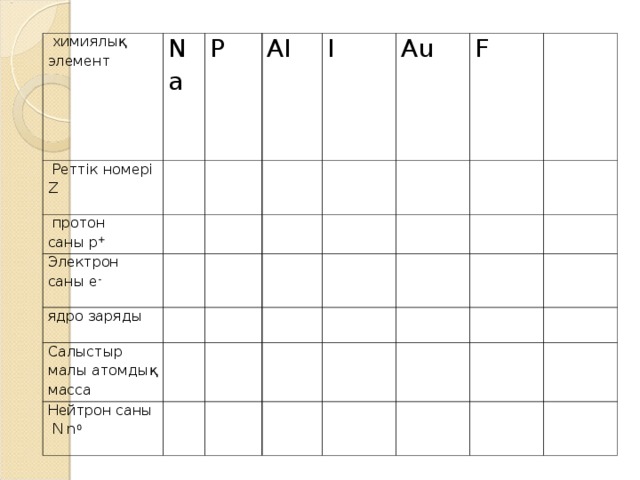
химиялық элемент
Na
Реттік номері
P
Z
протон
саны p +
AI
Электрон саны e -
I
ядро заряды
Салыстыр
малы атомдық масса
Au
Нейтрон саны
N n 0
F
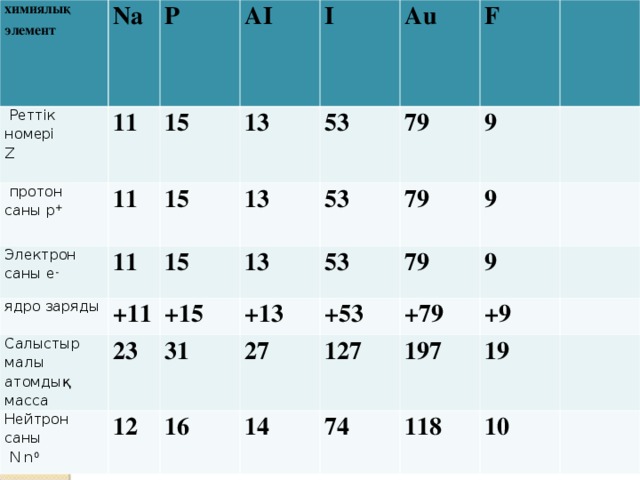
химиялық элемент
Реттік номері
Na
протон
саны p +
Z
11
P
Электрон саны e -
15
AI
11
ядро заряды
11
15
I
13
Салыстыр
малы атомдық масса
+11
15
13
Au
53
Нейтрон саны
N n 0
+15
23
13
53
F
79
31
12
53
+13
9
79
16
27
+53
79
9
127
14
+79
9
74
197
+9
19
118
10

Оқулықпен жұмыс
Үйге тапсырма §20 №3





































