
«Широко распростирает химия руки свои в дела человеческие… »
А.М.Ломоносов

Отметьте в таблице области применения перечисленных в ней реакций.
ПРИМЕНЕНИЕ РЕАКЦИИ ИЛИ ЕЕ ПРОДУКТОВ
ХИМИЧЕСКИЕ СВОЙСТВА АЦЕТИЛЕНА
Реакция с бромной водой
Идентификация непредельных соединений
Реакция горения
Резка и сварка металлов
Реакция с водой
А
Н
Получение мономера для производства поливинилхлорида
Реакция с хлороводородом
М
Производство уксусного альдегида
О
Т
Реакция с перманганатом калия
Ы
Г
С
Ч
С
Е
Б
Ш
Ю
З
А
Р
Е
Н
Ы

Бензол

Цель:
Рассмотреть строение молекулы бензола;
Ознакомить с физическими и химическими свойствами;
Применение бензола и его производных в народном хозяйстве.

Проблемный вопрос:
Какое же строение имеет молекула бензола, и к какому классу углеводородов его можно отнести?


История открытия бензола
С 1814 года улицы Лондона стали освещать газовые фонари. Светильный газ, получаемый из каменного угля нагреванием без доступа воздуха, хранился под давлением в железных баллонах.
Майкл Фарадей обнаружил, что в баллонах из-под газа остаётся бесцветная летучая жидкость. Она конденсируется из светильного газа при низких температурах. Фарадей провёл элементный анализ вещества и обнаружил, что это неизвестный ранее углеводород с массовым отношением углерода к водороду 12:1. Это значит, что на один атом углерода в веществе приходится один атом водорода.

Решить задачу
Плотность паров данного вещества по воздуху 2,69. Массовая доля углерода- 92,3%, водорода- 7,7%. Определите молекулярную формулу вещества.
Ответ: С 6 Н 6

История открытия бензола
В 1833 – 1835 гг . немецкий химик Э . Митчерлих исследовал это вещество , определил его формулу С 6 Н 6 и назвал бензином (от арабского слова, которое обозначает «благовоние») .
Позже его соотечественник Ю. Либих предложил новое имя соединению – бензол, которое прижилось и в русской номенклатуре.

Ароматические соединения, или арены — большая группа соединений карбоциклического ряда, молекулы которых содержат устойчивую циклическую группировку из шести атомов углерода (бензольное кольцо), обладающую особыми физическими и химическими свойствами.

Структура молекулы бензола
- Структуру бензола установил немецкий химик Фридрих Август Кекуле в 1865 г.
- Однажды Кекуле пришлось участвовать в качестве свидетеля в судебном процессе по делу об убийстве графини Герлиц. На этом процессе демонстрировалось в качестве улики кольцо графини в виде двух переплетенных змеек, которое похитил преступник. Эти змейки врезались в память ученому. Как-то раз, после долгой работы над учебником, Кекуле уснул, и ему приснились атомы углерода и водорода , сцепленные в нити, которые сближались и свертывались в трубку, напоминая двух змей. Одна из змей вцепилась в собственный хвост, продолжая крутиться.
- Сон оказался в руку. Кекуле сцепил все атомы углерода в шестиугольник с чередующимися двойными и одинарными связями.
По другой версии формула бензола предстала немецкому учёному Августу Кекуле во сне в виде шести обезьян, соединившихся друг с другом в виде математической фигуры - шестигранника
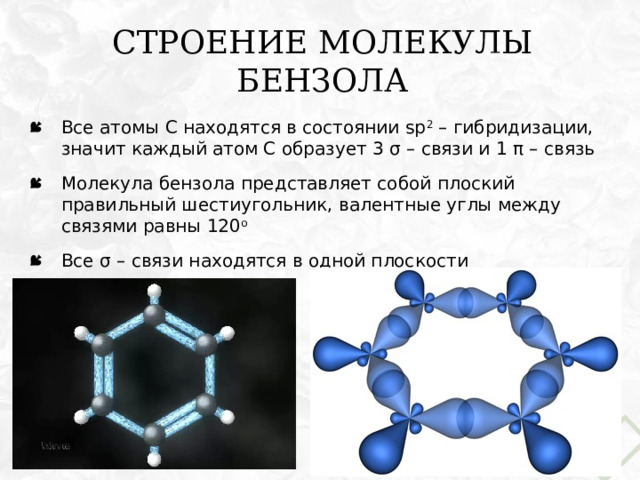
Строение молекулы бензола
- Все атомы С находятся в состоянии sp 2 – гибридизации, значит каждый атом С образует 3 σ – связи и 1 π – связь
- Молекула бензола представляет собой плоский правильный шестиугольник, валентные углы между связями равны 120 о
- Все σ – связи находятся в одной плоскости

Строение молекулы бензола
- 6 негибридизованных p – орбиталей атомов С расположенные перпендикулярно плоскости кольца и параллельно друг другу, перекрываются между собой и образуют единую сопряженную π - систему
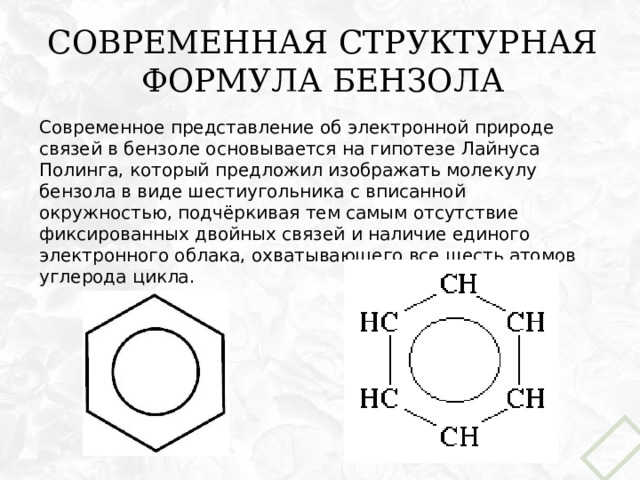
Современная структурная формула бензола
Современное представление об электронной природе связей в бензоле основывается на гипотезе Лайнуса Полинга, который предложил изображать молекулу бензола в виде шестиугольника с вписанной окружностью, подчёркивая тем самым отсутствие фиксированных двойных связей и наличие единого электронного облака, охватывающего все шесть атомов углерода цикла.
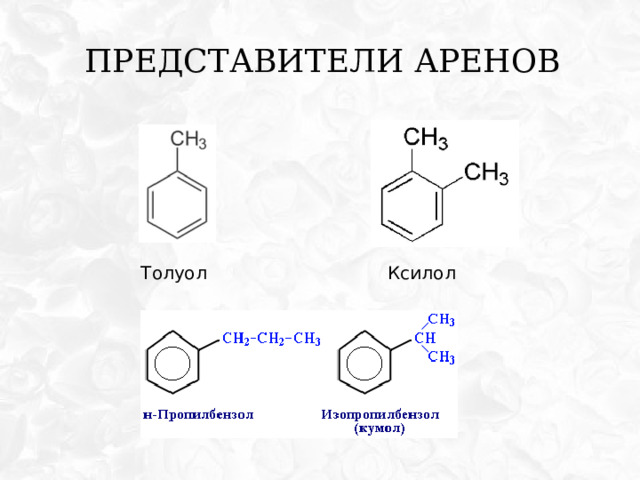
Представители аренов
Толуол
Ксилол

Номенклатура аренов
- Цикл нумеруется начиная с того атома, к которому присоединен простейший радикал, в сторону ближайшего
- Корнем в названии всех аренов будет слово «бензол»
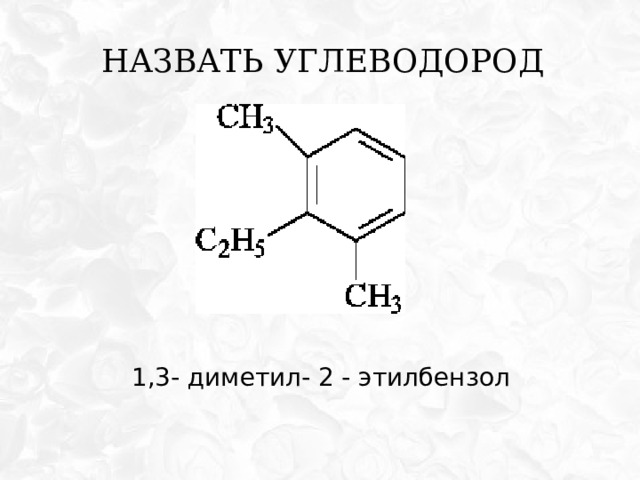
Назвать углеводород
1,3- диметил- 2 - этилбензол
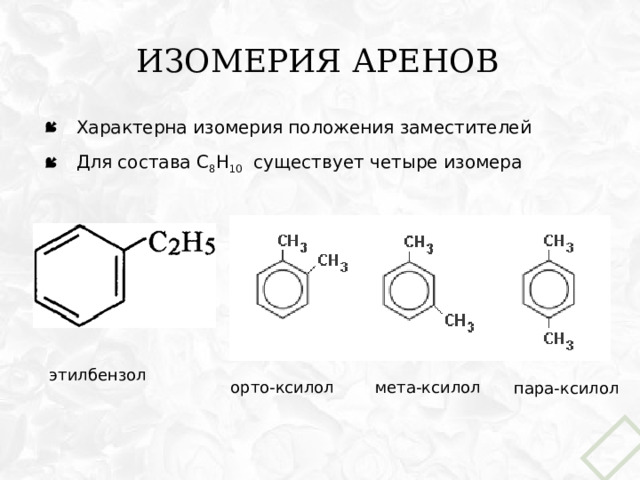
Изомерия аренов
- Характерна изомерия положения заместителей
- Для состава С 8 Н 10 существует четыре изомера
этилбензол
мета-ксилол
орто-ксилол
пара-ксилол

Получение
Бензол получают из каменноугольной смолы, образующейся при коксовании угля.
C акт . 400 о С
3С 2 H 2 → C 6 H 6 - реакция Зелинского
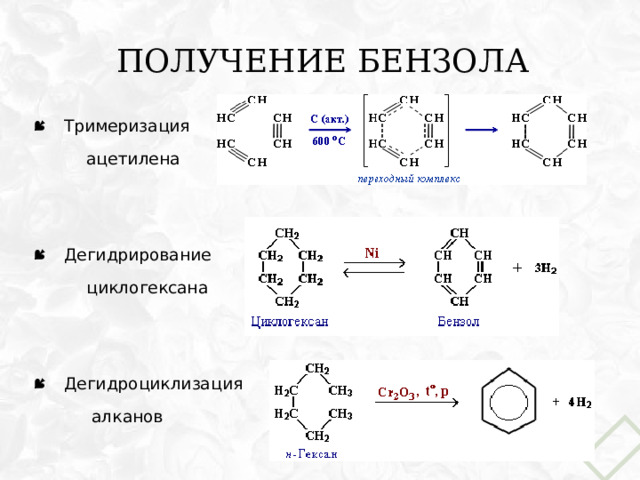
Получение бензола
ацетилена
циклогексана
алканов

Получение гомологов бензола

Физические свойства бензола
- Прозрачная бесцветная жидкость со сладковатым запахом.
- Легко переходит в твердое состояние: температура плавления бензола составляет +5,5 ºС, температура кипения + 80,1 ºС.
- В воде бензол практически нерастворим, но является хорошим растворителем многих органических веществ.
- Летуч.

Химические свойства
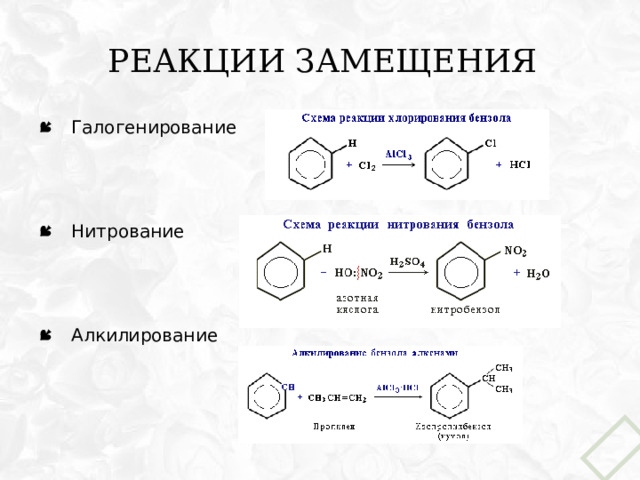
Реакции замещения
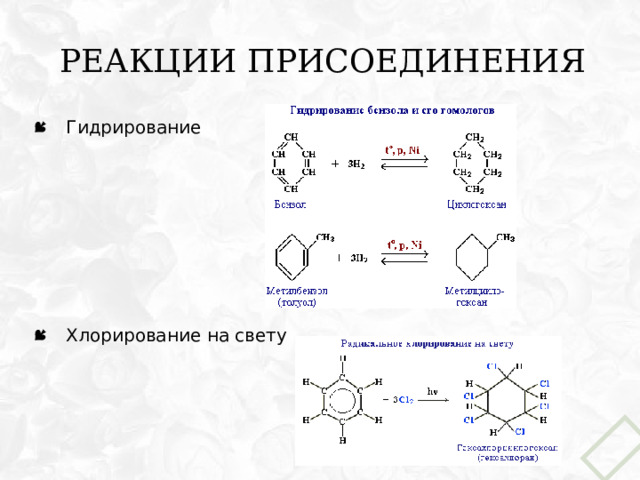
Реакции присоединения

Реакции окисления
- бензол устойчив к действию окислителей
- гомологи бензола легко окисляются
2 С 6 Н 6 + 15 О 2 = 12 СО 2 + 6 Н 2 О

Химические свойства
▪ Реакции окисления
Бензол не обесцвечивает раствор перманганата калия

Физиологическое действие бензола
- В больших дозах бензол вызывает тошноту и головокружение, а в некоторых тяжёлых случаях отравление может повлечь смертельный исход.
- Пары бензола могут проникать через неповрежденную кожу.
- Хроническое отравление бензолом может стать причиной лейкемии (рака крови) и анемии (недостатка гемоглобина в крови).
- Сильный канцероген

Применение бензола

Отметьте клетки, в которых записаны формулы аренов. Найдите среди них изомеры.

Тестирование
1.Общая формула ароматических углеводородов
А)С n H 2n Б)C n H 2n+2
В)C n H 2n-6 Г)C n H 2n-2
2.Ароматические углеводороды иначе называют
А)Циклоуглеводородами Б)Аренами
В)Бензольными Г)Пахучими
3. Бензолу не свойственно
А)Жидкое агрегатное состояние Б)Хорошая растворимость в воде
В)Характерный запах Г)Температура кипения 80,1°С
4.В какой из перечисленных реакций образуется хлорбензол
А) C 6 H 6 +Cl 2 Б)C 6 H 6 +Br 2
В) С 6 H 12 +Cl 2 Г) C 7 H 8 +Cl 2
5.Продукт реакции нитрования бензола
А) 1,4-динитробензол Б)Нитробензол
В)1,3,5-нитробензол Г)Смесь нитробензола и хлорбензола
6. Производные бензола, применяемые в народном хозяйстве:
А)Ацетон Б)Хлорбензол
В)Этиленгликоль Г)Глицерин
В)C n H 2n-6
Б)Аренами
Б)Хорошая
растворимость в воде
А) C 6 H 6 +Cl 2
Б)Нитробензол
А)Ацетон

Итог урока
Сравнение по таблице
Признаки сравнения
Алканы
Общая формула
CnH2n+2
Номенклатура
Алкены
Алкадиены
CnH2n
-ан
Нахождение в природе
Природный газ и нефть
CnH2n-2
Алкины
-ен-…
Реакция горения
Реакция замещения
+
_
Арены
-диен-…
CnH2n-2
+
-ин…
+
Реакция присоединения
_
_
_
+
_
_
+
+
_
+
+
CnH2n-6
бензол
Нефть
+
+
+

Домашнее задание
§ 14-15, в-сы 1-11, упр 12аб, з 1-2 стр 66-67


















































