Вкусные батарейки
Выполнил работу: ЯнцевГерман Валерьевич
Новосибирская область, город Искитим
МБОУ-СОШ №14 г.Искитима
Руководитель: Сивурова Татьяна
Владимировна
Оглавление
Введение 3
Батарейка 4
Чем опасна использованная батарейка? 5
Анализ статей 7
Практическая часть 7
Выводы 11
Литература 12
Введение
Мы не представляем своей жизни без приборов, которые работают за счет электрической энергии. Самыми миниатюрными и часто используемыми являются конечно батарейки.
Однажды в торговом центре я обратил внимание на автоматы, в которые люди складывали, нерабочие гальванические элементы. И я задумался, а какой вред несут использованные батарейки? И можно ли их заменить экологически чистыми источниками тока?
И я решил заняться изучением этих вопросов.
Цель работы: самостоятельно изготовить источники постоянного электрического тока в бытовых условиях из овощей и фруктов.
Задачи работы:
Изучить информацию о принципе работы батарейки.
Найти информацию о влиянии использованных батарее на окружающую среду
Изучить статьи об альтернативных источниках энергии
Сконструировать источники тока, используя потенциал овощей и фруктов.
Выявить экспериментальным путем зависимость силы тока и напряжения от физических и аграрных характеристик.
Место исследования:
кабинет физики МБОУ-СОШ №14 г.Искитима
Гипотеза: из доступных фруктов и овощей можно сделать источник тока и использовать его в качестве источника электроэнергии.
Предмет исследования: получение электрического тока с помощью самодельных источников тока, используя доступные овощи и фрукты
Объект исследования: самодельные источники тока из овощей и фруктов
Батарейка
1 Батарейка- это химический источник тока. Они бывают разной формы и размеров, разных видов: солевые, щелочные, ртутные, серебряные, литиевые. Одни изготовлены для одноразового использования, другие можно перезаряжать. И каждая из них имеет свои плюсы и минусы. Солевые самые дешевые, но они быстро разряжаются, их нельзя перезарядить, и выходят из строя при низких температурах. Щелочные имеют большую мощность, чем солевые, и практически не подвержены саморазрядке. Ртутные опасны для здоровья человека, но их можно перезаряжать несколько раз, и они могут работать в суровых климатических условиях. Серебряные работают при высоких и низких температурах, у них длительный срок службы, но они очень дорогие. Литиевые обладают длительным сроком службы, работают при высоких и низких температурах, как и серебряные и их можно перезаряжать.
Устройство пальчиковой батарейки
В магазинах можно увидеть большое количество батареек, они различны по некоторым принципам, но схема работы у них одна. У любой батарейки есть положительный полюс – анод, отрицательный полюс - катод и электролит. Именно эти составляющие и являются основными элементами батарейки.
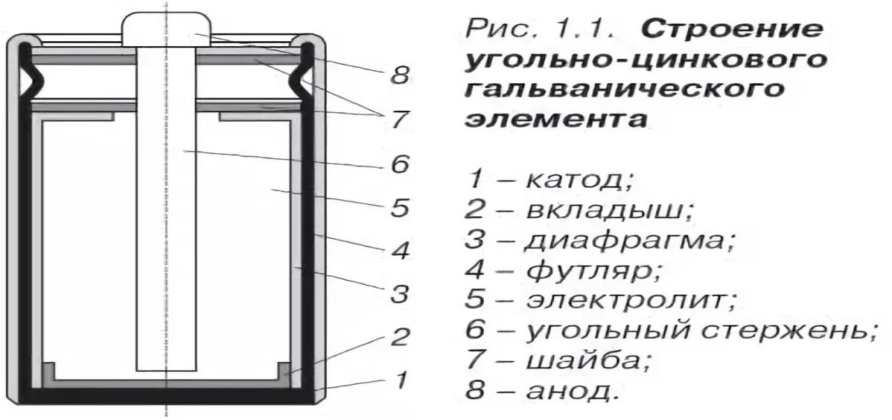
Принцип работы химического источника тока.
В источнике тока совершается работа по разделению положительно и отрицательно заряженных частиц, которые накапливаются на полюсах источника.
Гальванический элемент - это устройство, в котором химическая энергия окислительной-восстановительной реакции превращается в электрическую за счет разделения процессов окисления и восстановления.
Химические источники тока имеют основные составляющие - электрод, на котором окисляется восстановитель-анод, электрод, на котором восстанавливается окислитель – катод и электролит- раствор, необходимый для упорядочения движения электронов. При помещении электродов в электролит возникает разность потенциалов. Анод отдает электроны, катод их принимает. На поверхности идут химические реакции. ). В батарейке электроны движутся в определённом направлении, создавая электрический ток.
Металлы по своим химическим свойствам являются восстановителями. Металлы легко отдают валентные электроны и превращаются в положительно заряженные ионы.
То есть, для создания химического источника тока необходимы электроды из разных металлов и раствор электролита.
Чем опасна использованная батарейка?
2 Батарейка, даже отслужившая свой срок, не представляет опасности, при условии, что ее корпус не поврежден, и она хранится при комнатной температуре и минимальной влажности. Попадая же вместе с бытовыми отходами на свалку, и подвергаясь воздействию разнообразных атмосферных факторов, батарейка начинает ржаветь и разрушаться под воздействием коррозии. Ее корпус теряет герметичность, содержимое получает доступ во во внешнюю среду, отравляя ее, и ее обитателей.
Что происходит с батарейкой на свалке?
Щелочь и тяжелые металлы из разрушившейся батарейки представляют опасность для окружающей среды. Поступая вначале в почву, токсичные вещества достигают грунтовых вод, откуда попадают в водоемы, в том числе и те, из которых ведется забор водопроводной воды. Химическому загрязнению подвергаются земли и произрастающие на них растения, в том числе и многочисленные пищевые культуры; мясо и молоко сельскохозяйственных животных, пасущихся на зараженных пастбищах, тоже становятся опасным. Опасна не только пассивная коррозия, в результате которой батарейки загрязняют почву и воду; нередко свалки подвергаются
самовозгоранию, и находящиеся в мусоре батарейки, нагреваясь, выделяют в атмосферу диоксины, заражая еще и воздух. Диоксины в десятки тысяч раз ядовитее цианида и являются причиной раковых заболеваний и заболеваний репродуктивной системы.
В чем опасность содержимого батарейки?
Наибольшую опасность представляют содержащиеся в батарейках тяжелые металлы, прежде всего ртуть.
Ртуть - сильнейший яд, относящийся к первому классу опасности. Накапливаясь в тканях всех органов, вызывает нервные расстройства и расстройства двигательного аппарата, заболевания дыхательной системы, ухудшает зрение и слух, приводит к повреждению головного мозга и нервной системы в целом, разрушительно действует на почки и печень. Особо опасна для детей. Она массово использовалась до 2001 года.
Не меньшую угрозу представляют и другие тяжёлые металлы: кадмий, свинец.
Свинец - накапливается в почках и вызывает сильнейшие расстройства нервной системы и заболевания мозга.
Кадмий - накапливается в почках, печени, костях и щитовидной железе. Приводит к возникновению раковых заболеваний. В настоящее время во всем мире постепенно идёт замена еще достаточно распространённых и никель-кадмиевых аккумуляторов на более продвинутые и безопасные с экологической точки зрения никель-металл-гидридные и литий-ионные. В них больше электрическая ёмкость и количество циклов зарядки-разрядки. Но и они рано или поздно выходят их строя и требуют утилизации.
Токсичное воздействие тяжелых металлов на организм не проявляется одномоментно, полученные с водой и пищей микродозы отравляющего вещества накапливаются в организме на протяжении многих лет, оказывая разрушающее влияние.
Анализ статей
Изучив данный материал о вреде батареек, я задумался, а можно ли их заменить на более экологически чистые. Я нашел статьи в журналах: Энергия «из ничего» // журнал «Юный эрудит №10, 2009 год» и В.Н. Винер «Фруктовая батарейка» // журнал «Химия и Химики, №8, 2009 год». В данных статьях описывался опыт с лимонами, а именно авторы статьи предлагают взять лимон и два электрода (медный и цинковый), а также мультиметр. Оказалось, что если вставить эти электроды в лимон, то вольтметр покажет напряжение порядка одного вольта, а если взять три лимона, то горит светодиод. В статье В.Н. Винер «Фруктовая батарейка» // журнал «Химия и Химики, №8, 2009 год» описывается также данный опыт, но там говориться, что можно построить батарейку и из других овощей и фруктов.
Изучив данные статьи, я решил самостоятельно проверить данные опыты и проверить их действие на электронных часах.
Практическая часть
Итак, для создания «вкусной» батарейки я взял те фрукты и овощи, которые наиболее популярны оказались при проведении подобных работ.:
лимон, яблоко, картофель, огурец, грейпфрут;
медная пластина– это будет наш положительный полюс;
цинковая пластина – для создания отрицательного полюса;
провода, зажимы;
мультиметр;
светодиод;
электронные часы
Большинство фруктов содержит в своем составе слабые растворы кислот. Потому я первым делом проверил их на уровень кислотности.
| Название продукта | Уровень ph |
| Картофель сырой | 5,5 |
| Грейпфрут | 4 |
| Яблоко | 4 |
| Лимон | 2,4 |
| Огурец | 6,5 |
Прежде всего, я подготовил медную и цинковую пластины. Затем вставил в овощ или фрукт и получается «батарейка». Электроды располагал на одинаковом расстоянии друг от друга (1 см).
Результаты эксперимента я занес в таблицу.
| Основа батарейки | Напряжение на электродах, В | Сила тока, мА | Светодиод |
| Лимон | 0,94 | 0,85 | Не горит |
| грейпрфрут | 0,89 | 0,15 | Не горит |
| яблоко | 0,95 | 0,35 | Не горит |
| Картофель сырой | 0,91 | 0,6 | Не горит |
| Огурец | 0,93 | 0,29 | Не горит |
Я решил исследовать, как зависит напряжение от расстояния между электродами. Для этого овощи и фрукты, изменял расстояние между пластинками увеличил до 3 см и измерял напряжение. Результаты эксперимента занес в таблицу.
| Расстояние между электродами, см | Напряжение между электродами, В |
| Лимон | 0,9 |
| грейпфрут | 0,87 |
| яблоко | 0,92 |
| Картофель(сырой) | 0,78 |
| Огурец | 0,9 |
Вывод: напряжение между электродами уменьшилось с увеличением расстояния между ними.
Я решил измерить напряжение спустя 3 дня. Результаты измеренного напряжения на батарейках занес в таблицу:
| Основа батарейки | Напряжение ,В через 3 дня (расстояние 1 см) | Сила тока, мА Через 3 дня (расстояние 1 см) |
| Лимон | 0,86 | 0,8 |
| грейпфрут | 0,83 | 0,16 |
| яблоко | 0,9 | 0,3 |
| Картофель | 0,06 | 0,48 |
| огурец | 0,1 | 0,24 |
Вывод: постепенно напряжение на всех «вкусных» батарейках уменьшается. Вытаскивая пластины из овощей и фруктов, я обратил внимание на то, что они сильно окислились. Это значит, что кислота вступала в реакцию с ними. За счет этой химической реакции и протекал очень слабый электрический ток.
Затем я решил собрать батарейку, используя одновременно несколько фруктов. Вот, что получилось.
О
 пыт батарейка из 4 лимонов
пыт батарейка из 4 лимонов

Т


 ок такой батарейки 0,32 А и напряжение 3,76 В. От такой батарейки горит светодиод.
ок такой батарейки 0,32 А и напряжение 3,76 В. От такой батарейки горит светодиод.
Батарейка из картофеля, лимона, яблока и огурца выдает напряжение 3,68 В, а если заменить яблоко грейпфруктом, то напряжение будет3,53 В.



Электронные часы работают от огурца и яблока, от двух лимонов, а также от 4 картофелин.
Выводы
Проанализировав исследования, можно сделать выводы:
используя природный потенциал свежих фруктов и овощей, можно создать батарейку.
Полученные источники тока можно использовать для приборов с низким потреблением энергии.
В ходе исследовательской работы я:
Познакомился с устройством батарейки и принципом ее действия.
Узнал, что батарейки надо правильно утилизировать.
Изготовил овощные и фруктовые батарейки, проверил их действие.
Литература
https://ru.wikipedia.org/wiki/Типоразмеры_гальванических_элементов
http://cgon.rospotrebnadzor.ru/content/62/1040/
Энергия «из ничего» // журнал «Юный эрудит №10, 2009 год»
В.Н. Винер «Фруктовая батарейка» // журнал «Химия и Химики, №8, 2009 год»
1� https://ru.wikipedia.org/wiki/Типоразмеры_гальванических_элементов
2� http://cgon.rospotrebnadzor.ru/content/62/1040/









 пыт батарейка из 4 лимонов
пыт батарейка из 4 лимонов



 ок такой батарейки 0,32 А и напряжение 3,76 В. От такой батарейки горит светодиод.
ок такой батарейки 0,32 А и напряжение 3,76 В. От такой батарейки горит светодиод.












