Теориялық мүмкіндігіне қарағанда реакция өнімінің шығымының массалық үлесін есептеу
1-мысал.Лабараторияда 246 гнитробензолды тотықсыздандыру арқылы 180 г анилин алды. Аналиннің теориялық мүмкіндікке қарағандағы шығымның массалық үлесін табамыз.
Берілгені:
m (С6Н5NО2) = 246 г
m (С6Н5NH2) = 180 г
т/к ω(С6Н5NH2)=?
Шешуі: 1) Реакция теңдеуін жазамыз
С6Н5NО2+ 3H2 = С6Н5NH2 + 2H2O
2) Нитробензолмен анилиннің мольдік массаларын табамыз.
m (С6Н5NО2) =123 г/моль
m (С6Н5NH2) = 93 г/моль
3) Реакция теңдеуі бойынша 1 моль нитробензолды тотықсыздандырғанда 1 моль анилин алынады, тотықсызданған 1 моль нитробензол мен алынған 1 моль анилиннің массасын табамыз.
m = ѵ∙M m (С6Н5NО2) = 1 моль ∙ 123 г/моль = 123 г
m (С6Н5NH2) = 1 моль ∙ 93 г/моль = 93 г
4) Реакция теңдеуі бойынша 123 г нитробензолды тотықсыздандырғанда 93 г анилин алынады, ал 246 г нитробензолды тотықсыздандырғанда алынатын анилиннің массасын табамыз.
123 г -------- 93 г х = 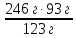 = 186 г
= 186 г
246 г --------х
5) Реакция шығымының массалық үлесін табамыз.
 =
=  ∙ 100%
∙ 100%  (С6Н5NH2) =
(С6Н5NH2) =  ∙ 100% = 96.8%
∙ 100% = 96.8%
Жауабы: шығымы 96.8%
2-мысал.Массасы 140,8 г шығымы 80% сірке – қышқылының массасын табыңыз
m (эфир) = 140,8 г
ω(эфир) = 80%
т/к m (СН3 СООН) =?
Шешуі: 1) Эфирдің теориялық шығымын анықтаймыз
ω =  ∙ 100% m (эфир) =
∙ 100% m (эфир) = ∙ 100%
∙ 100%
m (эфир) =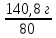 ∙ 100% = 176 г
∙ 100% = 176 г
2) реакция теңдеуін жазамыз
С2Н5ОН + СН3 СООН = СН3 СОО С2Н5 + H2O
3) Сірке қышқылы мен сірке-этил эфирінің мольдік массасын табамыз.
m (СН3 СООН) = 60 г/моль
m (СН3 СОО С2Н5 ) = 88 г/моль
4) Реакция теңдеуі бойынша 1 моль сірке-этил эфирін алу үшін 1моль сірке қышқылы қажет, алынатын сірке-этил эфирі мен қажетті сірке қышқылының массасын табамыз.
m = ѵ∙M m (СН3 СОО С2Н5) = 1 моль ∙ 88 г/моль = 88 г
m (СН3 СООН) = 1 моль ∙ 60 г/моль = 60 г
5) Реакция теңдеуі бойынша 88 г сірке-этил эфирін алу үшін 60 г сірке қышқылы қажет, ал 176 г сірке-этил эфирін алу үшін қажетті сірке қышқылының массасын табамыз.
88 г -------60 г
176 г -----х х = 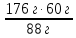 = 120 г
= 120 г
Жауабы: 120 г сірке қышқылы
Реакцияға түскен немесе реакция нәтижесінде түзілген заттардың массасы және зат мөлшері арқылы зат массасы мен газ көлемін табуға есептер шығару
1-мысал. 12,6 г азот қышқылы калий гидроксидімен әрекеттескен кезде түзілген тұздың массасын табыңыздар.
Берілгені: m(HNO3) = 12,6 г
m/к. m (КNO3) = ?
Шешуі: 1) Рекция теңдеуін жазамыз.
HNO3 + КОН = КNO3 + Н2 О
2)Азот қышқылы мен калий нитратының молярлық массаларын табамыз.
М (HNO3) =63 г/моль
М (КNO3) =101 г/моль
3) Реакция теңдеуі бойынша 63 г азот қышқылы калий гидроксидімен әрекеттескенде
1 моль азот қышқылы мен 1 моль калий нитратының массаларын табамыз.
m = v ∙ M
m(HNO3) = 1 моль ∙ 63 г/моль = 63 г
m (КNO3) =1 моль ∙ 101 г/моль =101 г
4) Реакция теңдеуі бойынша 63 г азот қышқылы калий гидроксидімен әрекеттескенде
101 г калий нитраты түзіледі, 12,6 г азот қышқылы калий гидроксидімен әрекеттескен кезде түзілетін калий нитратының массаларын табамыз.
63 г --- 101 г
12,6 г ---х г
х = 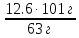 = 20.2 г Жауабы: 20,2 г калий нитраты түзіледі.
= 20.2 г Жауабы: 20,2 г калий нитраты түзіледі.
2-мысал. 3 г көмір толық тотығу үшін оттегінің қандай көлемі жұмсалады?
Берілгені:
m(С) = 3 г
m/к V(O2) = ?
Шешуі: 1) Рекция теңдеуін жазамыз.
С+О2 →СО2
2) Көмірдің молярлық массасын табамыз.
М (С) =12 г/моль.
3) Кез-келген газдың 1 молы қалыпты жағдайда 22,4 л көлем алатынын ескерсек, 1 моль көмір тотығу үшін жұмсалатын оттегі 22,4 л көлем алады. 1 моль көмірдің массасын табамыз
m = v ∙ M
m(С) = 1 моль ∙12 г/моль = 12 г
4) Реакция теңдеуі бойынша 12 г көмір тотығу үшін 22,4 л оттегі жұмсалады, ал 3 г көмір толық тотығу үшін қажетті оттегінің көлемін табамыз.
12 г---22,4 л
3 г ---х х = 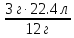 = 5.6 л
= 5.6 л
Жауабы: 5.6 л оттегі жұмсалады.
3-мысал. Күкірт жанғанда 112 л (қ.ж) газ түзілді. Жанған күкірттің массасын табамыз.
Берілгені:
V (SO2) = 3 г
m/к m (S) = ?
Шешуі: 1) Рекция теңдеуін жазамыз.
S+О2 →SО2
2) Күкірттің молярлық массасын табамыз.
М (S) =32 г/моль.
3) Кез-келген газдың 1 молы қалыпты жағдайда 22,4 л көлем алатынын ескерсек, 1 моль күкірт жанғанда түзілген күкірт (ІҮ) оксиді 22,4 л көлем алады. 1 моль күкірттің массасын табамыз .
m = v ∙ M
m(С) = 1 моль ∙32 г/моль = 32 г
Оқушыларды бағалау.
Үйге тапсырма:
4) Реакция теңдеуі бойынша 32 г күкірт жанғанда 22,4 л күкірт (ІҮ) оксиді түзіледі, ал 112 л күкірт (ІҮ) оксиді түзілген кезде жанған күкірттің массасын табамыз.
32 г---22,4 л
х ---112 л х = 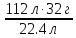 = 160 г
= 160 г
Жауабы: 160 г күкірт жанғанда
4-мысал. 0.3 моль тұз қышқылымен әрекеттесетін натрийдың массасын табамыз.
Берілгені:
v (HCI) =0, 3 моль
m/к m (Na) = ?
Шешуі: 1) Рекция теңдеуін жазамыз.
2Na + 2HCI→ 2NaCI + H2
2) Натрийдің молярлық массасын табамыз.
М (Na) =23 г/моль.
3) 2 моль натрийдың массасын табамыз.
m = v ∙ M
m(Na) = 2 моль ∙2 3 г/моль = 46 г
4) Реакция теңдеуі бойынша 2 моль тұз қышқылымен 46 г натрий әрекеттеседі, ал 0.3 моль тұз қышқылымен әрекеттесетін натрийдың массасын табамыз.
2 моль---46 г
0.3 моль ---х х = 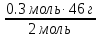 = 6.9 г
= 6.9 г
Жауабы: 6.9 г натрий әрекеттеседі.
Сандық есептер
1-100. Құрамында 16 г күкірт болса, күкіртті газдың SO2 массасы қандай екенін табыңдар.
Шешуі: 16гx г
S→SO2 16 г → х г х= 16 ∙ 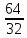 =32 г
=32 г
32 г 64 г 32 г →64 г
1-101. Құрамында 32 г мыс болса, куприттің Cu2 O массасы қандай болғаны
Шешуі: 32 гx г
2 Cu→Cu2O 32 г → х г х= 32 ∙ 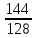 = 36 г
= 36 г
128 г 144 г128 г →144 г
1-102.Массасы 80г сусыз мыс (II) сульфатын алу үшін кристалгидраттың CuSO4 ∙5H2O қандай массасы қажет болатының есептеңдер?
Шешуі:x г 80 г
CuSO4 ∙5H2O → CuSO4 80 г → х г х= 250 ∙ 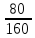 = 125 г
= 125 г
250 г 160 г160 г →250 г
1-103. Құрамында массалық үлесі 70% темір (III) оксиді Fe 2 O 3 және 30% темір (II) оксиді FeO бар қоспасының массасы 300 г.Осы қоспадан темірдің қандай массасын алуға болатындығын есептеңдер.
Шешуі: Қоспадағы әр заттың массасын табамыз:
m = (Fe 2 O 3 ) =0,7 ∙ 300 = 210 гm = (FeO ) =0,3 ∙ 300 = 90 г
Әр қосылыстың құрамындағы темірдің массасын есептейміз:
210 гx г
Fe 2 O 3 →Fe 210 г → х г х= 210 ∙ 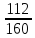 = 147 г
= 147 г
160 г 112 г160 г →112 г
90 гx г
Fe O →Fe 90 г → х г х= 90 ∙ 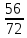 = 70 г
= 70 г
72 г 56 г72 г →56 г
Қоспадағы темірдің массасы:
m (Fe) = m1 (Fe ) + m2 (Fe) = 147 +70 = 217
1-104.Аммосфостың NH4H2PO4 2,5килограмында фосфор (V)оксидінің P2O5қандай массасы болады?
Шешуі: 2500 гx г
2NH4H2PO4→ P2O5 2500 г → х г х= 2500 ∙ 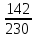 = 1,5 г
= 1,5 г
230 г 142 г230 г →142 г
1-105. Құрамында 42,8% көміртек және 57,2% оттек бар көміртек оксидінің формуласын табыңдар?
Шешуі:CxOу x: у = 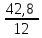 :
: 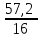 = 3,6 : 3,6 = 1: 1
= 3,6 : 3,6 = 1: 1
Жауабы:CO
1-106.Элементтік құрамы мынадай: темірдің массалық үлесі 0,7 (немесе 70%) оттектің массалық үлесі 0,3 (немесе 30%) қосылыстың химиялық формуласын табыңдар.
Fe x Oу x : у = 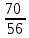 :
: 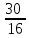 = 1,25 : 1,875 =
= 1,25 : 1,875 =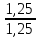 :
: 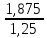 1: 1,5 = 2:3
1: 1,5 = 2:3
Жауабы: Fe2 O3
1-108.Күкірттің оттекпен қосылысының салыстырмалы молекулалық массасы оттек молекуласының массасынан екі есе ауыр.Осы тұншықтырғыш газдың формуласын табыңдар.
Шешуі:Mr (SxOу ) = 2 ∙ Mr (O2) = 2 ∙ 32 =64
SxOу құрамында күкірттің екі атомы болуы мүмкін емес:
Mr (2S ) = 2 ∙ 32 =64 себебі, зат құрамында оттек болуы керек.
Mr(O ) = 64 - Mr (S) = 64 – 32 = 32
У(O) =  = 2
= 2
Жауабы:SO2
1-109. Құрамындағы көміртек, сутек және оттек атомдарының массалық қатынастары 6:1:4 болатын сірке альдегидінің қарапайым формуласын табыңдар.
Шешуі:
Cx HуOz x : у : z =  :
:  = 0,5 : 1 : 0,25 =
= 0,5 : 1 : 0,25 =  :
:  = 2: 4 : 1 Жауабы:C 2 H4 O
= 2: 4 : 1 Жауабы:C 2 H4 O
1-110.Табиғи маржанның құрамында кальций, көміртек, оттек массалық қатынастары10:3:12-ге тең болады.Маржанның формуласын табыңдар.
Шешуі:
Cax CуOz x : у : z =  :
:  = 0,25:0,25:0,75 =
= 0,25:0,25:0,75 =  :
:  = 1: 1 :3 Жауабы:CaCO3
= 1: 1 :3 Жауабы:CaCO3
1-111. Құрамында элементтердің массалық үлестері мынадай: магний 41,4%, оттек 55,2% , сутек 3,4% болатын қосылыстың химиялық формуласын табыңдар.
Шешуі:MgxOуHz
x: у : z=  :
:  = 1,7 : 3,4 : 3,4/1,7 = 1: 2 :2
= 1,7 : 3,4 : 3,4/1,7 = 1: 2 :2
Жауабы:Mg (OH)2
1-112. Құрамындағы элементтердің массалық үлесі төмендегідей:натрий 42,1%, оттек 39%,фосфор 18,9% болатын тұздың химиялық формуласын табыңдар.
Шешуі: Na x PуOz
x : у : z=  :
:  = 1,8 : 2,4 : 0,6 / 0,6 = 3: 4 :1
= 1,8 : 2,4 : 0,6 / 0,6 = 3: 4 :1
Жауабы: Na 3PO4
1-113.Алюминий,оттек және сутек атомдарының массалық қатынастары 9:16:1 болатын қосылыстың қарапайым формуласын табыңдар.
Шешуі:AIxOуHz
x: у : z=  :
:  = 0,33 : 1 : 1 = 1: 3 : 3
= 0,33 : 1 : 1 = 1: 3 : 3
Жауабы:AI (OH) 3
1-114.Сутек, күкірт және оттек атомдары массаларының қатынастары 1:16:32 –ге тең болатын құрамында күкірті бар қышқылдың қарапайым формуласын табыңдар.
Шешуі:HxSуOz
x : у : z=  :
:  = 1 : 0,5 : 2 /0,5 = 2: 1 : 4
= 1 : 0,5 : 2 /0,5 = 2: 1 : 4
Жауабы: H 2 SO4
1-115. Күкірттің оттекті қосылысында 1 г күкіртке 1,5 г оттек сәйкес келеді.Салыстырмалы молекулалық массасы 80-ге тең болса, қосылыстың формуласы қандай болғаны?
Шешуі: Sx Oу x : у = 1 ∙32 : 1,5∙ 32 = 32 : 48 =  :
:  = 1:3
= 1:3
Жауабы: SO3
2-тәсіл. Sx Oу m (S) : m (O) = 1 : 1,5 =2 :3 2+3=5
5_______80
2______ x x = 80 ∙ 2:5 = 32 x =  = 1
= 1
5_______80
3______ x x = 80 ∙ 3 : 5 = 48 x =  = 3 Жауабы: SO3
= 3 Жауабы: SO3
1-116.Бір элементтің оксидінің формуласы ЭO2, ондағы оттектің массалық үлесі 53,3%.Элементті табыңдар.
Шешуі:ЭO2ω (Э) = 100 % - 53,3 % = 46,7 %
 : = 28
: = 28
Жауабы: SiO2
1-117.Кальций хлоридінің кристалгидратының 14,6 грамын сусыздандырғанда оның массасы 7,2 грамға кемиді.Кристалгдраттың формуласын табыңдар.
Шешуі: m (CaCI2) = 14,6 – 7,2 = 7,4
14,6 г 7,4 7,2 г
CaCI2 ∙ H2O =CaCI2 +у H2O
250 111 x
7,4 г __________7,2 г
111 г _________ xг
x = 111:  = 108 гу = =
= 108 гу = =  = 6
= 6
Жауабы: CaCI2 ∙6 H2O
1-118.Мольдік массасы 250г/моль болса, мыс (II) сульфатының кристалгидратының формуласы қандай болғаны? Кристалгидратының құрамындағы судың зат мөлшерін табыңдар.
Шешуі: M (Cu SO4) = 160 г/ моль
CuSO4 ∙x H2O x∙ Mr (H2 O) = 250 – 160 = 90 г/ моль
18 x = 90 x =  = 5
= 5
Жауабы: CuSO4 ∙5 H2O
1-119. Кальций сульфаты кристалгидраты құрамында 23,3 % кальций. 18,6 %күкірт,37,2 % оттек және 20,9 % су бар. Кристалгидраттың формуласын табыңдар.
Шешуі: Cax SуOz ∙
x : у : z =  :
:  :
:  = 0,58: 0,58: 2,32 : 1,16 = 1: 1 :4 : 2 Жауабы:CaSO4 ∙ 2 H2O
= 0,58: 0,58: 2,32 : 1,16 = 1: 1 :4 : 2 Жауабы:CaSO4 ∙ 2 H2O






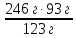 = 186 г
= 186 г =
=  ∙ 100%
∙ 100%  ∙ 100% = 96.8%
∙ 100% = 96.8%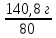 ∙ 100% = 176 г
∙ 100% = 176 г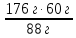 = 120 г
= 120 г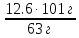 = 20.2 г Жауабы: 20,2 г калий нитраты түзіледі.
= 20.2 г Жауабы: 20,2 г калий нитраты түзіледі.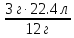 = 5.6 л
= 5.6 л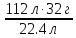 = 160 г
= 160 г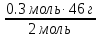 = 6.9 г
= 6.9 г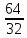 =32 г
=32 г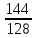 = 36 г
= 36 г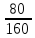 = 125 г
= 125 г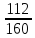 = 147 г
= 147 г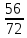 = 70 г
= 70 г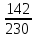 = 1,5 г
= 1,5 г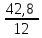 :
: 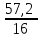 = 3,6 : 3,6 = 1: 1
= 3,6 : 3,6 = 1: 1 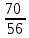 :
: 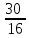 = 1,25 : 1,875 =
= 1,25 : 1,875 =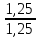 :
: 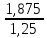 1: 1,5 = 2:3
1: 1,5 = 2:3









