Сульфат натрия в водном растворе диссоциирует
Na2SO4 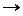 2Na+ + SO42-
2Na+ + SO42-
Так как натрий относится к первой группе металлов, то на катоде будет восстанавливаться водород из молекулы воды. На катоде выделяется водород, в прикатодном пространстве образуется гидроксид натрия.
На катоде (-): 4Н2О + 4е 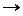 2Н2 + 4ОН-
2Н2 + 4ОН-
SO42- - анион кислородсодержащий, следовательно на аноде будет окисляться кислород из молекулы воды. На аноде выделяется кислород, в прианодном пространстве образуется серная кислота.
На аноде (+): 2Н2О – 4е 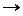 О2 + 4Н+
О2 + 4Н+
Таким образом, электролиз водного раствора сульфата натрия сводится к разложению воды на водород и кислород. В приведённых примерах используется инертный нерастворимый анод. В этом случае он выполняет единственную функцию – является передатчиком электронов.
Однако металлические аноды могут быть растворимыми. Растворимые аноды в растворах соответствующих солей под влиянием внешнего источника тока отдают свои собственные электроны и превращаются в положительно заряженные ионы, которые переходят в раствор
Me0 – nē → Men+
Кристаллическая решётка при этом разрушается. Такой процесс называется анодным растворением металла







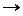 2Na+ + SO42-
2Na+ + SO42-









