
Изопроцессы и их графики. Газовые законы

Цель
Понять и проанализировать поведение газов в процессе изопроцессов, а также научиться интерпретировать графики, иллюстрирующие их.

Задачи
Определить основные параметры изопроцессов; Изучить три типа изопроцессов; Создать графики для каждого из типа процессов; Применить универсальный газовый закон к конкретным задачам.

Проблема
Недостаток представления о термодинамических процессах и их значении для понимания поведения газов.

Введение в термодинамику
Термодинамика изучает тепловые процессы и поведение веществ. Важная часть - газовые изопроцессы, где сохраняется один макропараметр. Основные типы: изотермический (постоянная температура), изобарный (постоянное давление) и изохорный (постоянный объем). Графическое представление газовых законов упрощает восприятие и решение задач. Мы изучим универсальный газовый закон и его практическое применение. Также рассмотрим проблемы обучения термодинамике и пути их решения.

Определение и особенности изопроцессов
Изопроцессы - термодинамические процессы с неизменным макропараметром (давление, объем или температура). Основные виды: изобарный (p = const), изохорный (V = const), изотермический (T = const). Изобарный процесс иллюстрируется законом Гей-Люссака, изохорный - законом Шарля, изотермический - законом Бойля-Мариотта. Эти процессы помогают понять влияние фиксированных параметров на теплообмен и работу в системах, что актуально как в теоретической, так и практической физике.

Изотермический процесс
Изотермический процесс происходит при постоянной температуре, где изменение объема газа влечет за собой изменение давления (PV = nRT). На P-V диаграммах этот процесс изображается гиперболами. Работа, выполняемая газом при сжатии или расширении, определяется интегралом по изменению объема. Исследование этих процессов имеет практическое применение, например, в холодильниках и кондиционерах, и важно для оптимизации инженерных решений.
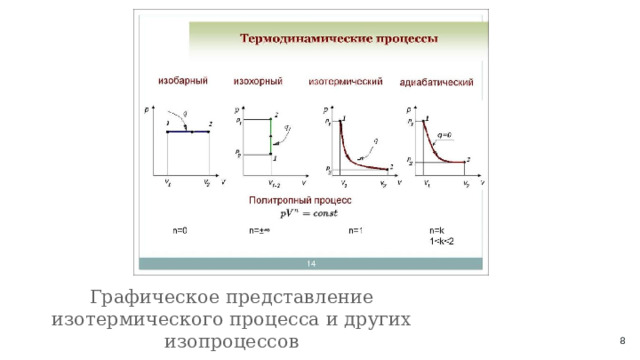
Графическое представление изотермического процесса и других изопроцессов

Графическое представление изотермического процесса и других изопроцессов

Изобарный процесс
Изобарный процесс сохраняет постоянное давление газа, изменяя объем и температуру. Он подчиняется закону Бойля-Мариотта, и на графике представлен горизонтальной линией. В процессе происходит работа газа, связанная с изменением объема, что учитывает первый закон термодинамики. Применение этих знаний важно в инженерии, таких как тепловые машины и холодильные системы.

Графическое представление изобарного процесса и его характеристики

Изохорный процесс
Изохорный процесс – это изменение температуры и давления газа при фиксированном объеме, где работа равна нулю. Он описывается уравнением состояния идеального газа: PV = nRT. При увеличении давления температура газа также возрастает, что визуализируется на линейных графиках зависимости P от T. Важно учитывать безопасность при резком нагреве газа и его применение в газовых системах. Изучение изохорных процессов актуально для физики, химии и инженерии, способствуя развитию технологий и энергоэффективных систем.
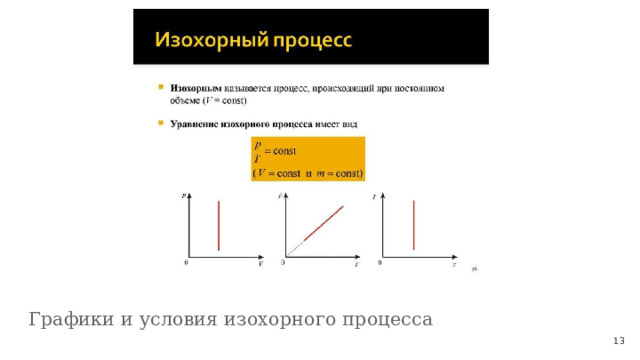
Графики и условия изохорного процесса
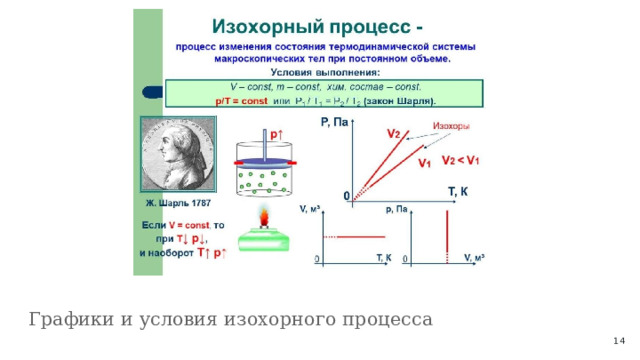
Графики и условия изохорного процесса

Графическое представление газовых законов
Газовые законы, включая изотермические, изобарные и изохорные процессы, визуализируются на графиках. Изотермический процесс (p-V график) показывает гиперболу с зависимостью pV=const. Изобарный процесс представлен прямой линией (V-T график) при постоянном давлении, а изохорный процесс — вертикальной линией (p-V график) с изменением давления при фиксированном объеме. Эти графики визуализируют взаимосвязи между температурой, давлением и объемом газа, что способствует более глубокому пониманию термодинамики.
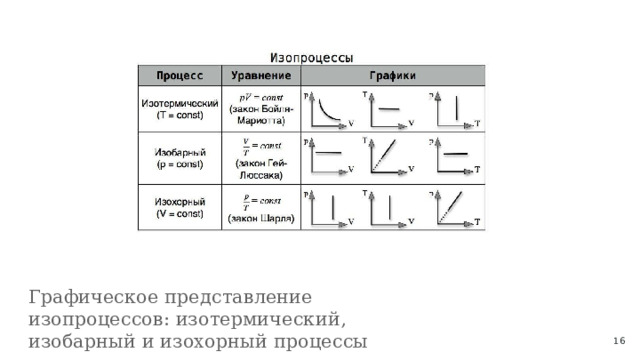
Графическое представление изопроцессов: изотермический, изобарный и изохорный процессы

Применение универсального газового закона
Универсальный газовый закон систематизирует поведение идеальных газов, объединяя законы Бойля, Шарля и Авогадро. Он описывает взаимосвязь давления, объема и температуры (PV=nRT), что критично для термодинамики. Применяется в изотермических, изобарных и изохорных процессах. При анализе газовых смесей этот закон адаптируется для каждого компонента. Задачи на его применение развивают наши практические навыки и помогают избежать ошибок при моделировании термодинамических процессов.

Проблемы обучения термодинамике
Обучение термодинамике в высшем образовании сталкивается с рядом проблем: недостаток практического применения теории, предвзятости восприятия и необходимость адаптации учебных программ. Проблемное обучение и практические кейсы помогают нам осваивать материал, связывая теорию с реальными примерами. Обновление учебных программ и использование научных методов также критичны для обучения. Создание учебного пространства для экспериментов улучшает понимание термодинамических процессов и мотивирует нас.

Заключение
Моё исследование изопроцессов и газовых законов подчеркивает их важность для понимания поведения газов. Я рассмотрел основные параметры и ключевые типы изопроцессов: изотермический, изобарный и изохорный. Графики помогают визуализировать теоретические аспекты и облегчают усвоение материала. Использование универсального газового закона делает анализ процессов более практичным. Важно развивать новые методы обучения для преодоления трудностей в понимании термодинамики.

Список литературы
1. Изопроцессы – Википедия, доступ: https://ru.wikipedia.org/wiki/изопроцессы
2. Первый закон термодинамики для изопроцессов, доступ: https://obrazovaka.ru/fizika/pervyy-zakon-termodinamiki-dlya-izoprocessov-primenenie.html
3. Газовые законы. Изопроцессы 10 класс, доступ: https://lc.rt.ru/classbook/fizika-10-klass/osnovy-molekulyarno-kineticheskoi-teorii/6169
...28. Подходы, ориентированные на студентов, в преподавании, доступ: https://tr-page.yandex.ru/translate?lang=en-ru&url=https://pubs.rsc.org/en/content/articlehtml/2016/rp/c6rp00049e.





































