
Карбоновые кислоты
Параграф 15 страница 76
Рис. 43 стр. 77 представители

Карбоновые кислоты – это органические вещества, в молекулах которых имеется одна или несколько карбоксильных групп – СООН, связанная с радикалом предельного углеводорода.
RCOOOH или C n H 2n+1 COOH

Домашнее задание: подготовить сообщение органические кислоты в природе и на производстве
Химический диктант
Выучить
гомологический ряд предельных карбоновых кислот (первых 5)
формулу бензойной кислоты
Формулы: Акриловой, олеиновой, линолевой и линоленовой
Формулы стеариновой и пальмитиновой (высшие насыщенные КК)

Строение
Атом углерода в карбоксильной группе, так же как и в карбонильной SP 2 -гибридизован.

Физические свойства
Атомы кислорода и водорода в карбоксильной группе способны образовывать межмолекулярные водородные связи.
- имеют высокие температуры кипения и плавления
- при нормальных условиях существуют в жидком или твердом агрегатном состоянии.

Номенклатура стр. 78 Таблица 7
Название радикала + окончание «-овая» + «кислота»

Изомерия
- Изомерия углеродного скелета
- Межклассовая изомерия со сложными эфирами.
2-метилпропановая (изомасляная)
кислота
Бутановая (масляная) кислота

Классификация
В зависимости от строения углеводородного радикала (R):
- предельные (насыщенные): пентановая, пальмитиновая, стеариновая.
- непредельные (ненасыщенные): линолевая, линоленовая, олеиновая.
- Ароматические: бензойная

Сорбиновая (2,4-гексадиеновая) кислота
СН 3 –СН=СН–СН=СНСООН была получена из ягод рябины. Используется как консервант
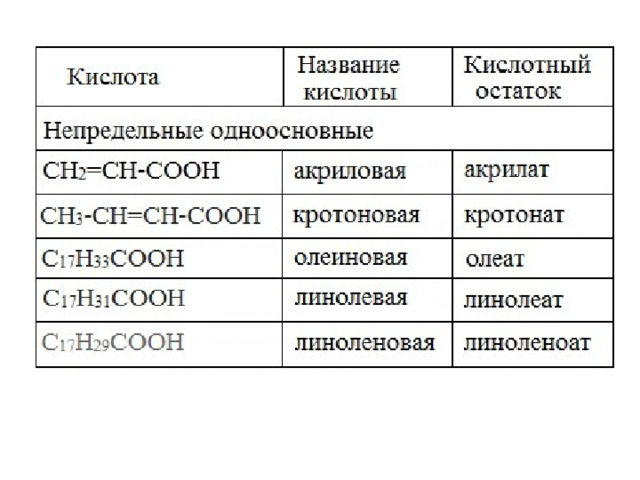

Линолевая кислота C 17 H 31 COOH и линоленовая кислота C 17 H 29 COOH входят в состав растительных масел.
Например, льняное масло содержит около 25% линолевой кислоты и до 58% линоленовой.

Получение
В промышленности:
1. Окисление альдегидов.
2RCHO + O 2 2RCOOH
Лабораторные окислители: Ag 2 O, Cu(OH) 2 , KMnO 4 , K 2 Cr 2 O 7 и др.
2. Окисление спиртов:
RCH 2 OH + O 2 RCOOH + H 2 O
t, кат.
t, Cu



Окисление спиртов
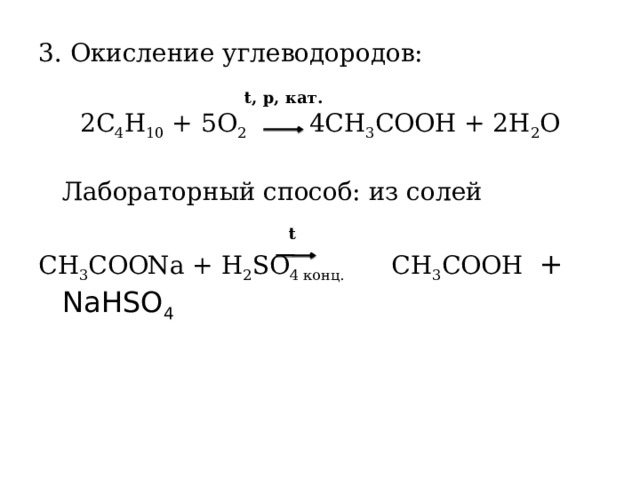
3. Окисление углеводородов:
2C 4 H 10 + 5O 2 4CH 3 COOH + 2H 2 O
Лабораторный способ: из солей
CH 3 COONa + H 2 SO 4 конц. CH 3 COOH + NaHSO 4
t, p, кат.
t

Химические свойства карбоновых кислот

Предельные и непредельные КК

Сила кислот
- С увеличением числа атомов углерода сила кислот убывает:
HCOOH CH 3 COOH C 2 H 5 COOH
- Введение атомов галогена в углеводородный радикал приводит к возрастанию силы кислоты:
CH 3 COOH CH 2 ClCOOH CHCl 2 COOH CCl 3 COOH
монохлоруксусная
уксусная
кислота
кислота
трихлоруксусная
кислота
дихлоруксусная
кислота

Химические свойства
1. Горение
CH 3 COOH + 2O 2 2CO 2 + 2H 2 O

2. Кислотные свойства
Карбоновые кислоты проявляют все свойства, присущие слабым неорганическим кислотам:
А. Диссоциируют в воде:
HCOOH HCOO - + H +
*Все карбоновые кислоты - слабые электролиты

Среда растворов – кислая
рН
лакмус: синий → красный
метилоранж: оранжевый →красный (розовый)

Б. С металлами до водорода:
Mg + 2CH 3 COOH (CH 3 COO) 2 Mg + H 2
В. С основными оксидами:
CaO + 2CH 3 COOH (CH 3 COO) 2 Ca + H 2 O
Г. С основаниями:
NaOH + CH 3 COOH CH 3 COONa + H 2 O
Д. С солями более слабых кислот:
K 2 CO 3 + 2CH 3 COOH 2CH 3 COOK + H 2 O + CO 2
(качественная реакция!)

3. Этерификация (образование сложного эфира):

В реакцию этерификации могут вступать и многоатомные спирты, например, глицерин

4. Замещение в углеводородном радикале:
5. С аммиачным раствором оксида серебра (только муравьиная кислота!)
HCOOH + Ag 2 O(аммиачный раствор) CO 2 + H 2 O + 2Ag
t

6. Декарбоксилирование солей карбоновых кислот.
CH 3 CH 2 COONa + NaOH C 2 H 6 + Na 2 CO 3
сплавление

Закрепление материала
1)Олеиновая кислота:
а. предельная одноосновная
б. предельная двухосновная
в. предельная одноосновная
г. непредельная двухосновная

Закрепление материала
2) Изомером пентановой кислоты является:
а. диэтиловый эфир
б. пропилацетат
в. пентаналь
г. этилацетат

Закрепление материала
3) В отличии от уксусной муравьиная кислота
а. вступает в реакцию со щелочью
б. образует сложные эфиры со спиртами
в. вступает в реакцию с аммиачным раствором оксида серебра
г. реагирует с кальцием















































