Комитет образования ЕАО
Областное государственное профессиональное образовательное бюджетное учреждение
«Сельскохозяйственный техникум»
Методическая разработка урока
по химии
«Мир органических кислот»

Разработала: преподаватель химии Л.В Аленникова
c. Ленинское, 2014 Предмет:
химия Тема урока:
Мир органических кислот Продолжительность:
1 час Группа:
1 курс «Мастер с/х производства» Тип урока: изучение нового учебного материала.
Технология: формирования ключевых компетентностей.
Цель урока:
Обучающие: Дать представление о гомологическом ряде, изомерии, номенклатуре, физических и химических свойствах и применении предельных одноосновных карбоновых кислот. Познакомить учащихся с отдельными представителями карбоновых кислот, показать их значение в природе и жизни человека.
Развивающие: развитие познавательных интересов, коммуникативных качеств, уверенности в своих силах.
Воспитательные: воспитывать культуру общения, внимание, инициативу, воспитание культуры умственного труда.
Оборудование: модель молекулы уксусной кислоты, образцы уксусной, бензойной, стеариновой кислот, компьютер, медиапроектор, распечатки материалов, алгоритмы. Презентация урока (Приложение 1)
Структура урока:
Организационный момент. Психологический настрой.
Изучение новой темы.
Закрепление изученного материала.
Контроль знаний.
Выполнение творческого задания.
Домашнее задание.
Выводы по теме урока. (ИОУЗ). Рефлексия занятия.
Ход урока
1. Вступительное слово учителя.
2. Изучение новой темы.
Объяснение темы происходит с применением презентации через медиапроектор. (Для организации понимания используются слайды, на которых через схематизацию объясняется НУМ.) Проблематизация осуществляется через историческую справку.
С давних времен люди использовали приправы для придания пище кислого вкуса. С этой целью использовались листья щавеля, стебли ревеня, сок лимона, ягоды кислицы. Разумеется, тогда никто и не думал о том, что кислый вкус во всех случаях обусловлен присутствием соединений одного класса. Вопрос: как называют класс веществ, образующихся при окислении альдегидов? (Слайд № 1, 2 учащиеся отвечают на вопрос и записывают в общем виде уравнение реакции получения карбоновых кислот в блок «Способ получения» (Слайд № 3)

Давайте ребята заполним с вами «Лист развития» 1 и 2 столбики, а 3 в конце урока: Что мы знаем о кислотах и что мы хотим узнать о них?
(Слайд№ 4)
(Слайд № 5) Благодаря работам выдающегося шведского химика Карла Вильгельма Шееле к концу 18 века стало известно около десяти различных органических кислот. Он выделил и описал лимонную, молочную, щавелевую и другие кислоты.
Беляев Павел подготовил презентацию о нахождении карбоновых кислот в природе. (Показ презентации). (Приложение 2)
Характеристика карбоновых кислот.
Вопрос: подумайте, что же объединяет такие разные по происхождению и нахождению в природе органические кислоты?
Учащиеся сами определяют, что в составе соединений данного класса имеется —СООН карбоксильная группа. (Приложение 3)
(Слайд № 6) Учитель обобщает сказанное учащимися, дает определение карбоновых кислот и объясняет этимологию термина «карбоксильная группа» как сочетание названий карбонильной и гидроксильной групп.
Давайте вместе сформулируем понятие «карбоновые кислоты».
Карбоновые кислоты — это органические соединения, молекулы которых содержат карбоксильную группу —СООН, связанную с углеводородным радикалом.
(Слайд № 7)Учащиеся записывают общую формулу карбоновых кислот в соответствующий блок в схеме «Характеристика карбоновых кислот».
Поясняю, что радикал в молекуле кислоты может быть предельным, непредельным и ароматическим. Учащиеся дополняют запись в блоке «Общая формула и особенности строения» в схеме «Характеристика карбоновых кислот».

(Слайд № 8) Выполните задание: расставьте формулы и названия кислот согласно данной классификации: олеиновая кислота С17Н33СООН, стеариновая кислота С17Н35СООН, линолевая кислота С17Н31СООН, пальмитиновая кислота С15Н31СООН, уксусная кислота СН3СООН, бензойная кислота С6Н5СООН, муравьиная кислота НСООН на соответствующие им места в схеме:
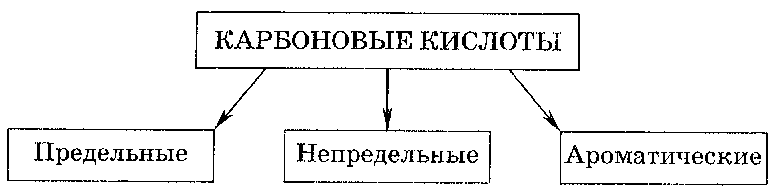
Обращаем внимание, что кислоты, содержащие больше 10 атомов углерода, называют высшими карбоновыми кислотами. Отмечаем это в блоке «Общая формула и особенности строения» в схеме «Характеристика кислот».
(Слайд № 9) Обсуждаем классификацию карбоновых кислот по основности — числу карбоксильных групп. Рассказываем, что карбоновые кислоты могут содержать не одну, а две и более карбоксильные группы, например щавелевая кислота НООС—СООН.
Для закрепления материала о составе карбоновых кислот учащиеся (фронтально) устно выполняют задание с использованием мини-тренажера «Кислородсодержащие органические соединения», (приложение 4) найдите в варианте 1 формулы карбоновых кислот и объясните, почему выбранные вами соединения относят к этому классу органических соединений).
Демонстрируем образцы карбоновых кислот муравьиной, уксусной, стеариновой и предлагаем ответить на вопрос: в каких агрегатных состояниях находятся карбоновые кислоты при обычных условиях? (Слайд № 10)
Физические свойства:
НСООН — бесцветная жидкость с резким запахом, растворяется в воде, пары раздражают дыхательные пути, жидкая кислота вызывает на коже ожоги. СН3СООН — бесцветная жидкость с резким запахом, растворяется в воде, может вызывать раздражение слизистых оболочек, при концентрации растворов более 30% - ожоги.
С17Н35СООН — бесцветные кристаллы, не растворяются в воде.
С17Н33СООН — жидкость, не растворяется в воде
С увеличением количества атомов (С), увеличивается температура кипения карбоновых кислот. (Техника безопасности)
Предлагаем составить структурные формулы молекул первых четырех представителей гомологического ряда предельных одноосновных кислот, имеющих линейную цепочку атомов углерода. (Слайд № 11)
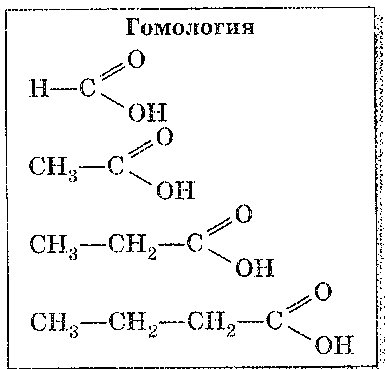
Обсуждаем вопрос: начиная с какой из карбоновых кислот возможно существование изомеров? Учащиеся записывают структурные формулы изомеров в блок «Изомерия». (Слайд № 12)
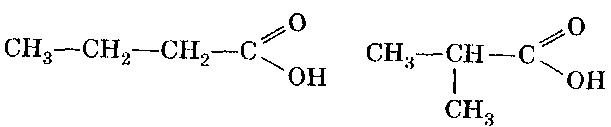
Как называют такой тип изомерии? Учащиеся отмечают на схеме, что данные соединения являются изомерами углеродного скелета.
Для закрепления знаний о гомологии и об изомерии карбоновых кислот учащиеся выполняют устно задание: (Слайд № 13)
1 . Какие из веществ, формулы которых приведены, являются: а) изомерами; б) гомологами?
. Какие из веществ, формулы которых приведены, являются: а) изомерами; б) гомологами?
2. Назовите все вещества по международной номенклатуре ИЮПАК, формулы которых даны. (При составлении международных названий кислот карбоксильный атом углерода всегда получает первый номер).
Обсуждаем вопрос: чем в первую очередь определяются химические свойства карбоновых кислот? Обобщая ответы учащихся, формулируем вывод: химические свойства карбоновых кислот обусловлены наличием в их молекулах карбоксильной группы.
Такие химические свойства карбоновых кислот, как изменение окраски индикаторов, взаимодействие с металлами, основными и амфотерными оксидами, основаниями, амфотерными гидроксидами и солями учащиеся просматривают с помощью видео опыт «Свойства уксусной кислоты». Уравнения реакций учащиеся записывают в схему
| Химические свойства |
| Характеристика реакции, уравнение реакции | Признаки реакции |
| Диссоциация: RCOOH ↔ RCOО- + Н+ (Слайд № 14) | Карбоновые кислоты очень слабые. Лакмус — красный, метилоранж — розовый |
| Взаимодействие с металлами, находящимися в электрохимическом ряду напряжений металлов до водорода: 2СН3СООН + Zn → (CH3COO)2Zn + Н2 (Слайд № 15) | Выделяется газ (водород) |
| Взаимодействие с основными и амфотерными оксидами: а) 2СН3СООН + MgO → (CH3COO)2Mg + Н2О; б) 2СН3СООН + ZnO → (CH3COO)2Zn + Н2О (Слайд № 16) | а) Оксид растворяется; б) оксид растворяется |
| Взаимодействие с гидроксидами металлов: СН3СООН + NaOH → CH3COONa + Н2О (Слайд № 18) | а) Изменяется окраска индикатора; б)осадок растворяется |
| Взаимодействие с солями: а) 2СН3СООН + Na2CО3 → 2CH3COONa + Н2О + СО2↑; б) 2СН3СООН + Na2SiО3 → 2CH3COONa + H2SiО3↓ (Слайд № 17) | а) Выделяется углекислый газ; б) образуется студенистый осадок |
Реакция этерификации — взаимодействие карбоновых кислот со спиртами — уже знакома учащимся, поэтому предлагаем записать ее в схему в общем виде и вспомнить, для чего используют эту реакцию. Обсуждаем условия проведения реакции.
| Реакция этерификации: R−СООН + НО−R ↔ R−СООR + Н2О (Слайд № 19) | Используется для получения сложных эфиров |
3. Для закрепления свойств учащиеся решают тест фронтально. (Приложение 5)
(Слайд № 20 – 57)
4. Контроль знаний. (решают тест индивидуально)- приложение 6
5. Проверка задания творческого уровня.
Любое изучаемое вещество интересно своим применением, об этом нам расскажет в своей презентации Бережнов Владислав. (Показ презентации)
6. Домашнее задание
Выучить тривиальные названия шести первых карбоновых кислот.
Записать возможные изомеры для пентановой кислоты, назвать их - на оценку “4”
Записать возможные изомеры для гексановой кислоты, назвать их - на оценку “5”
Индивидуальные задания (к уроку «Углеводы. Моносахариды»). Подготовить сообщения: «Углеводы в природе. Их значение в жизни человека», «Пентозы: рибоза и дезоксирибоза», «Фруктоза: нахождение в природе, физические свойства и применение».
7. Выводы по теме урока, итоги урока.
В конце урока учитель подводит его итог. Оценивается работа учащихся, где учитывается оригинальность и полнота подачи материала. Вернемся к приложению № 1 – 3 столбик, что же мы сегодня нового узнали на уроке?) Ответы учащихся. (Слайд № 58, 59)
8











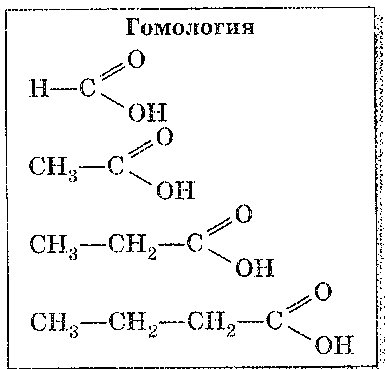

 . Какие из веществ, формулы которых приведены, являются: а) изомерами; б) гомологами?
. Какие из веществ, формулы которых приведены, являются: а) изомерами; б) гомологами?