Просмотр содержимого документа
«Карбоновые кислоты»

Карбоновые кислоты
Выполнила:
Шергина Ольга Ивановна
учитель химии
МКОУ «Нижнеполевская СОШ
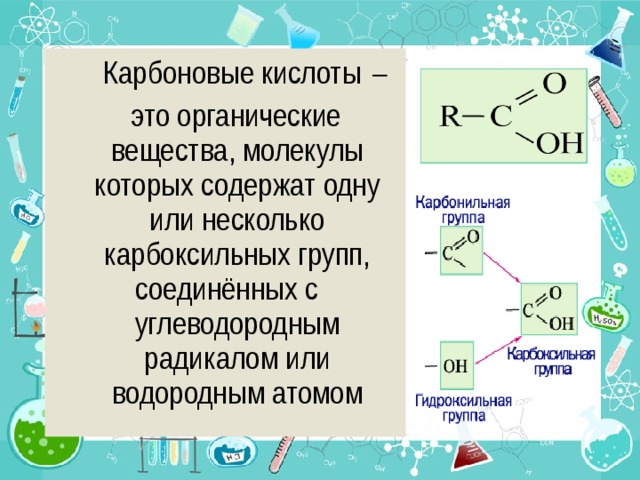
Карбоновые кислоты –
это органические вещества, молекулы которых содержат одну или несколько карбоксильных групп, соединённых с углеводородным радикалом или водородным атомом
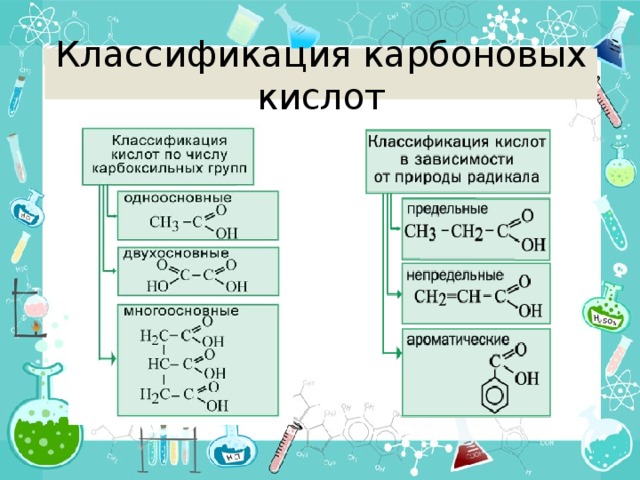
Классификация карбоновых кислот

Взаимное влияние атомов в молекуле
атомов углерода, кислорода и водорода. Атом углерода карбонильной группы приобретает некоторый положительный заряд (электронная плотность сдвигается от него в сторону атома кислорода карбонильной группы). В результате этот атом углерода притягивает к себе электронную пару от атома кислорода гидроксильной группы.
Гидроксильная группа в молекуле связана с карбонильной группой. Ослабление связи между кислородом и водородом объясняется разностью электроотрицательностей

Взаимное влияние атомов в молекуле
Компенсируя смещённую
электронную плотность,
атом кислорода
гидроксильной группы
оттягивает к себе
электронную пару
соседнего атома водорода. Вследствие этого связь между атомами кислорода и водорода в гидроксильной группе становится более полярной и атом водорода приобретает большую подвижность.

Номенклатура
- Название карбоновой кислоты образуется от названия соответствующего алкана с добавлением суффикса –ов, окончания -ая и слова кислота . Нумерация атомов углерода начинается с карбоксильной группы.
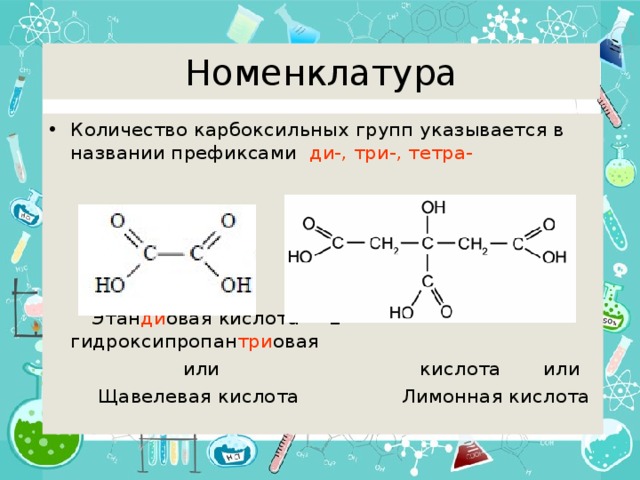
Номенклатура
- Количество карбоксильных групп указывается в названии префиксами ди-, три-, тетра-
Этан ди овая кислота 2-гидроксипропан три овая
или кислота или
Щавелевая кислота Лимонная кислота

Номенклатура
Многие кислоты имеют
исторически
сложившиеся, или
тривиальные, названия.

Изомерия предельных одноосновных карбоновых кислот
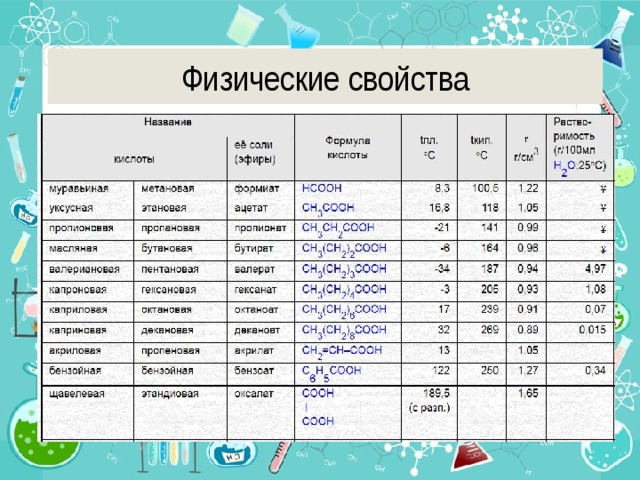
Физические свойства

Общие химические свойства карбоновых кислот
Обусловлены наличием гидроксильной группы:
- Растворимые в воде органические кислоты диссоциируют с образованием катионов водорода и анионов кислотного остатка:
CH ₃ -COOH ↔ CH ₃ -COO¯ + H ⁺
- Взаимодействуют с металлами, стоящими в электрохимическом ряду напряжений до водорода: 2CH ₃ -COOH + 2Na = 2CH ₃ -COONa + H ₂

Общие химические свойства карбоновых кислот
Карбоновые кислоты взаимодействуют:
- с основными и амфотерными оксидами с образованием соли и воды:
2CH ₃ COOH + СaO = (CH ₃ COO) ₂ Ca + H ₂ O
- с гидроксидами металлов с образованием соли и воды (реакция нейтрализации):
CH ₃ COOH + NaOH = CH ₃ COONa +H ₂ O
- С солями более слабых кислот, с образованием последних:
2CH ₃ COOH+K ₂ CO ₃ =2CH ₃ COOK+CO ₂↑ + H ₂ O

Химические свойства карбоновых кислот
- Карбоновые кислоты взаимодействуют со спиртами с образованием сложных эфиров (реакция этерификации):
CH ₃ COOH+ С ₂H₅OH = CH ₃ CO-O- С ₂H₅ + H ₂ O
- могут образовывать ангидриды в присутствии катализатора (P ₂O₅):
2 CH ₃ COOH → СH₃ - C – O - C- СH₃ + H ₂ O
II II
O O
ангидрид уксусной кислоты

Специфические химические свойства
- Наличие в молекуле предельных одноосновных карбоновых кислот радикала обуславливает взаимодействие с галогенами:

Специфические химические свойства
- Муравьиная кислота является самой сильной кислотой из карбоновых кислот;
- Легко окисляется в присутствии аммиачного раствора оксида серебра, подобно альдегидам, (реакция «серебряного зеркала»):
- При нагревании с концентрированной серной кислотой муравьиная кислота отщепляет воду и образует оксид углерода (II):

Применение уксусной кислоты

































