
ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА
ПЛАН
1. Введение. Основные понятия.
2. 1 закон термодинамики. Внутренняя энергия. Энтальпия.
3. Второй закон термодинамики. Энтропия.
4. Изобарно-изотермический потенциал, его связь с константой химического равновесия.
5. Применение термодинамических функций в термохимических расчетах.

1807г. Томас Юнг: «энергия ≡ внутренняя работа»,
Юлиус Майер и Джеймс Прескот Джоуль: теплота работа
1840г. Герман Иванович Гесс: энергетические эффекты химических реакций
XIX ВЕК, ТЕРМОДИНАМИКА сформировалась как фундаментальная наука, изучающая законы превращения энергии, которым сопровождаются
ВСЕ ВСЕ ВСЕ!!!! Физические и химические процессы.
Математическая оценка возможности самопроизвольного протекания процесса и изменения термодинамических параметров системы

СИСТЕМА – совокупность материальных объектов, отделенных от окружающей среды границей:
изолированные закрытые открытые
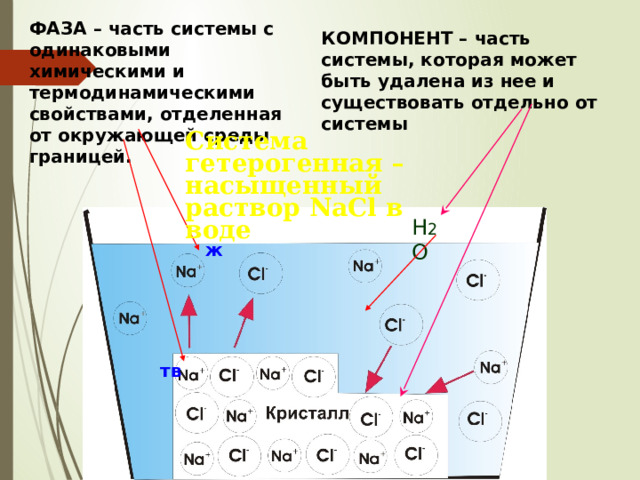
ФАЗА – часть системы с одинаковыми химическими и термодинамическими свойствами, отделенная от окружающей среды границей.
КОМПОНЕНТ – часть системы, которая может быть удалена из нее и существовать отдельно от системы
Система гетерогенная – насыщенный раствор NaCl в воде
Н 2 О
ж
тв

Состояние системы – совокупность всех физических и химических свойств системы; может быть описано количественно с помощью параметров состояния.
Пример: уравнение состояния идеального газа (Менделеева-Клапейрона)
pV = RT
СОСТОЯНИЕ РАВНОВЕСИЯ – состояние, которое остается неизменным во времени при отсутствии каких-либо измене-ний окружающей среды; параметры состояния одинаковы во всех точках системы.
СТАЦИОНАРНОЕ СОСТОЯНИЕ – состояние, которое остается неизменным во времени только за счет некоторых изменений в окружающей среде.
БЕЗРАЗЛИЧНОЕ РАВНОВЕСИЕ
УСТОЙЧИВОЕ РАВНОВЕСИЕ
НЕУСТОЙЧИВОЕ РАВНОВЕСИЕ
 0 Работа осуществляется над системой А Q не может самопроизвольно переходить в А А может самопроизвольно переходить в Q " width="640"
0 Работа осуществляется над системой А Q не может самопроизвольно переходить в А А может самопроизвольно переходить в Q " width="640"
I закон термодинамики Q = ΔU + А:
в общем случае поступившая в систему извне тепловая энергия (Q) может быть частично израсходована на изменение внутренней энергии системы ( Δ U), а частично – на выполнение работы (A).
Работа – направленное упорядоченное движение молекул и ионов (движение молекул расширяющегося газа, движение ионов в батарейке) .
Теплота (теплопередача, теплоперенос) – хаотическое движение молекул и ионов.
Работу выполняет система А 0
Работа осуществляется над системой А
Q не может самопроизвольно переходить в А
А может самопроизвольно переходить в Q

Внутренняя энергия – энергия химических связей внутри молекул, энергия межмолекулярного взаимодействия, кинетическая энергия поступательного, колебательного и вращательного движения молекул.
Пример: в закрытом сосуде
Н 2 О (ж) → Н 2 О (пар) при 100 о С Q=540 кал
1 г
499 кал – на U :
На преодоление водородных связей и сил межмолекулярного притяжения
Только 41 кал – на совершение А против атмосферного давления
 Н 1 , то Δ Н0, тепло поглощается, реакция эндотермическая. Изменение энтальпии системы в процессе образования 1 моля сложного вещества из простых веществ - энтальпия образования данного вещества (кДж/моль, Δ f Н). Для простых веществ Δ f Н принята равной 0. Например, выражение «энтальпия образования жидкой воды равна -285,8 кДж/моль» означает, что при образовании 1 моля жидкой воды (18 г) по уравнению Н 2 +1/2 О 2 = Н 2 О из 2 г Н 2 и 8 г О 2 выделяется 285,8 кДж тепловой энергии. Стандартное состояние: 298К и 101325Па стандартная энтальпия образования Δ f Н 0 . Так энтальпия образования водяного пара из водорода и кислорода равна -241,8 кДж/моль. Разность между значениями энтальпий образования жидкой и парообразной воды представляет собой энтальпию процесса испарения жидкой воды. " width="640"
Н 1 , то Δ Н0, тепло поглощается, реакция эндотермическая. Изменение энтальпии системы в процессе образования 1 моля сложного вещества из простых веществ - энтальпия образования данного вещества (кДж/моль, Δ f Н). Для простых веществ Δ f Н принята равной 0. Например, выражение «энтальпия образования жидкой воды равна -285,8 кДж/моль» означает, что при образовании 1 моля жидкой воды (18 г) по уравнению Н 2 +1/2 О 2 = Н 2 О из 2 г Н 2 и 8 г О 2 выделяется 285,8 кДж тепловой энергии. Стандартное состояние: 298К и 101325Па стандартная энтальпия образования Δ f Н 0 . Так энтальпия образования водяного пара из водорода и кислорода равна -241,8 кДж/моль. Разность между значениями энтальпий образования жидкой и парообразной воды представляет собой энтальпию процесса испарения жидкой воды. " width="640"
Для Р = const (изобарный процесс) : ΔU = U 2 -U 1 = Q P - А = Q Р - Р(V 2 – V 1 )
Q P = (U 2 + РV 2 ) - ( U 1 + РV 1 ), Q P – тепло, поступившее в систему при постоянном давлении,
U + РV ≡ Н – энтальпия системы .
Таким образом, при изменении состояния системы в изобарном процессе происходит изменение энтальпии системы: Q P = Н 2 – Н 1 , причем
если Н 2 1 , то Δ Н
если Н 2 Н 1 , то Δ Н0, тепло поглощается, реакция эндотермическая.
Изменение энтальпии системы в процессе образования 1 моля сложного вещества из простых веществ - энтальпия образования данного вещества (кДж/моль, Δ f Н). Для простых веществ Δ f Н принята равной 0. Например, выражение «энтальпия образования жидкой воды равна -285,8 кДж/моль» означает, что при образовании 1 моля жидкой воды (18 г) по уравнению
Н 2 +1/2 О 2 = Н 2 О
из 2 г Н 2 и 8 г О 2 выделяется 285,8 кДж тепловой энергии.
Стандартное состояние: 298К и 101325Па стандартная энтальпия образования
Δ f Н 0 . Так энтальпия образования водяного пара из водорода и кислорода равна -241,8 кДж/моль. Разность между значениями энтальпий образования жидкой и парообразной воды представляет собой энтальпию процесса испарения жидкой воды.

II закон термодинамики (аксиома):
Самопроизвольно могут протекать только те процессы, в которых система переходит из менее вероятного состояния (с большей внутренней энергией) в более вероятное (с меньшей внутренней энергией)
Процесс самопроизвольный, если он осуществляется без каких-либо воздействий со стороны окружающей среды. Например, газ может самопроизвольно расширяться, но не может самопроизвольно сжиматься в локальном объеме пространства. Направленное и упорядоченное движение молекул может самопроизвольно перейти в хаотическое движение, но обратный процесс не может происходить самопроизвольно, а только при воздействии на систему извне.
Количественная мера термодинамической вероятности состояния ( w ) – число микросостояний, которыми можно реализовать данное макросостояние.
Для N молекул в системе
w = X N
Х – количество микросостояний
1 микросостояние
2 микросостояние
Одно макросостояние – твердый сплав
 ΔQ/Т Л. Больцман (1844 – 1906) Для индивидуального кристаллического вещества при абсолютном нуле (0 К) S=0. Энтропия как мера связанной энергии характеризует ту часть энергии, которая не превращается в работу. Чем выше энтропия, тем выше теплота Q=ST и тем больше хаотическое движение молекул и рассеивание энергии и ниже работоспособность системы. Р.Д.Э. Клаузиус (1822 – 1888) " width="640"
ΔQ/Т Л. Больцман (1844 – 1906) Для индивидуального кристаллического вещества при абсолютном нуле (0 К) S=0. Энтропия как мера связанной энергии характеризует ту часть энергии, которая не превращается в работу. Чем выше энтропия, тем выше теплота Q=ST и тем больше хаотическое движение молекул и рассеивание энергии и ниже работоспособность системы. Р.Д.Э. Клаузиус (1822 – 1888) " width="640"
ln (w) = ln (X N ) Х≡S = k • ln w, S - энтропия
В изолированных системах самопроизвольно могут протекать только такие процессы, в результате которых энтропия увеличивается и ΔS ˃ 0.
1850г., Клаузиус, энтропия – для характеристики потерянной тепловой энергии при работе теплового двигателя.
ΔS=ΔQ/Т –для равновесного обратимого изотермического процесса ( ΔQ/Т – приведенная теплота, кДж\(моль • К))
Для неравновесного и необратимого процесса: ΔS ΔQ/Т
Л. Больцман
(1844 – 1906)
Для индивидуального кристаллического вещества при абсолютном нуле (0 К) S=0.
Энтропия как мера связанной энергии характеризует ту часть энергии, которая не превращается в работу. Чем выше энтропия, тем выше теплота Q=ST и тем больше хаотическое движение молекул и рассеивание энергии и ниже работоспособность системы.
Р.Д.Э. Клаузиус (1822 – 1888)
 0!!! " width="640"
0!!! " width="640"
Энтропия как мера неупорядоченности в системе . Увеличение энтропии связано с усилением хаотического движения молекул, атомов и ионов. Это и понятно, ведь чтобы молекулы двигались быстрее и дальше, они должны обладать большим запасом энергии, а энтропия – это тоже энергия! Следовательно, рост энтропии связан с увеличением неупорядоченности (хаотичности) в системе. Например, в кристалле льда молекулы более упорядочены, чем в жидкой воде; две жидкости, отделенные одна от другой (т.е.несмешивающиеся), более упорядочены, чем их гомогенная смесь.
S тв S ж S г
ЭНТРОПИЯ УВЕЛИЧИВАЕТСЯ!!! И Δ S 0!!!
 0 (ЭНЕРГИЯ УВЕЛИЧИВАЕТСЯ), ПРОЦЕСС НЕ МОЖЕТ ПРОТЕКАТЬ САМОПРОИЗВОЛЬНО Δ f G 0 – энергия Гиббса образования 1 моль вещества из простых веществ в стандартных условиях, кДж\моль " width="640"
0 (ЭНЕРГИЯ УВЕЛИЧИВАЕТСЯ), ПРОЦЕСС НЕ МОЖЕТ ПРОТЕКАТЬ САМОПРОИЗВОЛЬНО Δ f G 0 – энергия Гиббса образования 1 моль вещества из простых веществ в стандартных условиях, кДж\моль " width="640"
ОТКРЫТЫЕ СИСТЕМЫ (биологические, живые организмы): Δ S
ПРОТИВОРЕЧИЕ II закону?
Свободная энергия, энергия Гиббса, изобарно-изотермический потенциал:
G =Н-ТS или ΔG = ΔН - ТΔS - только для состояний при P=const и T=const
Д.У. Гиббс (1839 – 1903)
ЕСЛИ В ПРОЦЕССЕ:
ΔG =0 , СИСТЕМА НАХОДИТСЯ В РАВНОВЕСИИ
ΔG (ЭНЕРГИЯ УМЕНЬШАЕТСЯ), ПРОЦЕСС МОЖЕТ ПРОТЕКАТЬ САМОПРОИЗВОЛЬНО
ΔG 0 (ЭНЕРГИЯ УВЕЛИЧИВАЕТСЯ), ПРОЦЕСС НЕ МОЖЕТ ПРОТЕКАТЬ САМОПРОИЗВОЛЬНО
Δ f G 0 – энергия Гиббса образования 1 моль вещества из простых веществ в стандартных условиях, кДж\моль
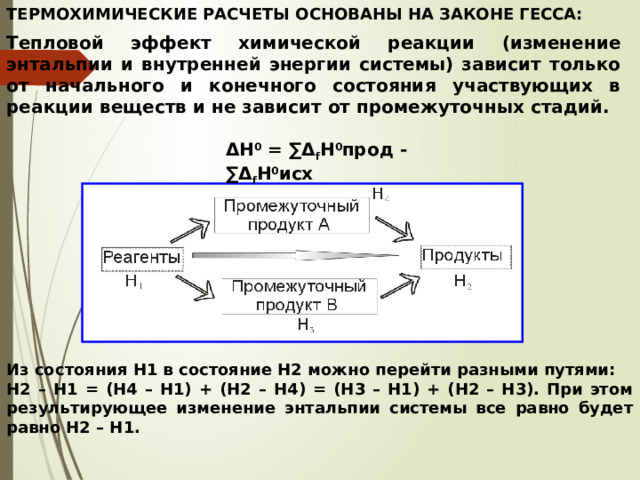
ТЕРМОХИМИЧЕСКИЕ РАСЧЕТЫ ОСНОВАНЫ НА ЗАКОНЕ ГЕССА:
Тепловой эффект химической реакции (изменение энтальпии и внутренней энергии системы) зависит только от начального и конечного состояния участвующих в реакции веществ и не зависит от промежуточных стадий.
ΔH 0 = ∑Δ f H 0 прод - ∑Δ f H 0 исх
Из состояния Н1 в состояние Н2 можно перейти разными путями:
Н2 – Н1 = (Н4 – Н1) + (Н2 – Н4) = (Н3 – Н1) + (Н2 – Н3). При этом результирующее изменение энтальпии системы все равно будет равно Н2 – Н1.

С + О 2 = СO 2 + Q 1 = -Δ Н 1
С+ 1/2О 2 =СО+Q 2 = -ΔН 2
СО+ 1/2 О 2 =СO 2 +Qз = -ΔН З
СО
Δ Н2
Δ Н3
СО 2
С
Δ Н1
Δ Н1 = Δ Н2 + Δ Н3

Термохимические уравнения сгорания:
(1) С (графит) + О 2 (г) → СО 2 (г) Н 0 = - 394,1 кДж
(2) С (алмаз) + О 2 (г) → СО 2 (г) Н 0 = - 396,0 кДж
Вычтем (2) из (1) и получим:
С (графит) – С(алмаз) = 0, Н 0 = +1,9 кДж С(графит) → С(алмаз), Н 0 = +1,9кДж
С(алмаз) → С(графит), Н 0 = - 1,9кДж
самопроизвольно
ВЫВОД:
1. ЛЮБАЯ СИСТЕМА ПРИ ИЗМЕНЕНИИ УСЛОВИЙ ЕЕ СУЩЕСТВОВАНИЯ (ВОЗДЕЙСТВИЕ ИЗ-ВНЕ) ПЕРЕСТРАИВАЕТСЯ (ИЗМЕНЯЕТСЯ) ТАКИМ ОБРАЗОМ, ЧТО УМЕНЬШАЕТСЯ ЕЕ СВОБОДНАЯ ЭНЕРГИЯ G ( Δ G
ΔG = ΔН - ТΔS
2. ПРИ ДАННОЙ ТЕМПЕРАТУРЕ СВОБОДНАЯ ЭНЕРГИЯ СИСТЕМЫ МОЖЕТ БЫТЬ УМЕНЬШЕНА:
- ЛИБО ЗА СЧЕТ УМЕНЬШЕНИЯ ЭНТАЛЬПИИ (ВНУТРЕННЕЙ ЭНЕРГИИ) СИСТЕМЫ
- ЛИБО ЗА СЧЕТ УВЕЛИЧЕНИЯ ЭНТРОПИИ СИСТЕМЫ.











 0 Работа осуществляется над системой А Q не может самопроизвольно переходить в А А может самопроизвольно переходить в Q " width="640"
0 Работа осуществляется над системой А Q не может самопроизвольно переходить в А А может самопроизвольно переходить в Q " width="640"

 Н 1 , то Δ Н0, тепло поглощается, реакция эндотермическая. Изменение энтальпии системы в процессе образования 1 моля сложного вещества из простых веществ - энтальпия образования данного вещества (кДж/моль, Δ f Н). Для простых веществ Δ f Н принята равной 0. Например, выражение «энтальпия образования жидкой воды равна -285,8 кДж/моль» означает, что при образовании 1 моля жидкой воды (18 г) по уравнению Н 2 +1/2 О 2 = Н 2 О из 2 г Н 2 и 8 г О 2 выделяется 285,8 кДж тепловой энергии. Стандартное состояние: 298К и 101325Па стандартная энтальпия образования Δ f Н 0 . Так энтальпия образования водяного пара из водорода и кислорода равна -241,8 кДж/моль. Разность между значениями энтальпий образования жидкой и парообразной воды представляет собой энтальпию процесса испарения жидкой воды. " width="640"
Н 1 , то Δ Н0, тепло поглощается, реакция эндотермическая. Изменение энтальпии системы в процессе образования 1 моля сложного вещества из простых веществ - энтальпия образования данного вещества (кДж/моль, Δ f Н). Для простых веществ Δ f Н принята равной 0. Например, выражение «энтальпия образования жидкой воды равна -285,8 кДж/моль» означает, что при образовании 1 моля жидкой воды (18 г) по уравнению Н 2 +1/2 О 2 = Н 2 О из 2 г Н 2 и 8 г О 2 выделяется 285,8 кДж тепловой энергии. Стандартное состояние: 298К и 101325Па стандартная энтальпия образования Δ f Н 0 . Так энтальпия образования водяного пара из водорода и кислорода равна -241,8 кДж/моль. Разность между значениями энтальпий образования жидкой и парообразной воды представляет собой энтальпию процесса испарения жидкой воды. " width="640"

 ΔQ/Т Л. Больцман (1844 – 1906) Для индивидуального кристаллического вещества при абсолютном нуле (0 К) S=0. Энтропия как мера связанной энергии характеризует ту часть энергии, которая не превращается в работу. Чем выше энтропия, тем выше теплота Q=ST и тем больше хаотическое движение молекул и рассеивание энергии и ниже работоспособность системы. Р.Д.Э. Клаузиус (1822 – 1888) " width="640"
ΔQ/Т Л. Больцман (1844 – 1906) Для индивидуального кристаллического вещества при абсолютном нуле (0 К) S=0. Энтропия как мера связанной энергии характеризует ту часть энергии, которая не превращается в работу. Чем выше энтропия, тем выше теплота Q=ST и тем больше хаотическое движение молекул и рассеивание энергии и ниже работоспособность системы. Р.Д.Э. Клаузиус (1822 – 1888) " width="640"
 0!!! " width="640"
0!!! " width="640"
 0 (ЭНЕРГИЯ УВЕЛИЧИВАЕТСЯ), ПРОЦЕСС НЕ МОЖЕТ ПРОТЕКАТЬ САМОПРОИЗВОЛЬНО Δ f G 0 – энергия Гиббса образования 1 моль вещества из простых веществ в стандартных условиях, кДж\моль " width="640"
0 (ЭНЕРГИЯ УВЕЛИЧИВАЕТСЯ), ПРОЦЕСС НЕ МОЖЕТ ПРОТЕКАТЬ САМОПРОИЗВОЛЬНО Δ f G 0 – энергия Гиббса образования 1 моль вещества из простых веществ в стандартных условиях, кДж\моль " width="640"














